Clear Sky Science · fr
Caractéristiques de l’adsorption du strontium sur les sédiments aquatiques dans le Sud-Ouest de la Chine
Pourquoi ce métal dans la boue compte
Lorsque des métaux lourds atteignent les rivières et les lacs, ils ne s’évaporent pas ; beaucoup se retrouvent collés à la vase au fond. Un de ces métaux est le strontium, qui se comporte de façon similaire au calcium dans nos organismes et peut devenir dangereux lorsque ses isotopes radioactifs sont présents. Cette étude examine comment les sédiments des rivières et des lacs du Sud-Ouest de la Chine retiennent le strontium, et comment la température, la chimie de l’eau et des éléments concurrents comme le calcium déterminent si ce métal reste enfermé dans la vase ou est relâché dans l’eau.
Rivières, lacs et un filet de sécurité invisible
Les chercheurs se sont concentrés sur trois types de sédiments aquatiques prélevés dans une rivière, un ruisseau et un lac de la région de Mianyang, dans la province du Sichuan. Ces sédiments jouent le rôle d’un filet de sécurité invisible : ils peuvent piéger le strontium dissous provenant de l’eau sus-jacente et des nappes phréatiques. L’équipe a mesuré avec soin les propriétés de base des sédiments, notamment leur alcalinité, leur teneur en matière organique et le nombre de sites microscopiques à la surface capables de fixer des particules chargées positivement. Ces sites de surface, largement contrôlés par de fines particules d’argile et de la matière organique, préparent le terrain pour la quantité de strontium que les sédiments peuvent retenir.
Comment les expériences ont été réalisées
Pour sonder le comportement du strontium, les scientifiques ont mené des tests de laboratoire contrôlés appelés expériences d’adsorption par lots. Ils ont agité de petites quantités de sédiment avec de l’eau contenant différents niveaux de strontium, puis mesuré la quantité de métal restant dans l’eau et celle transférée dans le sédiment. Ils ont répété ces tests sur une plage de températures proches des conditions naturelles des rivières et lacs et ajouté différentes concentrations de sel de calcium dissous pour voir à quel point le calcium rivalisait avec le strontium. Ils ont parallèlement suivi de près les variations d’acidité de l’eau (pH), car même de petits changements de pH peuvent faire basculer l’équilibre entre les métaux attachés au sédiment et ceux libres dans l’eau.
Une eau plus chaude et une vase plus riche retiennent plus de strontium
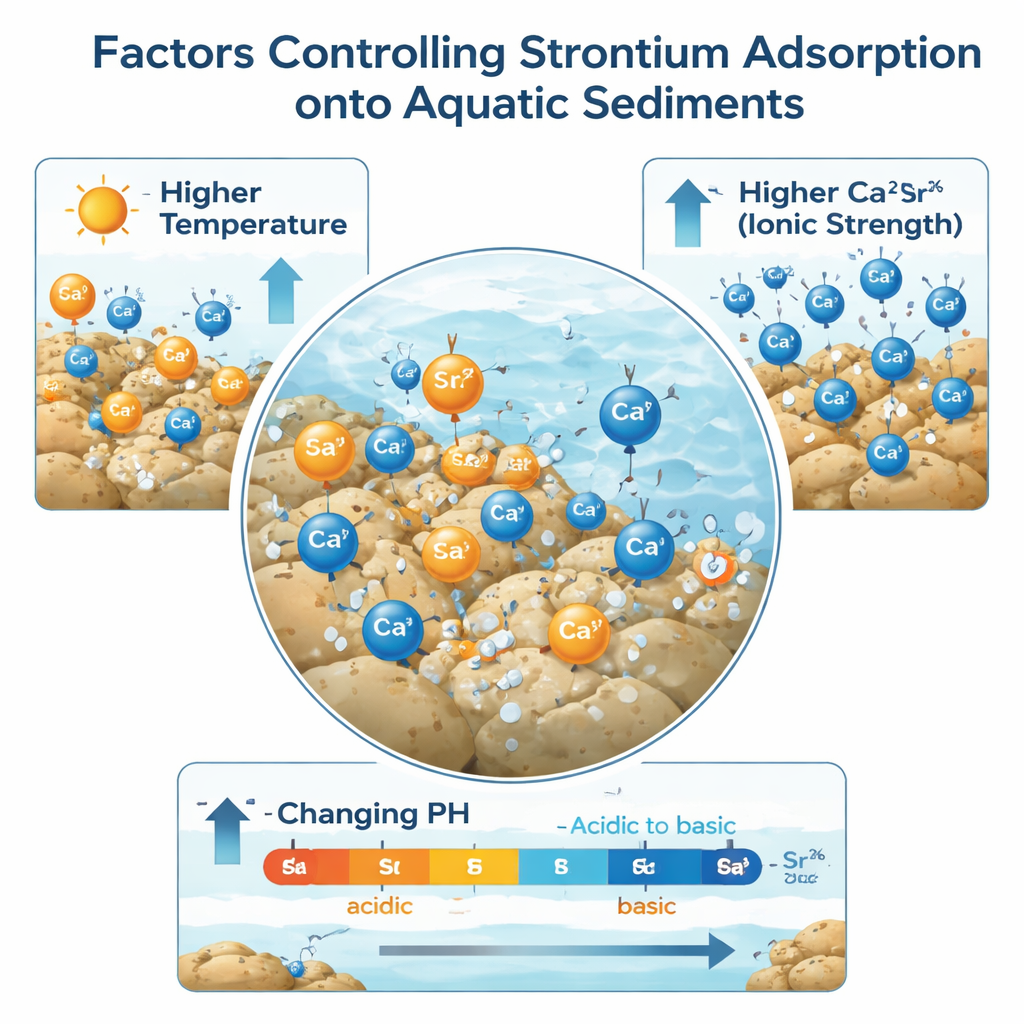
Les résultats montrent que l’adsorption du strontium sur les sédiments suit des schémas bien connus en chimie décrivant la façon dont les surfaces se couvrent. En termes simples, à mesure que l’eau se réchauffe, le sédiment peut retenir davantage de strontium. Sur la plage de températures testée, la quantité maximale de strontium pouvant se fixer au sédiment a augmenté d’environ 1 à 2 fois, selon le site. Des conditions plus chaudes accélèrent le mouvement du strontium dissous et facilitent l’accès des ions aux sites de liaison dans la vase. Parmi les trois sites étudiés, le sédiment lacustre, qui présentait une surface beaucoup plus grande et plus de sites capables d’échanger des charges, a stocké le plus de strontium par unité de masse.
Quand le calcium évince le strontium
Le calcium, proche chimique du strontium, s’est avéré être un rival puissant. Lorsque les chercheurs ont augmenté la concentration de calcium dans l’eau, les sédiments ont adsorbé beaucoup moins de strontium. Aux teneurs en calcium les plus élevées testées, la capacité de certains sédiments à retenir le strontium a chuté d’à près vingt fois. Cela indique que le strontium est souvent retenu par des forces électrostatiques relativement faibles, réversibles en présence d’un grand nombre d’autres ions positifs. L’équipe a également observé qu’à mesure que davantage de strontium était capté, l’eau devenait légèrement plus acide, ce qui suggère que des ions hydrogène étaient libérés lorsque le strontium prenait la place sur les surfaces des sédiments.
pH, efficacité d’élimination et implications pour la sécurité
Même dans la gamme de pH modeste typique des eaux naturelles, l’acidité de la solution a eu un impact net. À mesure que le pH initial des expériences passait d’un léger acidité vers une alcalinité douce, la part de strontium retirée de l’eau augmentait, atteignant environ la moitié du métal éliminé dans les cas les plus favorables. Dans les milieux réels, cela signifie que de modestes changements de la chimie de l’eau — comme une pollution qui acidifie une rivière ou un apport de sels qui augmente les niveaux de calcium — pourraient provoquer la libération dans l’eau d’un strontium auparavant piégé dans les sédiments. Dans l’ensemble, l’étude montre que les sédiments peuvent servir de réservoir temporaire important pour le strontium, mais que leur tenue n’est pas permanente. Comprendre comment la température, le calcium et le pH font pencher cet équilibre aide les scientifiques et les autorités à mieux prédire où le strontium finira et comment concevoir des stratégies de dépollution et de protection des eaux contaminées.
Citation: Luo, X., Zhang, D., Zhou, M. et al. Characteristics of strontium adsorption onto aquatic sediments in Southwest China. Sci Rep 16, 6948 (2026). https://doi.org/10.1038/s41598-026-38190-7
Mots-clés: strontium, sédiments aquatiques, pollution par les métaux lourds, qualité de l’eau, contamination par les radionucléides