Clear Sky Science · fr
Le modèle murin hypoxique « tight-skin » de l’hypertension pulmonaire de groupe 3
Pourquoi cette recherche est importante
L’hypertension pulmonaire est une élévation grave et souvent mortelle de la pression sanguine dans les poumons. L’une de ses formes les plus fréquentes, appelée hypertension pulmonaire de groupe 3, se développe chez les personnes atteintes de maladies pulmonaires chroniques comme l’emphysème ou la fibrose pulmonaire, ou chez celles exposées à une hypoxie prolongée. Pourtant, les médecins manquent encore de traitements ciblés pour cette affection, en partie parce que les chercheurs ne disposaient pas d’un modèle animal reproduisant fidèlement ce qui se passe dans les poumons humains. Cette étude présente un nouveau modèle murin qui ressemble étroitement à la maladie de groupe 3 et révèle une chaîne de signalisation délétère qui pourrait être ciblée par des traitements futurs.
Une souris qui reproduit des poumons endommagés
Les chercheurs se sont intéressés à une souche de souris connue sous le nom de « tight-skin » (Tsk). Ces animaux portent une mutation dans une protéine structurale appelée fibrilline-1. En raison de ce défaut, ils développent naturellement des modifications proches de l’emphysème et des cicatrisations pulmonaires, similaires à celles observées chez des personnes atteintes de maladies pulmonaires chroniques avancées. L’équipe a comparé ces souris à leurs congénères normaux en les maintenant soit dans l’air ambiant, soit en conditions d’hypoxie pendant quatre semaines, pour reproduire le manque d’oxygène chronique que beaucoup de patients humains subissent. 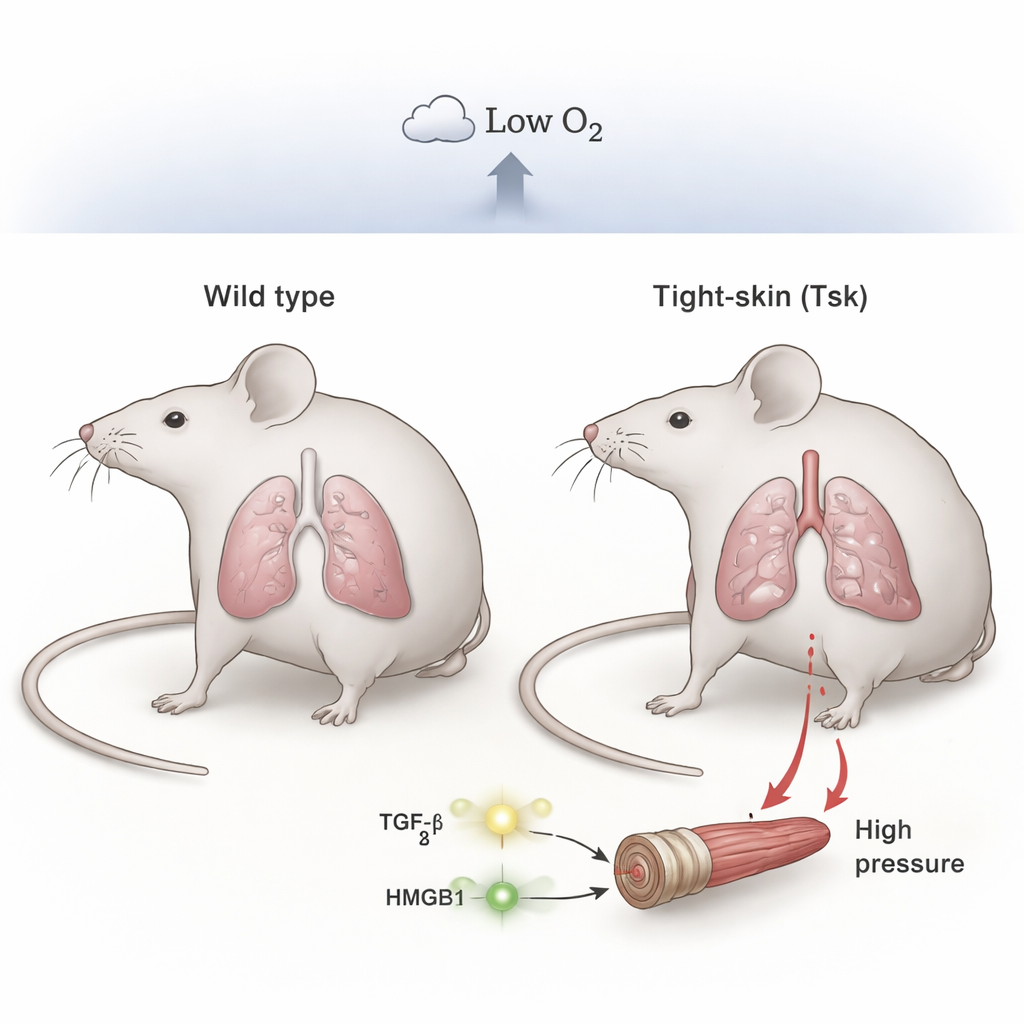
L’hypoxie transforme un poumon vulnérable en poumons à haute pression
Lorsque les souris normales et les souris tight-skin ont été maintenues en atmosphère ambiante, leurs pressions pulmonaires étaient similaires et dans les limites normales. Mais en condition d’hypoxie chronique, les différences étaient frappantes. Les souris normales n’ont développé que des augmentations modérées de pression, tandis que les souris tight-skin ont présenté une hypertension pulmonaire sévère, avec des pressions beaucoup plus élevées dans le côté droit du cœur et un épaississement évident des petites artères pulmonaires. La microscopie a montré des espaces aériens élargis (emphysème) et une forte muscularisation des très petits vaisseaux chez les animaux tight-skin, reflétant de près les lésions structurelles observées chez les patients atteints de la maladie de groupe 3. Cela indique qu’une lésion pulmonaire préexistante combinée à l’hypoxie pousse le système vers un état bien plus dangereux que l’hypoxie seule.
Un signal de danger dans le sang
L’équipe a ensuite cherché pourquoi les souris tight-skin réagissaient si fortement à l’hypoxie. Ils se sont concentrés sur une molécule appelée HMGB1, une protéine « signal de danger » libérée par les cellules stressées ou endommagées. Les souris tight-skin présentaient déjà des taux d’HMGB1 plus élevés dans leur sang au départ, et ces niveaux augmentaient encore pendant l’hypoxie. L’administration d’un petit peptide thérapeutique, P5779, qui bloque l’interaction de HMGB1 avec l’un de ses récepteurs clés (TLR4), a largement empêché le développement d’une hypertension pulmonaire sévère chez les souris tight-skin. Les animaux traités avaient des pressions pulmonaires plus basses, un moindre épaississement des vaisseaux pulmonaires et une moindre dilatation du côté droit du cœur. Ces effets protecteurs étaient bien plus marqués chez les souris tight-skin que chez les souris normales, ce qui désigne HMGB1 comme un amplificateur central de la maladie dans ce modèle.
Comment un signal de croissance alimente le signal de danger
Un autre acteur de cette histoire est le TGF-β, un facteur de croissance associé de longue date à la cicatrisation et au remodelage des poumons malades. Les chercheurs ont constaté que les souris tight-skin avaient une activité basale de TGF-β plus élevée dans leurs poumons, comme le montre l’activation accrue de son messager en aval, SMAD-3, autour des vaisseaux sanguins. Dans des expériences réalisées avec des fibroblastes adventitiels d’artère pulmonaire humaine — des cellules qui constituent la couche externe des vaisseaux — l’ajout de TGF-β augmentait la production de HMGB1. En retour, HMGB1 stimulait la prolifération de ces fibroblastes et des cellules musculaires lisses voisines. Fait important, cet effet prolifératif dépendait du récepteur TLR4 et était bloqué par P5779, mais pas par le blocage d’un autre récepteur de HMGB1 appelé RAGE. Ensemble, ces résultats décrivent une boucle dans laquelle la fibrilline-1 mutante favorise l’activation de TGF-β, TGF-β élève les niveaux d’HMGB1, et HMGB1 stimule la croissance excessive des cellules de la paroi vasculaire qui rétrécit les artères pulmonaires. 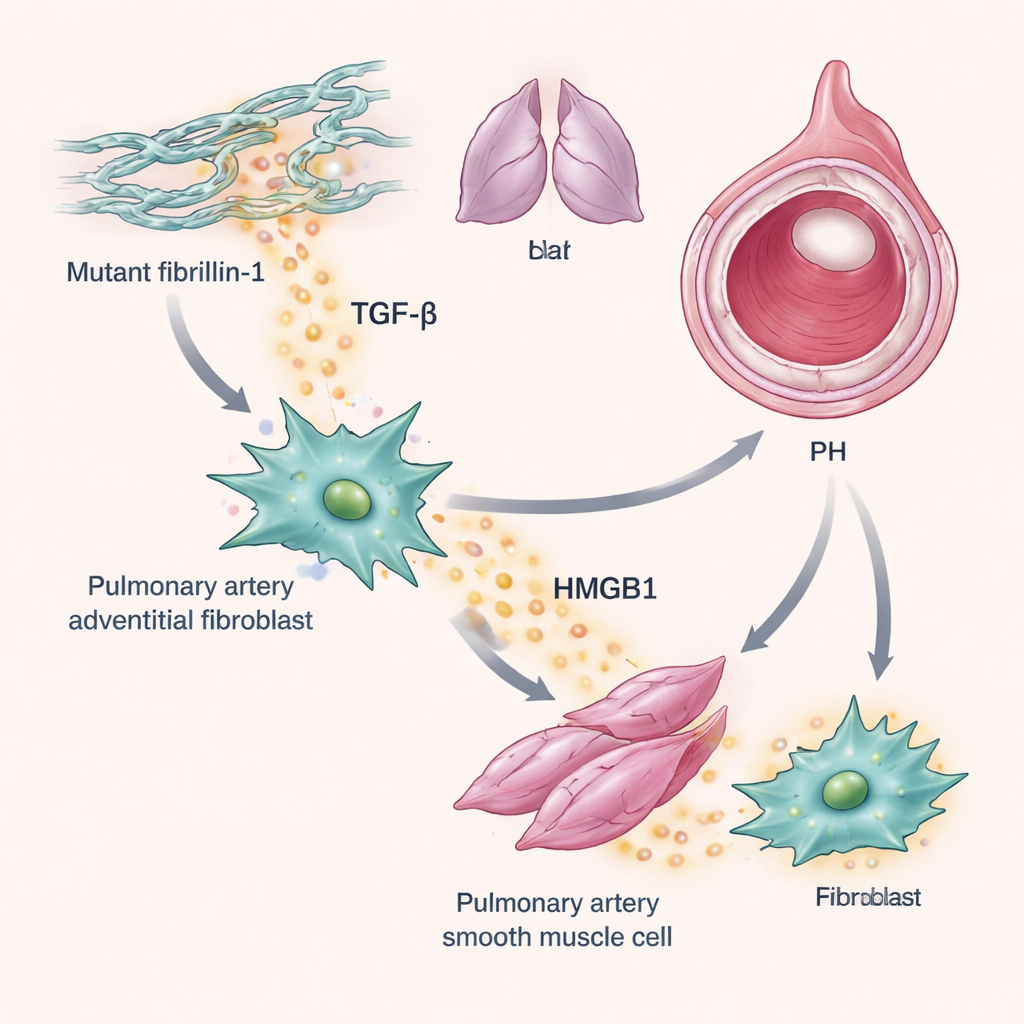
Conséquences pour les patients
En combinant une architecture pulmonaire de type emphysème avec une hypoxie chronique, le modèle murin tight-skin reproduit de nombreuses caractéristiques clés de l’hypertension pulmonaire de groupe 3 que les modèles plus simples basés uniquement sur l’hypoxie ne captent pas. Ce travail met en évidence une voie TGF-β–HMGB1–TLR4 qui transforme des poumons blessés et pauvres en oxygène en poumons à haute pression. Pour les personnes vivant avec une maladie pulmonaire chronique, ces résultats suggèrent de nouvelles pistes thérapeutiques : des médicaments qui atténuent la signalisation TGF-β, ou qui bloquent les interactions HMGB1–TLR4 comme le fait P5779 chez la souris, pourraient un jour aider à prévenir ou ralentir l’élévation de la pression pulmonaire. Le modèle lui-même offre également une nouvelle plateforme puissante pour tester de tels traitements avant leur passage en clinique.
Citation: Chi, L., Foley, A.E., Goodarzi, G. et al. The hypoxic tight-skin mouse model of Group 3 pulmonary hypertension. Sci Rep 16, 6968 (2026). https://doi.org/10.1038/s41598-026-38174-7
Mots-clés: hypertension pulmonaire, maladie pulmonaire chronique, hypoxie, HMGB1, TGF-beta