Clear Sky Science · fr
IL-18 favorise la fibrose pancréatique via la libération d’IL-4 par les cellules étoilées du pancréas et induit la polarisation macrophagique vers M2
Pourquoi la cicatrisation du pancréas est importante
La pancréatite chronique est une inflammation de longue durée du pancréas qui détruit progressivement cet organe vital, provoquant souvent des douleurs sévères, des troubles digestifs et un risque accru de cancer du pancréas. Une caractéristique centrale de la maladie est la fibrose — le tissu cicatriciel qui remplace les cellules pancréatiques saines. Cette étude pose une question simple mais cruciale : quels signaux à l’intérieur du pancréas transforment une inflammation persistante en cicatrisation permanente, et l’inhibition de ces signaux pourrait‑elle ralentir ou arrêter les dommages ?
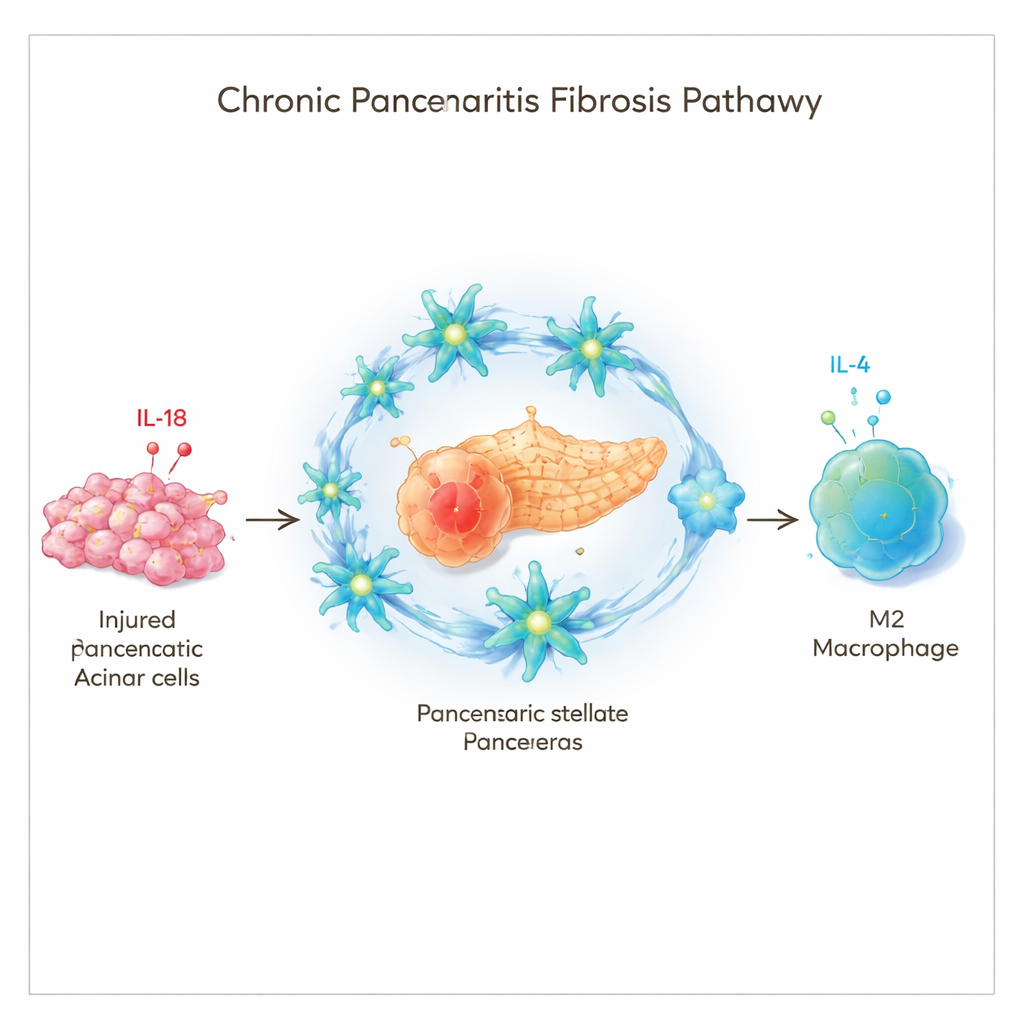
Un signal d’alarme problématique
Les chercheurs se sont concentrés sur une molécule appelée interleukine‑18 (IL‑18), partie du « système d’alarme » immunitaire. L’IL‑18 augmente pendant l’inflammation et a été associée à la fibrose du cœur, des reins et du foie. En analysant des échantillons de tissu de personnes atteintes de pancréatite chronique et en utilisant des modèles murins de la maladie, l’équipe a constaté que les niveaux d’IL‑18 étaient beaucoup plus élevés dans les pancréas malades que dans les pancréas sains. Fait important, plus il y avait d’IL‑18 dans le pancréas d’un patient, plus la fibrose était étendue. Ils ont identifié une source majeure d’IL‑18 dans les cellules acinaires lésées — les cellules productrices d’enzymes digestives du pancréas — qui libèrent de l’IL‑18 lorsqu’elles sont endommagées.
Les cellules de soutien qui se transforment en faiseurs de cicatrices
Le tissu cicatriciel dans la pancréatite chronique est principalement produit par les cellules étoilées du pancréas, un type de cellule de soutien qui est normalement au repos mais peut passer à un état actif formant des cicatrices. L’étude a montré que ces cellules étoilées portent le récepteur de l’IL‑18, ce qui signifie qu’elles peuvent détecter directement ce signal d’alarme. Chez des souris génétiquement dépourvues de ce récepteur, des lésions répétées ont entraîné beaucoup moins de cicatrisation pancréatique, moins d’activation des cellules étoilées et un profil différent d’infiltration des cellules immunitaires. Cela indique que l’IL‑18 n’est pas qu’un simple marqueur de l’inflammation ; c’est un moteur qui pousse les cellules étoilées et les tissus environnants vers la fibrose.
Comment les cellules immunitaires sont orientées vers un mode cicatrisant
Un autre acteur clé dans la pancréatite chronique est le macrophage, une cellule immunitaire qui peut adopter différentes « personnalités ». Dans un état (souvent appelé M1), les macrophages sont des défenseurs agressifs ; dans un autre (M2), ils se tournent vers la remodelage tissulaire et, malheureusement, peuvent favoriser la fibrose. Les scientifiques ont observé que les souris dépourvues du récepteur de l’IL‑18 avaient moins de macrophages de type M2 dans leur pancréas. De manière surprenante, l’IL‑18 seule n’a pas directement converti les macrophages en type M2 en culture. À la place, l’IL‑18 a agi sur les cellules étoilées, les poussant à libérer une autre molécule de signalisation, l’interleukine‑4 (IL‑4). L’IL‑4 est bien connue pour orienter les macrophages vers l’état M2, pro‑fibrose. Lorsque des macrophages ont été exposés au fluide provenant de cellules étoilées traitées par l’IL‑18, ils ont fortement basculé vers le profil M2 — mais cet effet a largement disparu lorsque l’IL‑4 a été bloquée.
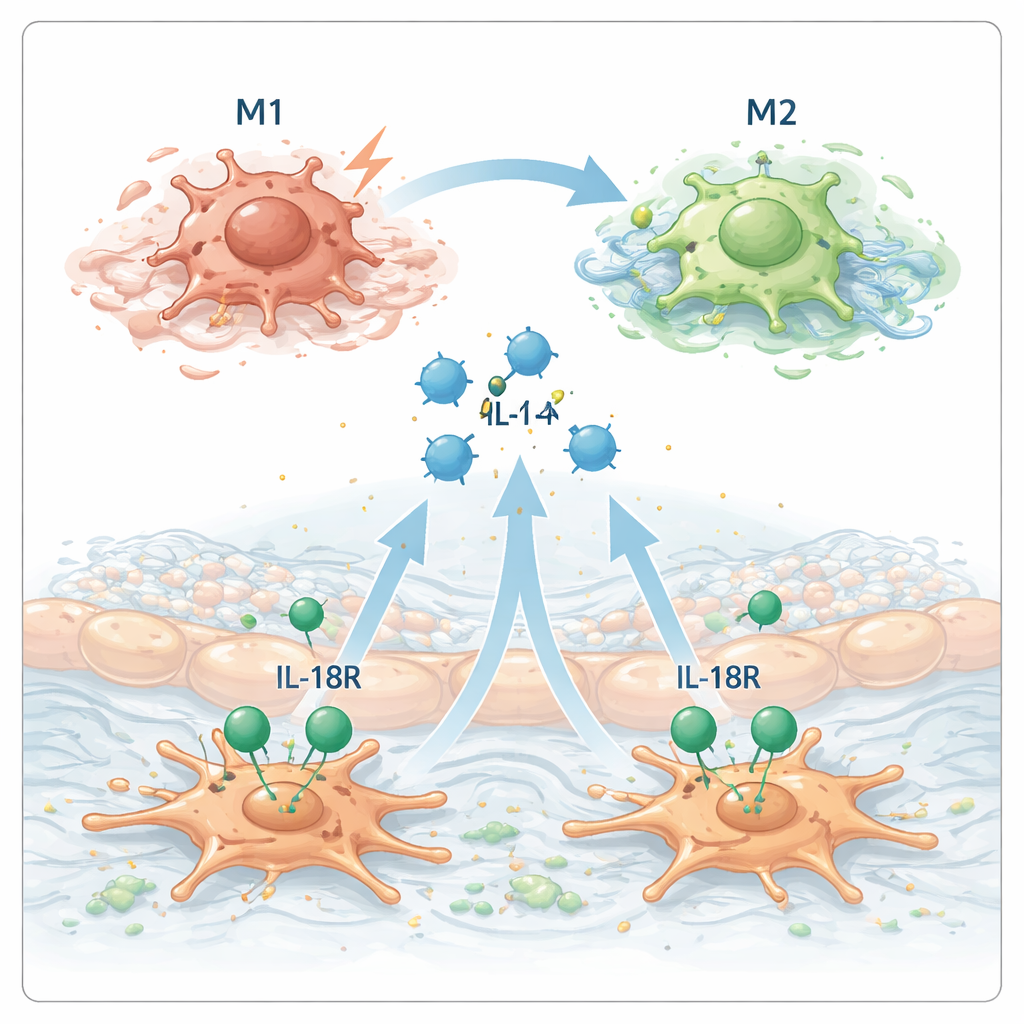
Une réaction en chaîne qui aggrave la cicatrisation
En rassemblant ces éléments, les chercheurs proposent une réaction en chaîne à l’intérieur du pancréas malade. D’abord, les cellules acinaires sont blessées et libèrent de l’IL‑18. Ensuite, l’IL‑18 active les cellules étoilées voisines via son récepteur. En réponse, les cellules étoilées sécrètent de l’IL‑4, qui instruit alors les macrophages à adopter l’état M2 promoteur de cicatrisation. Ces macrophages M2, à leur tour, stimulent davantage les cellules étoilées et favorisent le dépôt de collagène et d’autres composants du tissu cicatriciel, approfondissant la fibrose. Dans des expériences chez la souris, l’administration d’IL‑18 supplémentaire pendant la pancréatite chronique a aggravé la maladie et la cicatrisation, mais le blocage de l’IL‑4 a atténué ces effets néfastes.
Ce que cela signifie pour les traitements futurs
Pour les non‑spécialistes, le message essentiel est que la cicatrisation dans la pancréatite chronique n’est pas aléatoire ; elle est pilotée par une conversation spécifique entre les cellules pancréatiques endommagées, les cellules étoilées et les cellules immunitaires. L’IL‑18 se situe près du sommet de cette chaîne de communication, et l’IL‑4 agit comme un messager intermédiaire clé. En interférant avec l’IL‑18, son récepteur sur les cellules étoilées, ou la signalisation de l’IL‑4 vers les macrophages, des thérapies futures pourraient réduire ou ralentir l’accumulation de tissu cicatriciel dans la pancréatite chronique, préservant potentiellement la fonction pancréatique et améliorant la qualité de vie des patients.
Citation: Tu, G., Peng, C., Xie, S. et al. IL-18 promotes pancreatic fibrosis via release of IL-4 from pancreatic stellate cells and induces macrophage M2 polarization. Sci Rep 16, 7540 (2026). https://doi.org/10.1038/s41598-026-38168-5
Mots-clés: pancréatite chronique, fibrose pancréatique, IL-18, IL-4, polarisation des macrophages