Clear Sky Science · fr
Analyse HPLC–DAD des compléments alimentaires fonctionnels suivie d’une identification par FTIR assistée par microextraction liquide–liquide des ingrédients actifs en IR
Pourquoi il est important de vérifier ce qu’il y a vraiment dans votre boisson
Des boissons pour le sport promettant une récupération musculaire accélérée aux eaux vitaminées censées renforcer l’immunité, les boissons fonctionnelles et les compléments alimentaires sont devenus des produits courants. Pourtant, l’étiquetage ne reflète pas toujours le contenu réel de la bouteille, et des additifs cachés ou des dosages erronés peuvent affecter la santé et les performances. Cette étude décrit une nouvelle approche de laboratoire qui aide les scientifiques et les régulateurs à vérifier la composition chimique réelle de boissons complexes, en combinant des techniques de séparation et d’identification optique pour percer le bruit des sucres, sels et autres ingrédients.
Démêler des listes d’ingrédients surchargées
Les boissons fonctionnelles modernes, comme les boissons contenant des acides aminés à chaîne ramifiée (BCAA), contiennent généralement un cocktail d’ingrédients actifs — des acides aminés tels que la valine, la leucine et l’isoleucine, ainsi que des acides, édulcorants, caféine et vitamines. Identifier chacun de ces composants avec précision n’est pas trivial, car ils sont mélangés dans une « soupe » chimique dense qui inclut aussi des conservateurs, arômes et parfois des contaminants. Les contrôles qualité traditionnels reposent largement sur la chromatographie liquide haute performance (HPLC), qui sépare un échantillon en bandes chimiques individuelles, et sur la spectrométrie de masse, une technique puissante mais coûteuse. Les auteurs explorent ici l’association de la HPLC avec la spectroscopie infrarouge à transformée de Fourier (FTIR), une méthode qui lit l’empreinte infrarouge unique de chaque molécule, pour créer un outil plus accessible pour le contrôle qualité de routine.
Le problème de l’eau et des sels
Bien que la FTIR soit rapide et riche en informations, elle bute lorsqu’on l’utilise directement sur des échantillons liquides issus de systèmes HPLC standards. Le problème tient au fait que l’eau, les solvants organiques courants et particulièrement les sels de tampon dissous absorbent fortement dans l’infrarouge et laissent leurs propres signatures spectrales. Après évaporation de la phase mobile, les cristaux issus des sels de tampon peuvent recouvrir ou déformer complètement le signal des véritables ingrédients. Les auteurs ont d’abord étudié soigneusement l’influence de différentes surfaces de dépôt des échantillons séchés, comme divers métaux et cristaux, sur le signal de fond. Ils ont montré que le simple papier d’aluminium offrait une forte réflexion et un fond relativement propre, en faisant un support simple et efficace pour les mesures ultérieures.
Une microextraction minuscule qui change tout
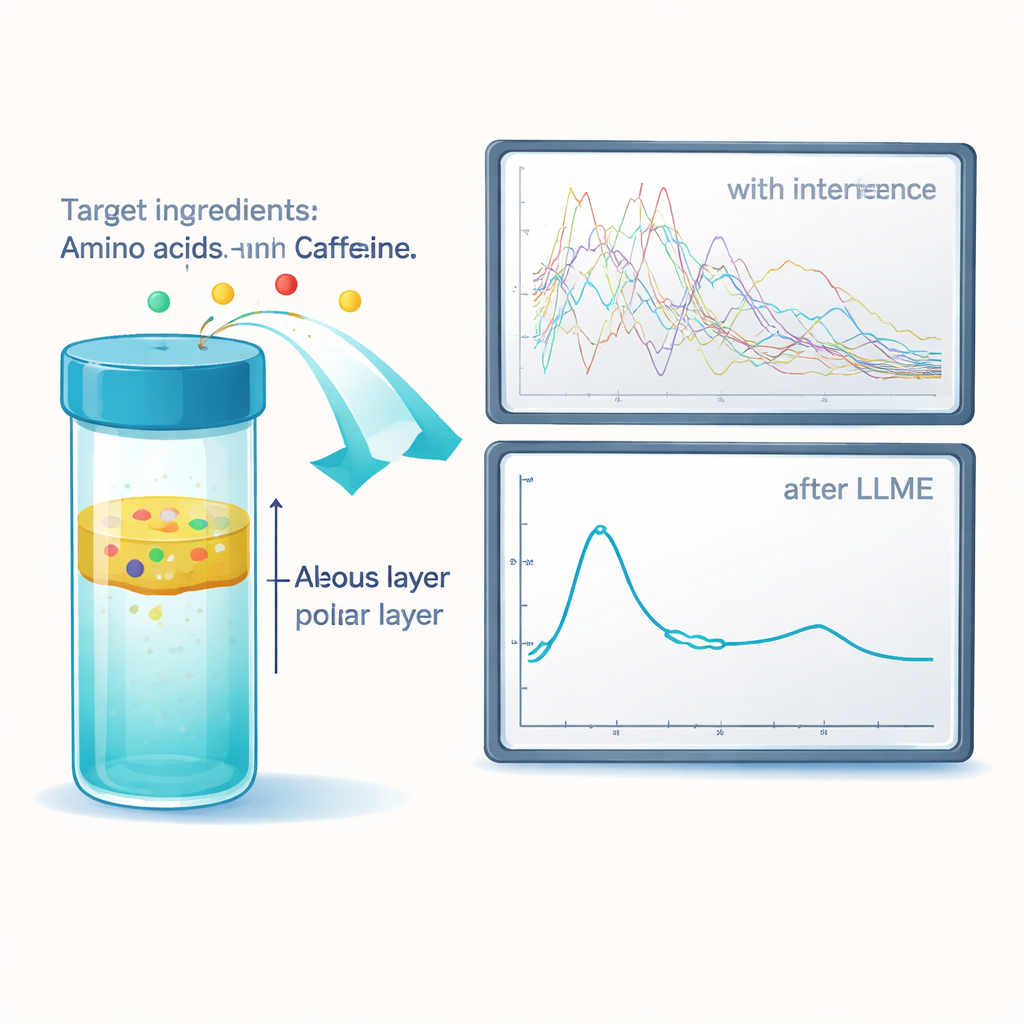
Pour éviter les interférences des solvants et des sels, les chercheurs ont introduit une étape de microextraction liquide–liquide (LLME) entre la HPLC et la FTIR. Dans cette approche, chaque fraction collectée de la HPLC provenant d’une boisson BCAA est mise en contact avec un très faible volume d’un liquide lourd et non polaire qui n’absorbe pas dans la région infrarouge. Lors d’un mélange vigoureux, les ingrédients recherchés migrent de la phase aqueuse vers ce solvant spécial, tandis que la plupart des sels et autres composants gênants restent en arrière. L’équipe a testé plusieurs solvants candidats et a montré que l’un d’eux, un composé fluoré, extrayait de manière fiable suffisamment de chaque ingrédient cible pour fournir des empreintes FTIR nettes. Comparée à la simple évaporation du solvant d’origine, la LLME, seule ou combinée à une évaporation, a produit des spectres bien plus propres, même en présence de mélanges de solvants et de tampons complexes.
Application de la méthode à une boisson sportive réelle
Une fois la technique optimisée, les auteurs se sont tournés vers une boisson BCAA commerciale. Après séparation du contenu par HPLC et nettoyage par LLME, ils ont enregistré les spectres FTIR de chaque fraction purifiée. Les empreintes résultantes leur ont permis d’identifier avec confiance des ingrédients clés, notamment l’acide citrique, la vitamine C (acide L-ascorbique), les trois BCAA (valine, leucine, isoleucine) et la caféine. Fait important, tout cela a été réalisé avec des instruments de laboratoire standard — un système HPLC ordinaire, un microscope FTIR de paillasse et du matériel verrier courant — plutôt qu’avec des équipements hautement spécialisés ou extrêmement coûteux. Cela signifie que la méthode pourrait être adoptée par de nombreux laboratoires de contrôle qualité dépourvus de spectromètres de masse avancés.
Ce que cela signifie pour les consommateurs et les régulateurs
L’étude montre qu’une étape simple ajoutée — la microextraction avec un solvant compatible infrarouge — transforme une énigme analytique difficile en un test de routine gérable. Si la nouvelle méthode HPLC–LLME–FTIR ne remplace pas la spectrométrie de masse de haut niveau pour des analyses ultra-traces ou très détaillées, elle offre une solution pratique et peu coûteuse pour confirmer les principaux ingrédients actifs dans des boissons et compléments complexes et vérifier la véracité des étiquettes. Pour les consommateurs, cela se traduit par de meilleures protections contre les produits trompeurs ; pour les régulateurs et fabricants, cela fournit un outil robuste pour soutenir des marchés plus sûrs et plus transparents pour les aliments fonctionnels, la nutrition sportive et les produits de santé connexes.
Citation: Pavelek, D., Kaykhaii, M., Jampilek, J. et al. HPLC–DAD analysis of functional dietary supplements followed by liquid–liquid microextraction-assisted FTIR identification of IR-active ingredients. Sci Rep 16, 7028 (2026). https://doi.org/10.1038/s41598-026-38160-z
Mots-clés: compléments alimentaires, boissons fonctionnelles, contrôle de qualité, spectroscopie infrarouge, acides aminés à chaîne ramifiée