Clear Sky Science · fr
L'effet potentiel du remplacement par l'albumine sur la modulation immunitaire et la dynamique du sphingosine 1‑phosphate
Pourquoi cela compte pour les patients en soins intensifs
Les personnes en unité de soins intensifs présentent souvent des taux très bas d'une protéine sanguine appelée albumine. Les médecins administrent parfois des perfusions d'albumine en espérant stabiliser la pression artérielle et améliorer la survie, mais les grands essais n'ont pas clairement montré de bénéfice. Cette étude pose une question différente : au‑delà de l'équilibre hydrique, l'albumine pourrait‑elle influencer le système immunitaire en transportant dans le sang une petite molécule lipophile messagère — et cela pourrait‑il expliquer pourquoi certains patients semblent tirer plus d’avantage que d’autres ?
Un examen plus détaillé de l'albumine et d'un petit messager
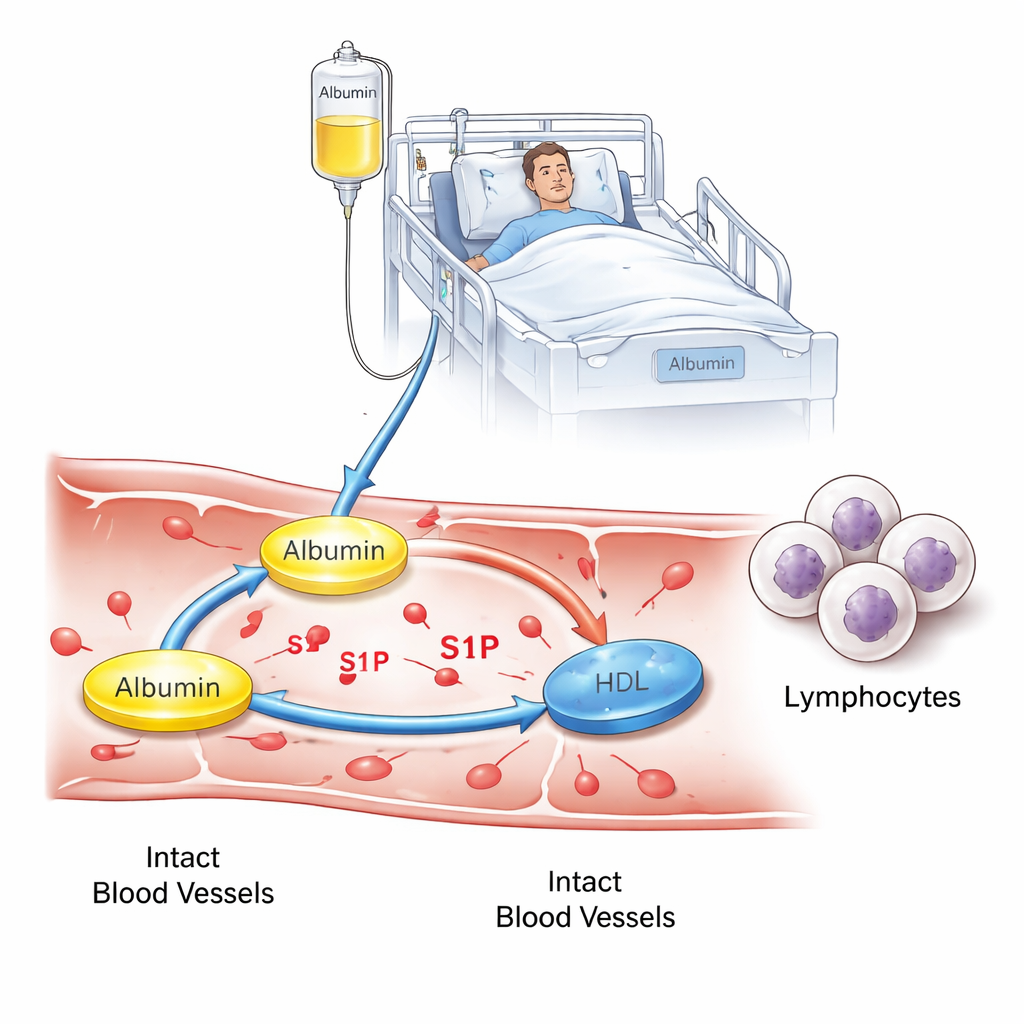
L'albumine ne se contente pas de retenir l'eau dans nos vaisseaux sanguins. Elle transporte aussi de nombreuses petites molécules, dont le sphingosine 1‑phosphate (S1P), qui régule le déplacement des globules blancs dans l'organisme et la perméabilité des vaisseaux en cas de maladie grave. Chez des personnes en bonne santé, le S1P circule principalement lié à deux transporteurs : l'albumine et les lipoprotéines de haute densité (HDL, souvent appelées « bon cholestérol »). Lorsque l'état devient critique — en particulier lors de septicémie — les taux d'albumine et de HDL peuvent chuter, et des travaux antérieurs ont montré que les niveaux de S1P diminuent aussi, ce qui est associé à des issues plus défavorables. Les auteurs ont cherché à tester si l'administration d'albumine humaine aux patients en réanimation présentant une hypoalbuminémie pouvait modifier la répartition du S1P entre albumine et HDL, et si ce déplacement se traduirait par des changements des cellules immunitaires ou de la stabilité vasculaire.
Comment l'étude a été conduite au chevet
L'équipe a suivi 47 adultes dans une seule unité de soins intensifs pendant environ un an. Tous avaient une hypoalbuminémie, mais ce sont les médecins traitants — et non les chercheurs — qui ont décidé qui recevrait une perfusion d'albumine. Sur cette base, les patients ont été répartis en trois groupes : un petit groupe témoin avec albumine normale, un groupe plus large avec hypoalbuminémie qui n'a pas reçu d'albumine, et un groupe traité avec hypoalbuminémie ayant reçu 180 grammes d'albumine humaine sur trois jours. Des prélèvements sanguins ont été effectués pour des analyses biologiques standards, des mesures détaillées du S1P et des décomptes des différents types de globules blancs. Les chercheurs ont aussi utilisé des méthodes spécialisées pour déterminer si le S1P de chaque échantillon était principalement lié à l'albumine ou aux HDL, puis ont réalisé des tests en laboratoire pour voir comment le plasma des patients affectait le déplacement des globules blancs et la cohésion des couches cellulaires endothéliales des vaisseaux.
Ce qui a évolué dans le sang — et ce qui ne l'a pas fait
Comme prévu, les perfusions d'albumine ont nettement augmenté les taux d'albumine sanguine dans le groupe traité, confirmant que le traitement fonctionnait sur un plan basique. De manière surprenante, les concentrations totales de S1P dans le sang n'ont pas augmenté avec la thérapie à l'albumine et sont restées inférieures à celles des patients en réanimation dont l'albumine était normale dès le départ. Le changement important concernait le transporteur : après traitement, une plus grande proportion de S1P était liée à l'albumine et moins aux HDL, montrant une redistribution mesurable entre transporteurs sans modification de la quantité totale. Parallèlement, les effectifs de deux types clés de cellules immunitaires circulantes — les cellules T CD4 et les cellules B — ont diminué au cours des trois jours de traitement. Ce schéma est compatible avec l'idée que l'altération du transport du S1P pourrait modifier la recirculation des cellules immunitaires, même si le dessin de l'étude ne permet pas d'établir une relation causale.
Tester la protection vasculaire et le mouvement cellulaire en laboratoire
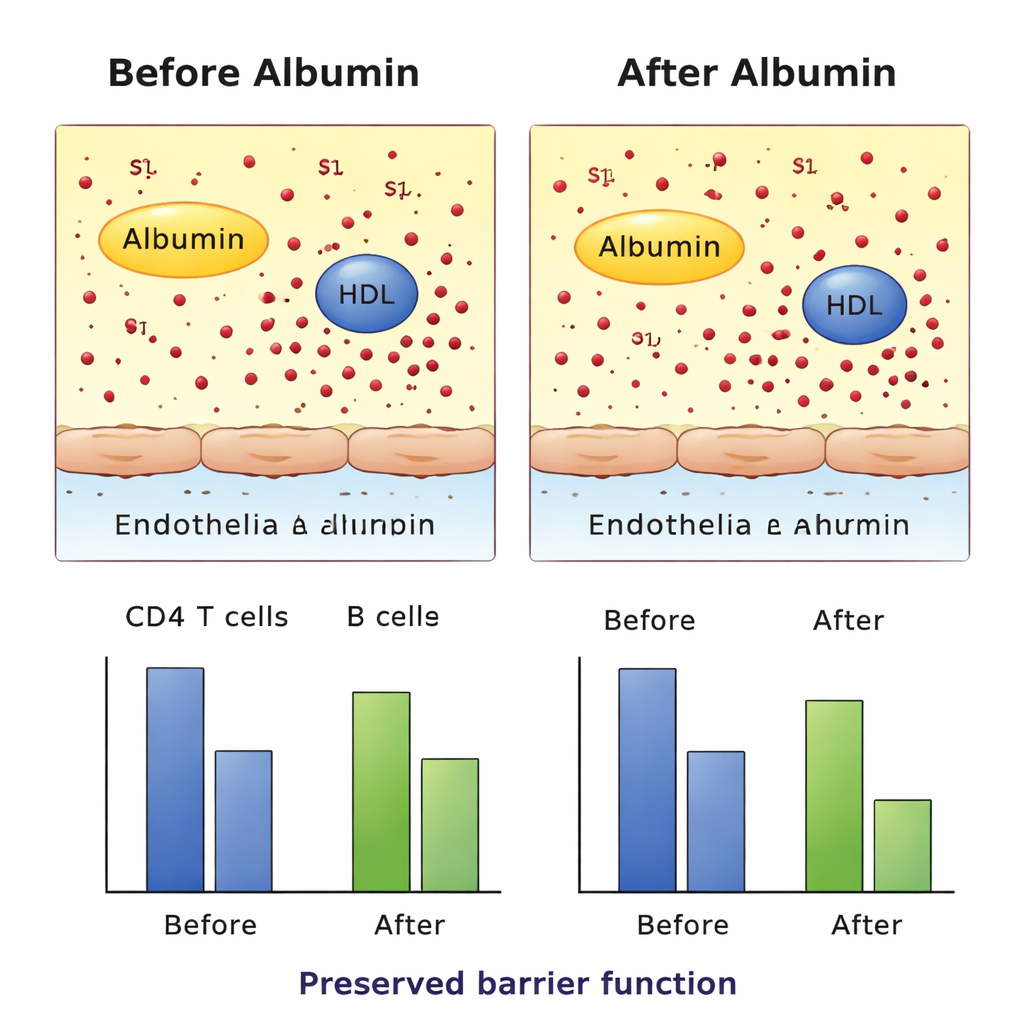
Pour déterminer si ce basculement des transporteurs avait des effets indésirables, les chercheurs ont testé les échantillons des patients dans plusieurs systèmes expérimentaux contrôlés. Ils ont exposé des cellules endothéliales en culture au plasma des différents groupes et ont surveillé la résistance électrique de la couche cellulaire, un indicateur de la cohésion de la barrière. Ils ont aussi utilisé un test de migration dans lequel des cellules immunitaires fluorescentes traversaient une membrane en direction du plasma des patients, simulant le « rappel » dirigé par le S1P. Dans ces expériences ex vivo, le plasma des patients traités par albumine n'a pas affaibli la barrière endothéliale et n'a pas significativement réduit la migration des cellules immunitaires induite par le S1P par rapport aux témoins. Des tests supplémentaires au niveau des récepteurs ont montré que le S1P porté par les HDL ou par l'albumine pouvait encore activer ses récepteurs cibles, du moins dans les conditions étudiées.
Ce que cela implique pour les décisions thérapeutiques futures
Pour les non‑spécialistes, le message principal est que les perfusions d'albumine chez les patients très malades ne semblent pas restaurer la quantité globale de ce messager important, le S1P, mais elles le déplacent du HDL vers l'albumine dans la circulation. Ce déplacement s'accompagne de changements subtils des cellules immunitaires circulantes sans altération évidente de la stabilité vasculaire dans les tests en laboratoire. Ces résultats soutiennent l'idée que l'albumine a des rôles immunomodulateurs au‑delà de sa simple fonction osmotique et que ses bénéfices — s'ils existent — pourraient être limités à des sous‑groupes de patients particuliers, comme ceux présentant un HDL très bas ou une inflammation marquée. Des études plus larges et ciblées seront nécessaires pour déterminer si des patients soigneusement sélectionnés peuvent tirer un avantage clinique significatif de ce rôle plus nuancé de la thérapie par l'albumine.
Citation: Winkler, M.S., Enzmann, F., Schilder, M. et al. The potential effect of albumin replacement on immune modulation and sphingosine 1-phosphate dynamics. Sci Rep 16, 5412 (2026). https://doi.org/10.1038/s41598-026-38157-8
Mots-clés: thérapie par l'albumine, maladie critique, sphingosine 1‑phosphate, immunologie de la septicémie, barrière vasculaire