Clear Sky Science · fr
INHBA : un gène pan-mort cellulaire lié aux mitochondries associé au pronostic et à l’immunité des CSCO
Pourquoi cela importe pour le cancer de la bouche
Le carcinome épidermoïde de la cavité buccale, une forme fréquente de cancer de la bouche, peut priver les personnes de capacités élémentaires comme parler, manger voire sourire sans gêne. En dépit de la chirurgie, de la radiothérapie et de la chimiothérapie, de nombreux patients connaissent des récidives et une survie à long terme médiocre. Cette étude propose un regard neuf sur le cancer buccal en se concentrant sur la façon dont un seul gène, nommé INHBA, influence la mort cellulaire, le voisinage tumoral constitué de cellules de soutien et le succès ou l’échec des traitements modernes tels que l’immunothérapie.
Un examen approfondi d’un cancer buccal mortel
La plupart des cancers de la tête et du cou prennent naissance dans la muqueuse buccale, et plus de 90 % d’entre eux sont des carcinomes épidermoïdes de la cavité buccale (CSCO). Dans le monde, les cas et les décès dus aux CSCO augmentent et devraient croître d’environ 40 % d’ici 2040. Les soins standards reposent sur la chirurgie associée à la radiothérapie et à la chimiothérapie, mais de nombreuses tumeurs résistent et récidivent. Les immunothérapies récentes, qui visent à réveiller les défenses de l’organisme, ne profitent qu’à une fraction des patients. Pour dépasser l’approche par essais‑erreurs, les chercheurs doivent comprendre quels gènes pilotent les CSCO et comment ils interagissent avec le système immunitaire.
Mort cellulaire, centrales énergétiques et une nouvelle catégorie de gènes
Nos cellules sont programmées pour mourir selon plusieurs modalités étroitement régulées, incluant des processus appelés apoptose, autophagie, ferroptose, entre autres. Dans le cancer, ces programmes de mort sont souvent reconfigurés de sorte que les cellules tumorales survivent alors qu’elles ne devraient pas. L’équipe à l’origine de cette étude s’est intéressée à un large groupe qu’elle appelle les gènes « pan‑mort cellulaire » — des gènes situés au carrefour de différentes voies de mort — et s’est focalisée plus précisément sur ceux associés aux mitochondries, ces petites centrales énergétiques cellulaires. En combinant de larges jeux de données publics sur le cancer avec un catalogue spécialisé de gènes mitochondriaux, ils ont défini un ensemble de « gènes pan‑mort cellulaire associés aux mitochondries » et recherché ceux qui étaient le plus fortement liés au comportement des CSCO et au pronostic des patients.
Identifier INHBA parmi de nombreux suspects
À l’aide de statistiques avancées et de neuf algorithmes d’apprentissage automatique différents, les chercheurs ont trié des milliers de gènes et identifié 19 gènes mitochondriaux pan‑mort cellulaire fortement corrélés au pronostic dans les CSCO. Parmi eux, INHBA s’est distingué. Son activité était systématiquement plus élevée dans les échantillons tumoraux que dans le tissu buccal normal et était associée à une survie plus mauvaise aussi bien dans les CSCO que dans l’ensemble plus large des cancers de la tête et du cou. Lorsque les tumeurs furent séparées en groupes à INHBA élevé et faible, celles à niveaux supérieurs présentaient des signaux biologiques plus agressifs, incluant des voies liées à l’invasion tissulaire, à l’angiogenèse et au stress mitochondrial. Des tests en laboratoire sur des échantillons de patients ont confirmé que les niveaux d’ARN d’INHBA étaient bien élevés dans des tumeurs réelles.
Le rôle caché des cellules de soutien autour de la tumeur
Pour savoir où INHBA est le plus actif, l’équipe a eu recours au séquençage d’ARN unicellulaire et à la transcriptomique spatiale, des technologies qui cartographient l’activité génique au niveau cellulaire et à travers des coupes de tissu. Ils ont constaté qu’INHBA n’est pas principalement produit par les cellules cancéreuses elles‑mêmes, mais par les fibroblastes associés au cancer — des cellules de soutien qui remodèlent le tissu et façonnent l’environnement immunitaire. Un sous‑type particulier, appelé CAF myofibroblastique, montrait des niveaux d’INHBA particulièrement élevés. Des cartes détaillées des communications ont suggéré que ces fibroblastes riches en INHBA dialoguent intensément avec les cellules immunitaires et les cellules tumorales, contribuant à créer une niche cicatricielle immunosuppressive autour de la tumeur. Ce microenvironnement semble favoriser la croissance tumorale et pourrait atténuer l’efficacité de certaines immunothérapies.
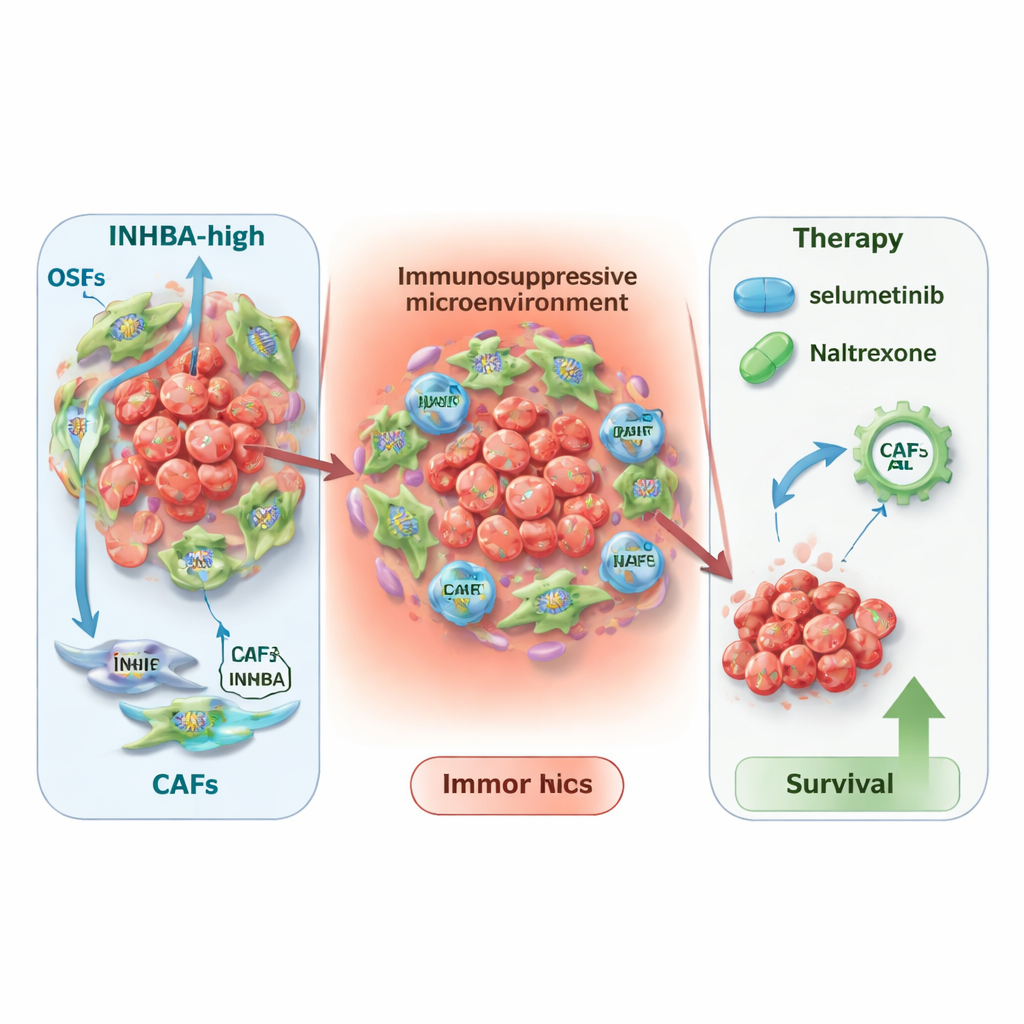
Nouvel éclairage thérapeutique et portée plus large
Sachant qu’INHBA signale un voisinage tumoral plus dangereux, les chercheurs ont examiné comment cela pourrait orienter la thérapie. Chez les patients recevant une immunothérapie, de faibles niveaux d’INHBA étaient associés à de meilleurs résultats avec des médicaments ciblant PD‑L1 ou CTLA4, tandis que des niveaux élevés d’INHBA semblaient prédire un bénéfice supérieur des approches CAR‑T. En explorant deux grandes bases de données de réponse aux médicaments, ils ont également signalé deux médicaments existants — le sélumétinib et la naltrexone — comme particulièrement prometteurs dans les tumeurs à INHBA élevé. La modélisation moléculaire a montré que ces deux médicaments pourraient se lier fortement à la protéine INHBA, suggérant un effet potentiel direct. Enfin, une analyse pancancéreuse a révélé qu’INHBA est augmenté et lié à une survie défavorable dans de nombreux autres types tumoraux, ce qui suggère que son importance dépasse largement le cancer de la bouche.
Ce que cela signifie pour les patients
En termes clairs, cette étude identifie INHBA comme un gène « chef d’orchestre » qui aide les tumeurs orales mortelles à croître, se propager et échapper au système immunitaire, principalement en agissant via des cellules de soutien spécialisées plutôt que par les seules cellules cancéreuses. Mesurer INHBA dans les tumeurs pourrait aider les médecins à repérer les patients à haut risque, prédire qui bénéficiera de différents types d’immunothérapie et choisir des médicaments ciblés susceptibles d’être plus efficaces dans ce contexte. Étant donné qu’INHBA joue un rôle nuisible similaire dans plusieurs autres cancers, des thérapies ciblant ce gène et ses partenaires fibroblastiques pourraient à terme profiter à un large éventail de patients, rapprochant les soins d’une prise en charge précise et personnalisée.
Citation: Zhang, X., Sun, M., Qiu, T. et al. INHBA: a mitochondrial-related pan-cell death gene associated with the prognosis and immunity of OSCC. Sci Rep 16, 7642 (2026). https://doi.org/10.1038/s41598-026-38131-4
Mots-clés: carcinome épidermoïde de la cavité buccale, INHBA, microenvironnement tumoral, fibroblastes associés au cancer, immunothérapie