Clear Sky Science · fr
L'inhibition de CDK2 favorise la différenciation neuronale dans le neuroblastome
Pourquoi cette étude sur le cancer pédiatrique est importante
Le neuroblastome est l’un des cancers solides les plus fréquents chez les jeunes enfants et reste mortel pour de nombreux patients à haut risque malgré des traitements intensifs. Cette étude explore une nouvelle façon d’aborder la maladie : au lieu de chercher seulement à tuer les cellules cancéreuses, elle se demande s’il est possible de les pousser à devenir des cellules nerveuses inoffensives. Les auteurs se concentrent sur une protéine appelée CDK2 et montrent que la bloquer pourrait à la fois ralentir la croissance tumorale et encourager la maturation des cellules cancéreuses, ouvrant la voie à des thérapies plus douces et ciblées.
Une protéine qui pose problème dans les tumeurs agressives
Les chercheurs ont commencé par exploiter plusieurs larges collections d’échantillons tumoraux d’enfants atteints de neuroblastome. Ils ont posé une question simple : quand le gène CDK2 est‑il le plus activé ? La réponse est frappante. Les tumeurs présentant les niveaux les plus élevés de CDK2 avaient tendance à être à un stade avancé, classées à haut risque et plus susceptibles de récidiver après le traitement. Les enfants dont les tumeurs exprimaient beaucoup de CDK2 avaient généralement un pronostic plus mauvais au fil du temps. Ces cancers portaient souvent des copies supplémentaires d’un autre gène oncogénique puissant, MYCN, et paraissaient au microscope plus primitifs et moins semblables à des cellules nerveuses normales. Ensemble, ces schémas suggèrent que CDK2 est étroitement lié aux formes les plus dangereuses de la maladie.
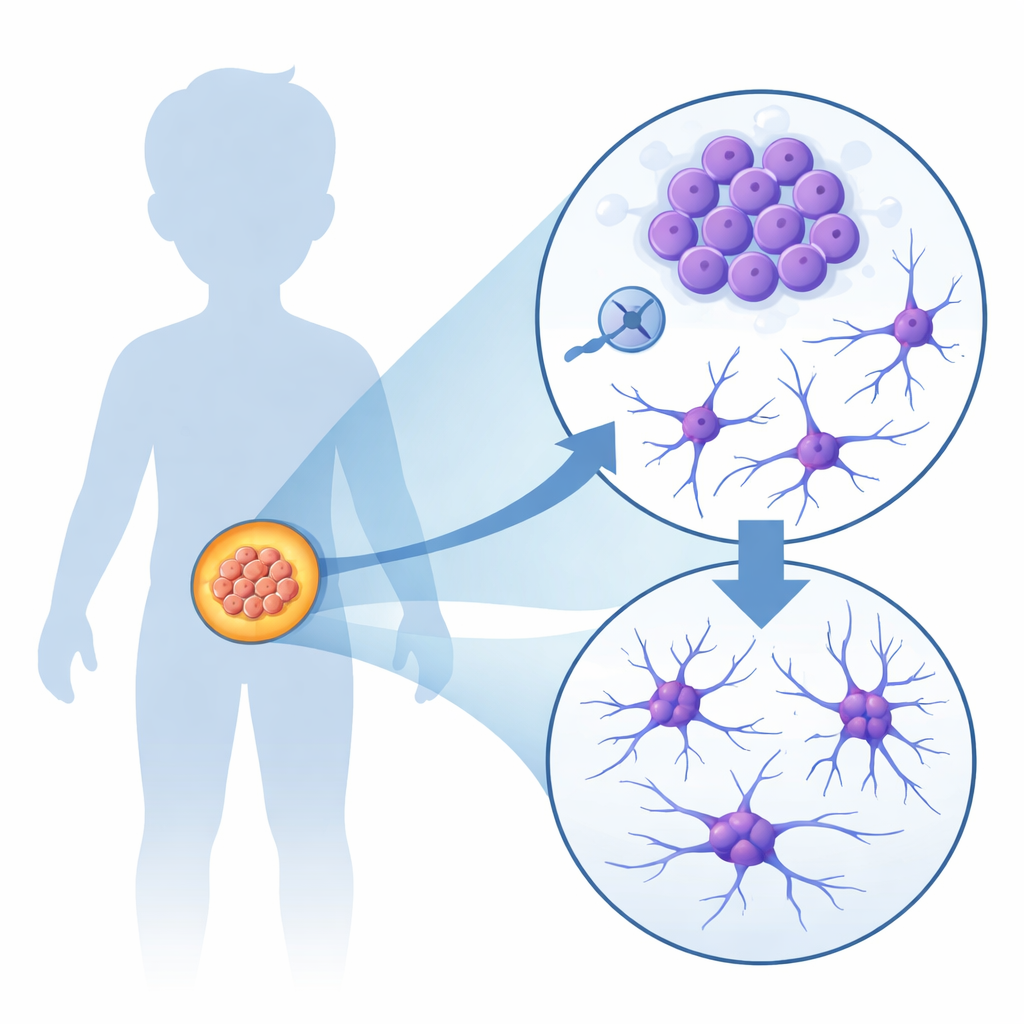
De cellules en division rapide à des prolongements de type nerveux
Pour savoir ce que fait réellement CDK2 à l’intérieur des cellules tumorales, l’équipe a utilisé des lignées cellulaires humaines de neuroblastome cultivées en laboratoire. Ils ont soit désactivé le gène CDK2, soit bloqué la protéine CDK2 avec des molécules de type médicament. Dans les deux cas, quelque chose de remarquable s’est produit : au lieu de se diviser sans fin comme le font généralement les cellules cancéreuses, de nombreuses cellules ont commencé à étendre de longs et fins prolongements rappelant les branches des cellules nerveuses en développement. Les gènes associés à la croissance et à la communication neuronales ont été activés, tandis que les gènes liés à la division cellulaire et à la réparation de l’ADN ont été réprimés. Ces changements étaient les plus marqués dans les cellules portant des copies supplémentaires de MYCN, le sous‑type même qui provoque les formes les plus agressives chez l’enfant.
CDK2 et MYCN : une boucle d’amplification
En approfondissant, les scientifiques ont découvert que CDK2 et MYCN sont reliés par une boucle de rétroaction. MYCN se lie directement à l’ADN près du gène CDK2 et en augmente l’activité, contribuant à maintenir des niveaux élevés de CDK2 dans les cellules tumorales. Lorsque MYCN était réduit, les niveaux de CDK2 diminuaient. À l’inverse, la perte de CDK2 atténuait le programme de signalisation plus large de la famille MYC qui stimule la croissance rapide. Cela signifie que, dans de nombreuses tumeurs à haut risque, MYCN et CDK2 coopèrent pour maintenir les cellules dans un état immature et à division rapide et pour bloquer leur tendance naturelle à se différencier en cellules nerveuses.
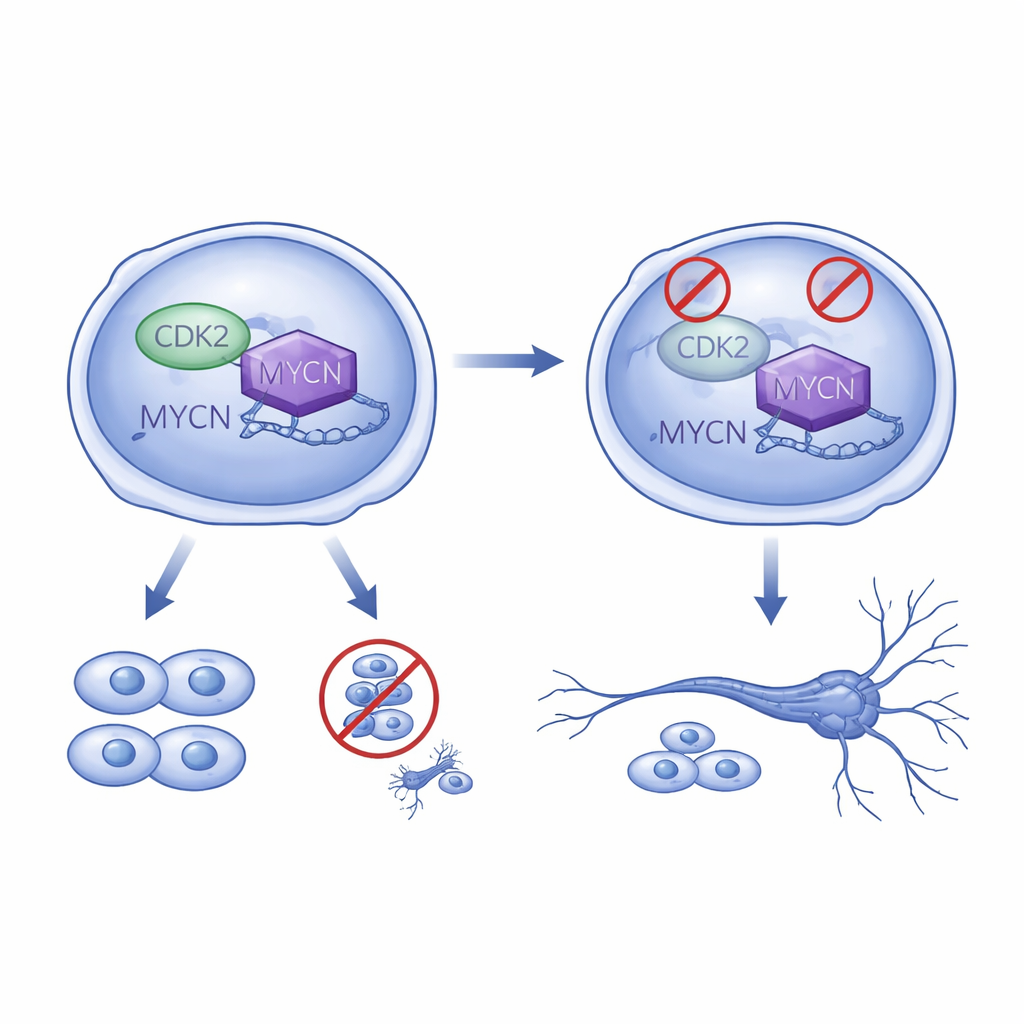
Renforcer les traitements existants en poussant les cellules à mûrir
Parce que CDK2 et MYCN coopèrent, les chercheurs ont testé des combinaisons d’inhibiteurs de CDK2 avec des composés expérimentaux ciblant MYC. Dans plusieurs modèles cellulaires de neuroblastome, ces paires de médicaments réduisaient la survie cellulaire plus que chaque traitement isolé et produisaient souvent davantage de prolongements de type nerveux, suggérant une différenciation renforcée. Ils ont aussi associé l’inhibition de CDK2 à l’acide tout‑trans‑rétinoïque (ATRA), un médicament dérivé de la vitamine A déjà utilisé pour aider les cellules de neuroblastome à se différencier après chimiothérapie. En milieu de culture, la combinaison d’inhibiteurs de CDK2 et d’ATRA donnait des « scores de différenciation » supérieurs — des prolongements plus longs et des marqueurs neuronaux plus forts — que les traitements seuls, indiquant une manière possible d’améliorer une thérapie standard existante.
Ce que cela pourrait signifier pour les enfants atteints de neuroblastome
Concrètement, cette étude montre que des niveaux élevés de CDK2 caractérisent des tumeurs de neuroblastome particulièrement agressives et immatures, et que réduire l’activité de CDK2 peut pousser les cellules cancéreuses à se comporter davantage comme des cellules nerveuses normales et parfois à mourir. Comme CDK2 est intégré au même réseau de stimulation de la croissance que MYCN, cibler les deux en même temps — ou associer des inhibiteurs de CDK2 à des rétinoïdes comme l’ATRA — pourrait un jour offrir une stratégie thérapeutique fondée sur la différenciation plus efficace. Bien que ces résultats en soient encore au stade des cultures cellulaires et nécessitent des tests rigoureux chez l’animal et en essais cliniques, ils dessinent une voie prometteuse vers des traitements qui n’attaquent pas seulement les cellules tumorales, mais les incitent à se développer et à se calmer.
Citation: Alzrigat, M., Mahmoud, L., Topçu, A.N. et al. CDK2 inhibition promotes neuronal differentiation in neuroblastoma. Sci Rep 16, 5255 (2026). https://doi.org/10.1038/s41598-026-38123-4
Mots-clés: neuroblastome, inhibition de CDK2, différenciation neuronale, MYCN, thérapie par rétinoïdes