Clear Sky Science · fr
Obinutuzumab induit une déstabilisation lysosomale via une inhibition dépendante de la sphingomyéline de TRPML2
Pourquoi cette histoire d’anticorps importe
Pour de nombreuses personnes atteintes de lymphomes à cellules B, les anticorps thérapeutiques modernes ont transformé un diagnostic autrefois uniformément mortel en une maladie traitable. Pourtant, tous les anticorps ne se valent pas : certains détruisent les cellules cancéreuses de façon plus puissante et plus fiable que d’autres. Cet article explore pourquoi un tel médicament, l’obinutuzumab, est meilleur pour tuer directement les cellules lymphomateuses que son prédécesseur le rituximab, en zoomant sur un coupable inattendu niché au cœur de la cellule : ses centres de recyclage, appelés lysosomes, et l’équilibre subtil entre lipides et canaux ioniques dans leurs membranes.
De la cible de surface à l’autodestruction interne
Tant le rituximab que l’obinutuzumab reconnaissent la même cible sur les cellules B, une protéine appelée CD20. Mais les auteurs montrent que l’obinutuzumab est internalisé beaucoup plus rapidement et plus efficacement. Une fois lié au CD20 à la surface de la cellule cancéreuse, les complexes anticorps–récepteur sont entraînés vers l’intérieur par endocytose et dirigés vers des compartiments acides, y compris les lysosomes. Là, l’obinutuzumab déclenche une perméabilisation de la membrane lysosomale : la membrane normalement robuste devient poreuse, permettant à des enzymes digestives comme les cathépsines de se répandre dans la cellule et de déclencher des voies de mort cellulaire. Des modifications de l’équilibre en sels et en eau de ces compartiments, qui font gonfler les lysosomes, ont été identifiées comme un facteur amplifiant fortement cet effet létal.
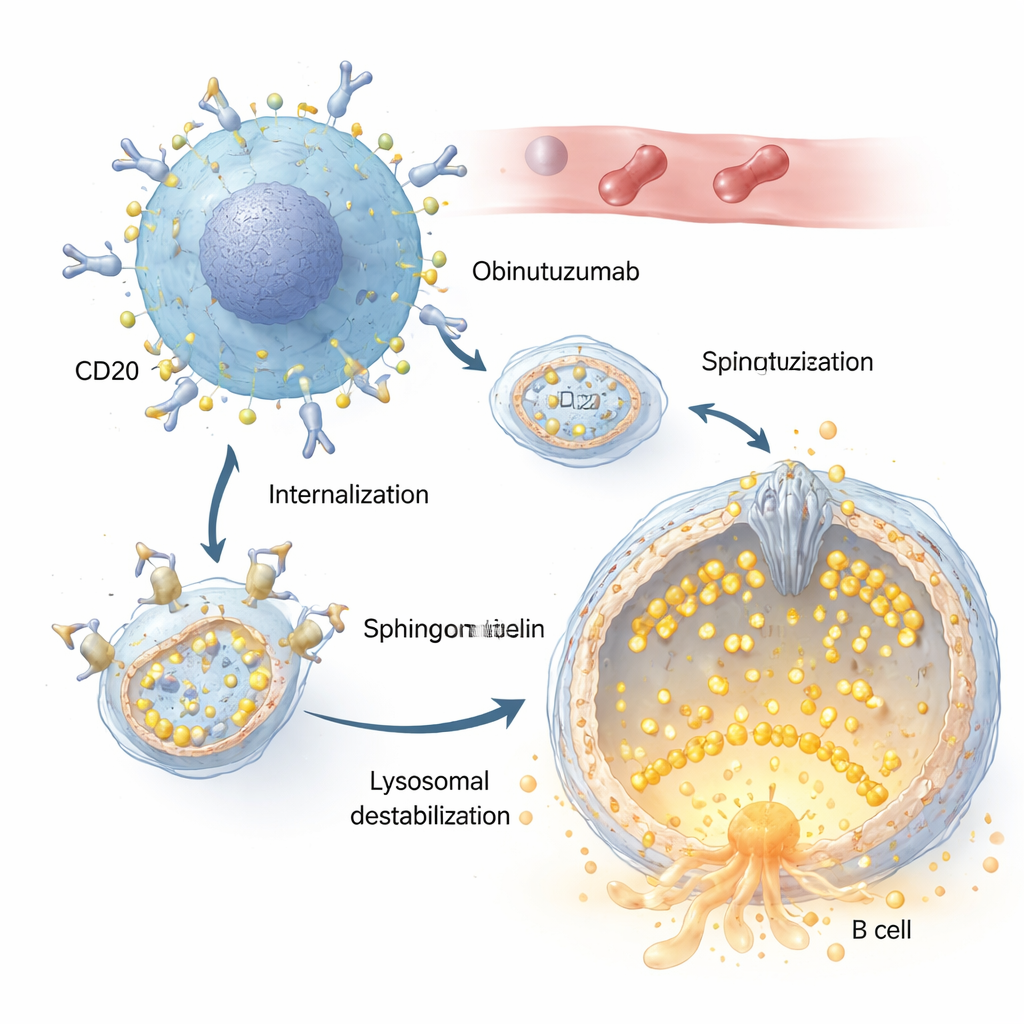
Le rôle d’un minuscule canal gardien
Au centre de cette histoire se trouve TRPML2, un canal calcique intégré à la membrane lysosomale. En conditions normales, TRPML2 aide les lysosomes à faire face au stress mécanique et osmotique en libérant du calcium, ce qui soutient la réparation membranaire, le trafic et le contrôle du volume. À l’aide de colorants calciques fluorescents et de versions de TRPML2 conçues pour détecter le calcium, les chercheurs montrent que l’obinutuzumab bloque rapidement ce canal : en quelques minutes après le traitement, un agent qui ouvre normalement les canaux TRPML ne provoque plus d’explosion de calcium. Des approches génétiques réduisant les niveaux de TRPML2, ou des inhibiteurs de faible masse moléculaire bloquant l’activité des TRPML, rendent toutes deux les cellules lymphomateuses plus sensibles à l’obinutuzumab, entraînant davantage de fuite lysosomale et des taux plus élevés de mort cellulaire directe.
Comment les lipides membranaires font basculer l’équilibre
L’étude s’interroge ensuite sur le lien entre l’internalisation de l’anticorps et l’inhibition du canal. L’attention se porte sur la sphingomyéline, un lipide abondant dans les membranes cellulaires connu pour interférer avec les canaux TRPML. À l’aide d’une sonde fluorescente liant la sphingomyéline, les auteurs constatent que les vésicules contenant l’obinutuzumab sont riches en sphingomyéline une fois qu’elles atteignent les compartiments acides, bien plus que les vésicules contenant le rituximab. Lorsque les cellules sont traitées par une sphingomyélinase, une enzyme qui réduit la sphingomyéline, l’activité de libération calcique de TRPML2 est rétablie même en présence d’obinutuzumab. Dans ces conditions, les lysosomes sont moins susceptibles de fuir et moins de cellules meurent, ce qui suggère fortement que l’accumulation de sphingomyéline désactive TRPML2 et prépare les lysosomes à la rupture.
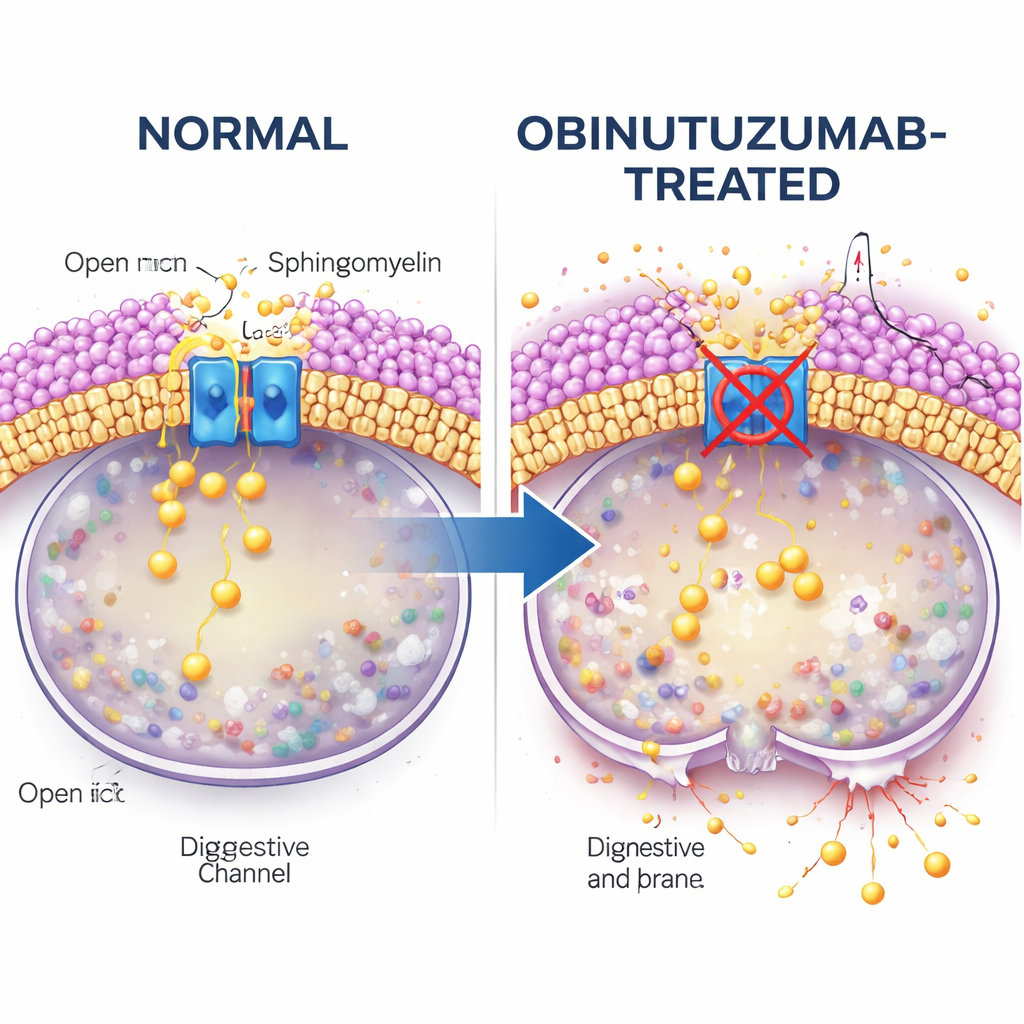
Itinéraires de trafic et points de contrôle du cholestérol
La voie empruntée par l’obinutuzumab pour pénétrer dans la cellule importe également. La microscopie électronique et un marquage d’anticorps sensible au pH révèlent que l’obinutuzumab quitte la surface cellulaire et entre dans des vésicules intracellulaires plus rapidement que le rituximab. Lorsque les chercheurs perturbent des voies d’absorption spécifiques, ils observent que bloquer une forme d’endocytose dépendante du cholestérol (avec un composé appelé filipine) empêche l’obinutuzumab d’éteindre TRPML2 et réduit partiellement les dommages lysosomaux et la mort cellulaire. D’autres inhibiteurs d’endocytose n’ont pas cet effet protecteur. Cela indique une voie spécialisée, riche en cholestérol et en sphingomyéline, qui délivre l’obinutuzumab aux lysosomes d’une manière qui instaure l’inhibition de TRPML2 et la déstabilisation membraneaire qui s’ensuit.
Ce que cela signifie pour les traitements anticancéreux futurs
En termes simples, ce travail montre que l’obinutuzumab tue si efficacement les lymphomes B parce qu’il conduit leurs lysosomes dans un état de fragilité. En dirigeant les complexes anticorps–CD20 vers des compartiments riches en sphingomyéline, le médicament éteint indirectement un canal calcique protecteur, TRPML2. Une fois ce dispositif de sauvegarde perdu, les lysosomes sont plus susceptibles d’éclater sous stress, déversant des enzymes corrosives qui démantèlent la cellule cancéreuse de l’intérieur. Comprendre cet axe lipide–canal ionique dépasse l’explication de la supériorité de l’obinutuzumab sur le rituximab : cela suggère aussi de nouvelles stratégies pour renforcer les thérapies par anticorps — par exemple en les associant à des médicaments qui modifient les sphingolipides ou stimulent l’activité de TRPML2 afin d’ajuster finement le moment et la façon dont les lysosomes tumoraux s’autodétruisent.
Citation: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Mots-clés: obinutuzumab, lymphome B, lysosome, sphingomyéline, TRPML2