Clear Sky Science · fr
Propriétés fonctionnelles des vésicules extracellulaires dérivées des myotubes squelettiques basées sur les profils de microARN : une analyse comparative avec les vésicules extracellulaires dérivées de cellules souches mésenchymateuses
Messages musculaires dans de minuscules paquets
Nos muscles font bien plus que nous faire bouger : ils envoient en permanence des « messages » moléculaires dans tout le corps. Cette étude examine comment de minuscules particules libérées par les cellules musculaires se comparent à des particules semblables issues de cellules souches largement utilisées en thérapie. En décodant les signaux génétiques transportés par ces particules, les auteurs posent une question concrète : pour quels types de maladies les particules d’origine musculaire pourraient-elles être supérieures à celles issues de cellules souches ?
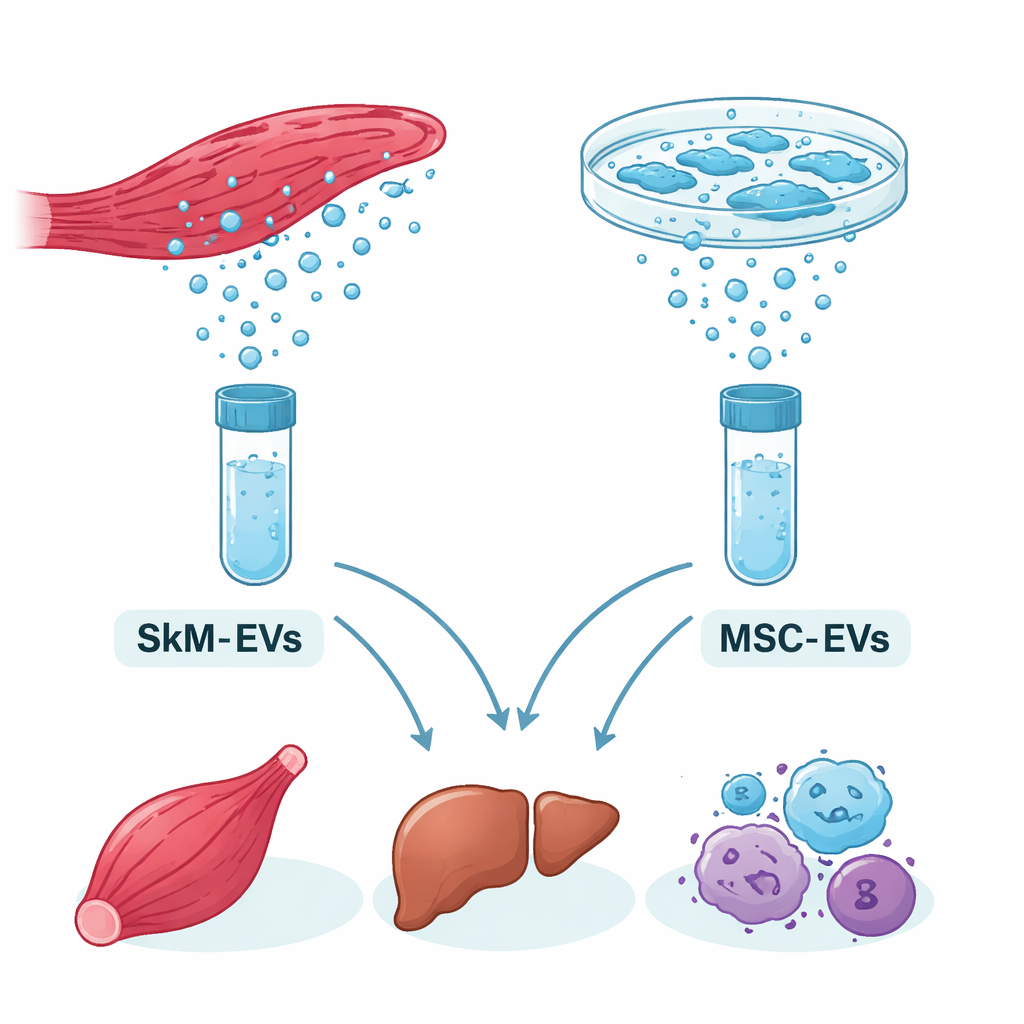
Petits coursiers voyageant dans le corps
Toutes les cellules libèrent des bulles microscopiques appelées vésicules extracellulaires, ou VE. Ce sont des colis nano‑taille enrobés de lipides et chargés de cargaisons moléculaires. Un type clé de cargaison est constitué par les microARN : de courts fragments d’ARN qui contribuent à augmenter ou diminuer l’expression des gènes et à façonner le comportement cellulaire. Le muscle squelettique, le tissu qui permet le mouvement, s’avère être le plus grand organe sécrétoire de l’organisme et peut libérer de fortes quantités de VE, notamment lorsqu’il est stimulé par des approches non invasives comme l’échographie. Les cellules souches mésenchymateuses, en revanche, sont déjà largement utilisées dans les essais cliniques, et leurs VE sont testées pour la réparation tissulaire et la modulation de l’inflammation.
Lire le code génétique de la cargaison
Plutôt que de tester directement les VE chez l’animal ou chez l’humain, les chercheurs ont réanalysé des jeux de données de séquençage existants qui recensent quels microARN sont présents dans les VE issues de myotubes squelettiques de souris (fibres musculaires cultivées en laboratoire) et dans celles issues de cellules souches mésenchymateuses dérivées de la moelle osseuse. Les VE musculaires présentaient quelques microARN dominants, tels que miR-206-3p et miR-378a-3p, représentant plus de 60 % de leur cargaison, tandis que les VE des cellules souches transportaient un mélange plus homogène, incluant la famille let-7 à action large. Comme chaque microARN peut influencer de nombreux gènes cibles, et que plusieurs microARN peuvent converger sur une même voie, l’équipe a développé des méthodes computationnelles pour comprendre comment des profils entiers — et non des molécules isolées — pourraient remodeler des programmes cellulaires.
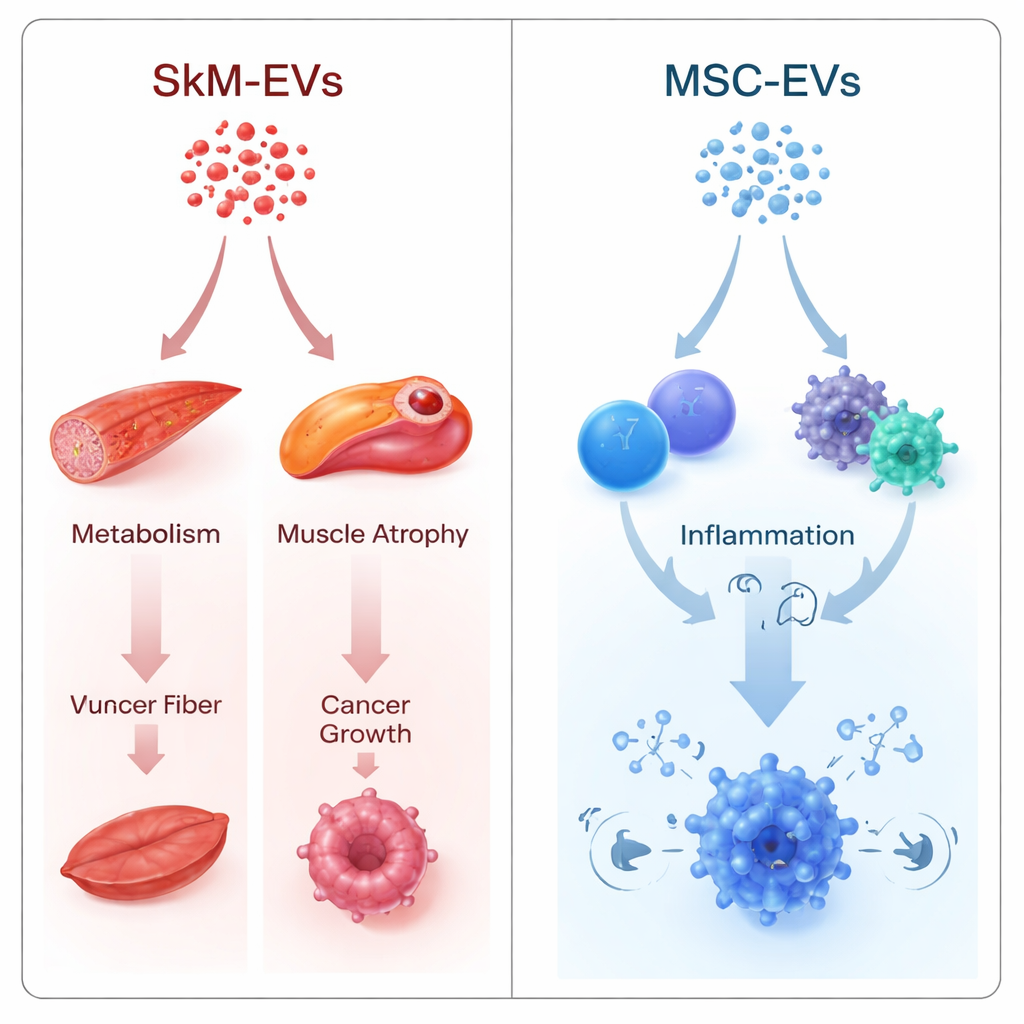
Voies liées au muscle, au métabolisme et au cancer
Les auteurs ont utilisé deux stratégies complémentaires. L’une a comparé tête‑à‑tête les VE musculaires et celles des cellules souches, en identifiant où leurs microARN différaient. L’autre a traité chaque type de VE séparément, en convertissant son profil de microARN en un « score d’impact » au niveau des gènes estimant la force avec laquelle la cargaison pourrait réprimer certaines voies. Malgré des démarches mathématiques différentes, les deux approches ont convergé vers les mêmes conclusions. Les VE d’origine musculaire présentaient une tendance prédite à supprimer des voies liées à l’atrophie musculaire (signalisation FoxO et TGF‑β), au contrôle de la glycémie et à l’équilibre énergétique (FoxO, mTOR, AMPK), ainsi qu’à des voies favorisant la croissance tumorale (signalisation ErbB et un ensemble désigné « microARN dans le cancer »). Nombre des cibles les plus influentes étaient des régulateurs centraux de la néoglucogenèse hépatique, des moteurs clés de l’atrophie musculaire et des gènes promoteurs du cancer.
Vésicules de cellules souches et système immunitaire
Les VE de cellules souches racontent une histoire différente. Leur cargaison en microARN était prédite pour agir plus fortement sur des voies liées à l’immunité : la signalisation NF‑κB, les interactions cytokine–récepteur, la signalisation des récepteurs B et T, et la différenciation des cellules Th17. Ces voies sont centrales pour la détection des infections, l’activation et l’arrêt de l’inflammation, et la définition de l’identité des cellules immunitaires. Ce biais concorde avec des preuves expérimentales croissantes montrant que les VE de cellules souches peuvent moduler largement les réponses immunitaires et sont testées dans des contextes où apaiser l’inflammation est crucial, comme les maladies auto‑immunes et inflammatoires.
Des prédictions informatiques aux traitements futurs
Globalement, le travail suggère que les VE d’origine musculaire pourraient être naturellement adaptées aux affections impliquant la perte musculaire, le dérèglement métabolique ou la prolifération cellulaire non contrôlée, tandis que les VE de cellules souches pourraient mieux convenir aux maladies résultant d’un dérèglement immunitaire. Les résultats reposent entièrement sur des analyses computationnelles de données existantes et ne démontrent pas encore un bénéfice chez les patients ; ils ne prennent pas non plus en compte d’autres cargaisons des VE comme les protéines ou les lipides. Néanmoins, en transformant des profils complexes de microARN en « empreintes » au niveau des voies, cette étude propose une feuille de route pour associer les sources de VE aux types de maladies et aide à prioriser les combinaisons les plus prometteuses à tester en laboratoire puis, éventuellement, en clinique.
Citation: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
Mots-clés: vésicules extracellulaires, muscle squelettique, microARN, cellules souches mésenchymateuses, voies de signalisation cellulaire