Clear Sky Science · fr
Conception de cryogels fonctionnalisés par polyéthylèneglycolamine–métal pour une liaison, une activité et une durabilité à long terme supérieures de la catalase
Pourquoi il est important de maintenir les enzymes en place
Le peroxyde d'hydrogène est un sous-produit chimique courant, présent partout, de l'industrie agroalimentaire aux traitements médicaux, et les cellules vivantes s'appuient sur l'enzyme catalase pour le décomposer en eau et en oxygène inoffensifs. En industrie, toutefois, la catalase est généralement utilisée sous forme libre et dissoute : elle perd rapidement en activité, n'est pas facilement récupérable et doit être remplacée fréquemment. Cette étude explore une méthode pour « garer » la catalase à l'intérieur d'un matériau poreux type éponge afin qu'elle reste active plus longtemps, puisse être réutilisée de nombreuses fois et fonctionne de manière plus efficace — autant d'atouts susceptibles de réduire les coûts et de rendre les procédés enzymatiques plus propres et plus durables.

Construire une éponge intelligente
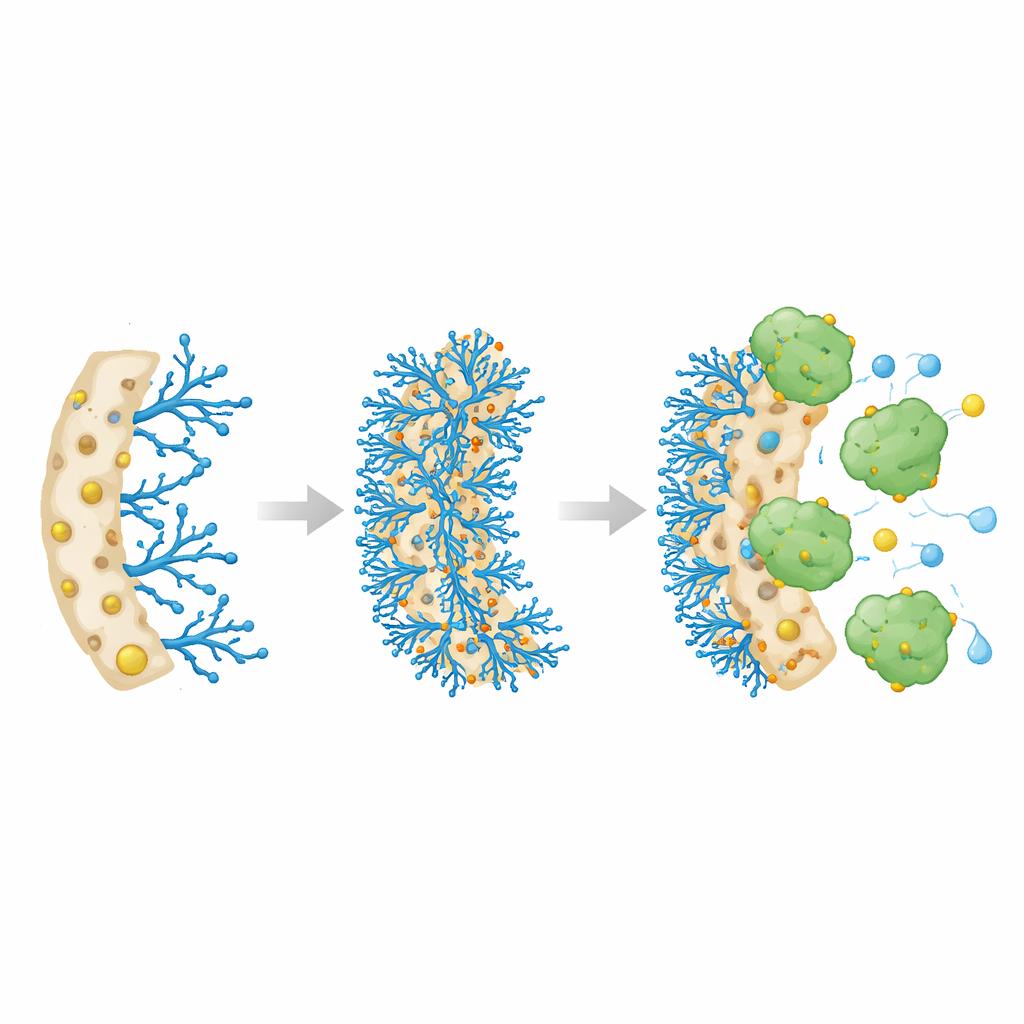
Les chercheurs ont conçu une éponge polymère particulière, appelée cryogel, formée par congélation et décongélation d'un mélange liquide de sorte que les cristaux de glace creusent de larges pores interconnectés. Ces pores laissent circuler les liquides librement, comme l'eau à travers un loofah, tandis que la structure solide reste robuste et élastique. L'équipe a utilisé comme matrice de base le Poly(HEMA-co-GMA), puis y a greffé chimiquement une molécule branchée riche en groupes azotés, la polyéthylèneglycolamine (PEI). Enfin, des ions métalliques — cuivre, nickel ou cobalt — ont été fixés sur ces sites azotés. L'idée était que ces ions métalliques servent de points d'ancrage attirant fortement la catalase et la maintenant en place sans obstruer l'écoulement du liquide à travers l'éponge.
Accorder le matériau pour de meilleures performances
Pour comprendre comment chaque étape de la conception modifiait le matériau, l'équipe a utilisé plusieurs techniques de laboratoire pour sonder sa structure, sa chimie et sa stabilité. Ils ont montré que l'ajout de PEI puis de métaux ne détruisait pas le réseau poreux mais augmentait en fait la capacité de l'éponge à retenir l'eau, ce qui est favorable pour maintenir les enzymes dans des conditions propices à leur activité. Parmi les trois métaux, le cuivre a créé l'environnement le plus hydraté et le mieux organisé. Des images microscopiques ont révélé que le matériau initial ressemblait à des granules compactes, tandis que les versions traitées au PEI et aux métaux s'ouvraient en un réseau plus continu et plus net de larges pores. Les mesures de teneur en métal ont confirmé que le cuivre se liait de manière plus forte et en plus grande quantité que le nickel ou le cobalt, ce qui suggère qu'il offrirait les sites d'ancrage les plus efficaces pour la catalase.
Verrouiller la catalase en place
Lorsque la catalase a été introduite dans les différentes éponges porteuses de métaux, les trois ont capté l'enzyme rapidement, mais la version au cuivre s'est distinguée. Elle a adsorbé la plus grande quantité de catalase — environ 392 milligrammes par gramme d'éponge sèche — et a atteint un plateau en environ huit heures. Les chercheurs ont ensuite comparé l'activité de l'enzyme immobilisée à celle de la catalase libre en solution. Bien que la vitesse de réaction maximale par gramme d'enzyme ait quelque peu diminué, la catalase immobilisée a montré une attraction apparente beaucoup plus forte pour son substrat, le peroxyde d'hydrogène. Concrètement, cela signifie que l'enzyme fixée effectuait son travail plus efficacement à des concentrations de substrat plus faibles, probablement parce que l'éponge cuivrée poreuse et hydratée concentrait le substrat à proximité de l'enzyme et aidait à maintenir sa conformation active.
Une enzyme qui dure
Un des principaux avantages de l'immobilisation des enzymes est la promesse de réutilisabilité et d'une longue durée de vie en stock. Ici, la catalase fixée sur le cryogel à base de cuivre s'est révélée bien plus durable que sa contrepartie libre. Après 15 cycles d'utilisation répétés, l'enzyme immobilisée conservait encore environ un tiers de son activité initiale, alors que la catalase libre serait typiquement jetée après une seule utilisation. Lors d'essais de stockage à température réfrigérée sur 70 jours, la catalase immobilisée a conservé plus de 60 % de son activité, soit environ le double de celle de l'enzyme libre. L'éponge a également permis de détacher puis de recharger l'enzyme plusieurs fois à l'aide d'une solution saline simple, montrant que le matériau lui‑même peut être réutilisé sans perte majeure de capacité.
Ce que cela signifie pour une utilisation réelle
Pour un lecteur non spécialiste, l'idée principale est que les chercheurs ont construit une sorte d'« éponge enzymatique » réutilisable qui maintient la catalase fermement mais en douceur, l'aidant à mieux fonctionner à des niveaux de produits chimiques plus bas et à durer beaucoup plus longtemps en activité et en stockage. En associant un cryogel très poreux à la PEI et aux ions cuivre, ils ont créé une plateforme qui combine une forte charge d'enzyme, une efficacité améliorée et une grande stabilité à long terme. De tels matériaux pourraient être intégrés dans des systèmes industriels ou environnementaux pour décomposer le peroxyde d'hydrogène et des substances apparentées de façon plus fiable et avec moins de déchets, offrant une étape pratique vers des technologies enzymatiques plus écologiques.»}
Citation: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Mots-clés: immobilisation d'enzymes, catalase, cryogel, polymères fonctionnalisés au cuivre, biocatalyse