Clear Sky Science · fr
Étudier le rôle oncogénique d’EZH2 aberrant dans l’hépatoblastome
Pourquoi cette histoire de cancer compte pour les familles
L’hépatoblastome est un cancer du foie rare mais grave qui touche principalement les très jeunes enfants. Les traitements actuels reposent largement sur une chimiothérapie intensive et des interventions chirurgicales majeures, parfois même des greffes de foie, qui peuvent laisser des effets secondaires durables. Cette étude pose une question porteuse d’espoir : existe‑t‑il un « interrupteur » moléculaire principal qui favorise ce cancer et que l’on pourrait éteindre, rendant le traitement à la fois plus précis et plus efficace ?
Un interrupteur caché à l’intérieur des cellules tumorales du foie
Les chercheurs se sont concentrés sur une protéine nommée EZH2, qui fait partie de la machinerie contrôlant l’activation ou la répression des gènes sans changer l’ADN lui‑même. En utilisant une technique puissante qui lit l’activité de milliers de gènes dans des noyaux cellulaires individuels, ils ont examiné à la fois le tissu tumoral et le foie sain adjacent chez des enfants atteints d’hépatoblastome. Ils ont découvert un groupe particulier de cellules tumorales, dérivées de cellules hépatiques, qui se divisaient activement et présentaient des niveaux très élevés d’EZH2. Ces cellules tumorales dites « en cycle » étaient beaucoup plus fréquentes dans la forme embryonnaire la plus agressive de la maladie que dans le tissu hépatique de fond.
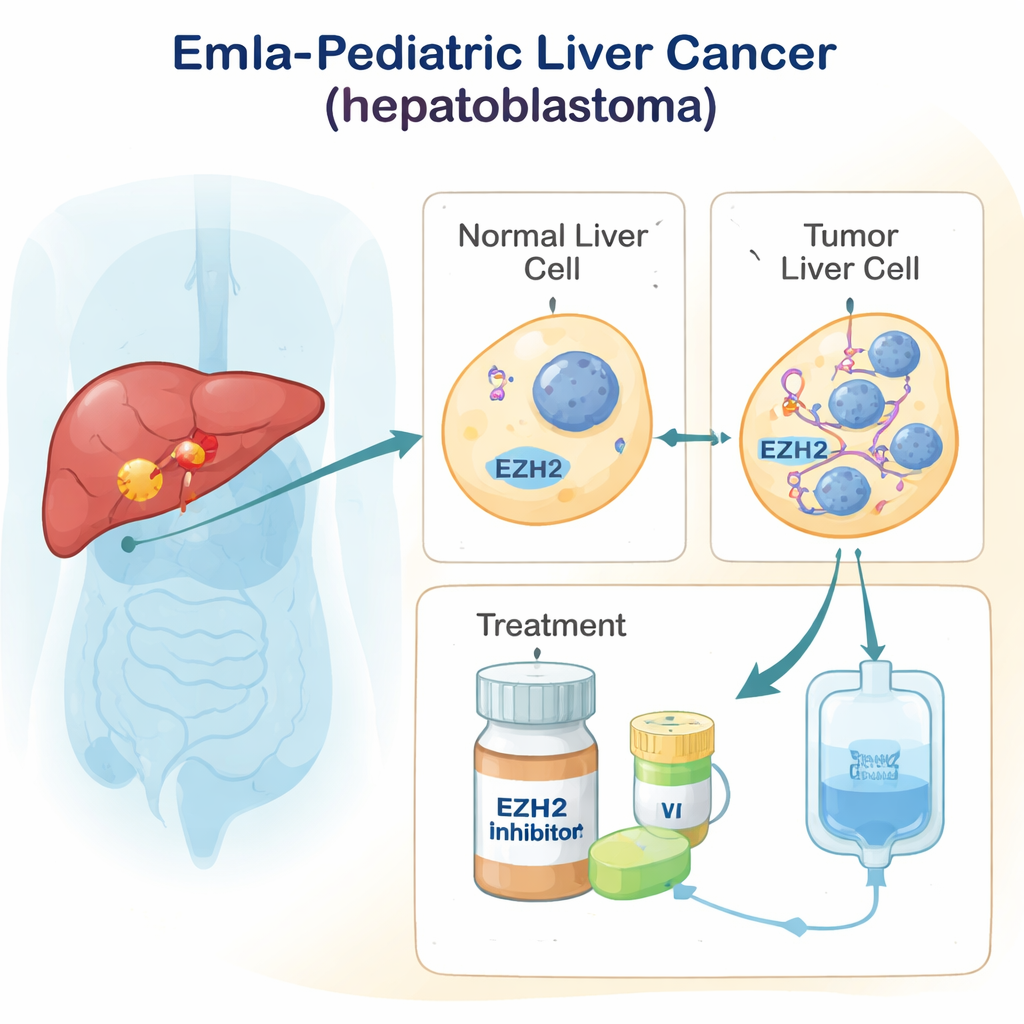
Ce qui rend ces cellules tumorales si agressives
En comparant les profils d’activité génique, l’équipe a montré que les cellules tumorales riches en EZH2 étaient chargées de signaux favorisant une division cellulaire rapide et des modifications de la structure des chromosomes. Ils ont aussi observé des signes d’altérations des voies normales de contrôle de la croissance, ce qui suggère qu’EZH2 ne se contente pas de réprimer des gènes protecteurs, mais reconfigure aussi d’autres voies liées au cancer de manière inattendue. Lorsqu’ils ont examiné des lames tumorales de patients au microscope, ils ont confirmé que la protéine EZH2 était particulièrement abondante dans les régions embryonnaires des tumeurs, et souvent présente dans des cellules prises en train de se diviser. Fait intéressant, d’autres composants du complexe EZH2 n’augmentaient pas toujours en parallèle, laissant entendre qu’EZH2 pourrait agir à la fois via ses rôles classiques de répression génique et via des mécanismes moins traditionnels, « hors script ».
Indices génétiques et points faibles vulnérables
L’équipe a également recherché dans l’ADN de 11 tumeurs pédiatriques des altérations des gènes impliqués dans cette machinerie. Chaque tumeur portait des variantes d’EZH2 et d’un autre membre du complexe, SUZ12, et la plupart présentaient aussi des mutations de CTNNB1, un moteur bien connu des tumeurs hépatiques. Bien que ces variantes d’EZH2 et de SUZ12 ne soient pas encore établies comme directement délétères, leur présence aux côtés d’une suractivité marquée d’EZH2 suggère qu’elles pourraient modifier subtilement le fonctionnement du complexe. Les analyses d’expression génique globales sur de nombreuses tumeurs ont montré que EZH2 et plusieurs gènes de division cellulaire étaient systématiquement plus élevés dans la tumeur que dans le foie normal, tandis que certains gènes qui contribuent normalement au contrôle de la croissance et à l’organisation tissulaire étaient réduits.
Réduire EZH2 pour renforcer la chimiothérapie
Pour déterminer si EZH2 est plus qu’un simple témoin, les chercheurs ont traité des lignées cellulaires de cancer du foie et des cellules tumorales dérivées de patients en laboratoire avec des médicaments inhibant EZH2, puis les ont exposées au cisplatine, une chimiothérapie standard. Les inhibiteurs d’EZH2 seuls ont eu des effets modestes. Mais combinés au cisplatine, de nombreuses cellules d’hépatoblastome sont devenues beaucoup plus sensibles et sont mortes à des doses de chimiothérapie plus faibles, en particulier dans les lignées qui ressemblent aux tumeurs pédiatriques les plus agressives. Dans un modèle murin portant des tissus humains d’hépatoblastome, le blocage d’EZH2 associé au cisplatine a réduit les tumeurs davantage que chaque traitement seul et a diminué une marque chimique (H3K27me3) liée à l’activité d’EZH2, montrant que le médicament atteignait sa cible dans le tissu vivant.
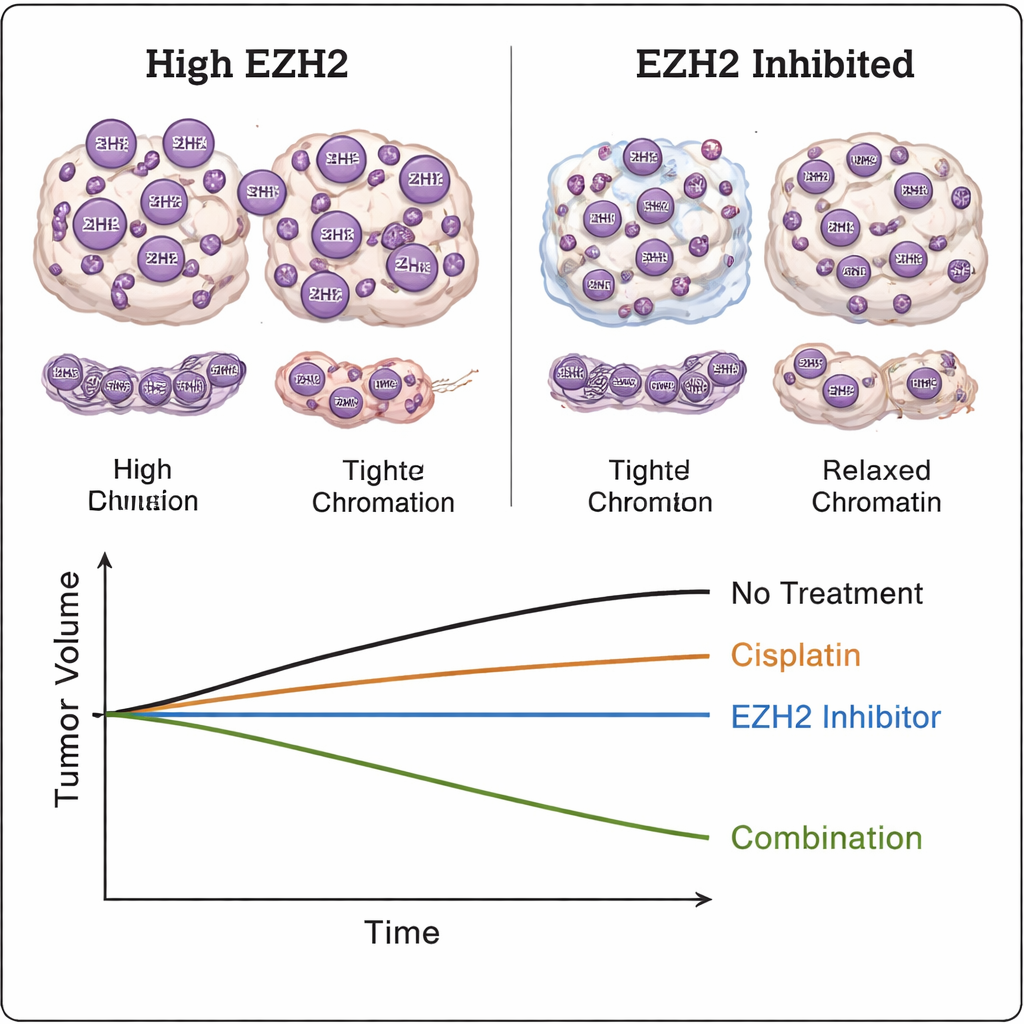
Ce que cela pourrait signifier pour les enfants atteints d’un cancer du foie
Pris ensemble, les résultats positionnent EZH2 comme un moteur central d’une population cellulaire à croissance rapide et résistante au traitement dans l’hépatoblastome, en particulier dans le sous‑type embryonnaire qui a tendance à être plus agressif. En atténuant EZH2, les médecins pourraient un jour affaiblir ces cellules difficiles à éliminer et améliorer l’efficacité des chimiothérapies existantes, potentiellement à des doses plus faibles. Bien que des recherches supplémentaires et des essais cliniques soient nécessaires avant que de telles stratégies n’atteignent la clinique, ce travail établit les bases scientifiques pour cibler EZH2 comme option thérapeutique nouvelle et plus ciblée pour les enfants confrontés à ce cancer du foie rare.
Citation: Glaser, K., DePasquale, E.A.K., Berklite, L. et al. Investigating the oncogenic role of aberrant EZH2 in hepatoblastoma. Sci Rep 16, 7563 (2026). https://doi.org/10.1038/s41598-026-38038-0
Mots-clés: hépatoblastome, EZH2, cancer du foie pédiatrique, thérapie épigénétique, cisplatine