Clear Sky Science · fr
Un outil pour prédire les effets du pH et de la température sur l’activité de la pepsine porcine et humaine lors de la digestion gastrique in vitro
Pourquoi les enzymes de l’estomac comptent pour l’alimentation quotidienne
À chaque fois que nous mangeons, des enzymes puissantes dans notre estomac commencent à fragmenter les protéines alimentaires en morceaux plus petits que notre organisme peut utiliser. L’une des plus importantes de ces enzymes est la pepsine. Les scientifiques alimentaires utilisent souvent une version porcine de la pepsine dans les tests de laboratoire pour remplacer la forme humaine, en supposant qu’elles se comportent de façon comparable. Cette étude pose une question simple mais cruciale : dans les conditions changeantes d’un estomac réel — où l’acidité (pH) et la température varient — la pepsine humaine et la pepsine porcine agissent-elles vraiment de la même façon, et comment peut-on prédire leur comportement ?
Comment les conditions changeantes de l’estomac influent sur la digestion
Dans l’estomac, le pH et la température sont loin d’être constants. Une boisson froide peut temporairement refroidir l’estomac de plus de 10 degrés, et un repas copieux ou alcalin peut élever le pH gastrique de plusieurs unités avant qu’il ne revienne lentement à un état plus acide. Comme la capacité de la pepsine à découper les protéines dépend fortement à la fois de l’acidité et de la chaleur, ces variations peuvent accélérer ou ralentir la digestion. Il est difficile de suivre cela directement chez les personnes, aussi les chercheurs s’appuient sur des modèles in vitro — des versions contrôlées en verrerie de la digestion. Ces modèles utilisent généralement la pepsine porcine comme substitut de la pepsine humaine, mais jusqu’à présent les scientifiques disposaient de peu de données claires sur la façon dont les deux enzymes réagissent lorsque pH et température varient ensemble, comme après un repas.
Mesurer les performances de la pepsine dans de nombreuses conditions
Les auteurs ont testé la pepsine humaine prélevée dans le liquide gastrique et la pepsine porcine commerciale sur 37 combinaisons de pH (de très acide à quasi neutre) et de température (du froid de réfrigérateur à des températures élevées). Ils ont ensuite utilisé ces mesures pour construire des modèles mathématiques capables de prédire l’activité de chaque enzyme pour n’importe quelle combinaison d’acidité et de chaleur rappelant l’estomac. Les deux enzymes fonctionnaient de manière optimale autour de pH 2 et de la température corporelle, mais la version humaine conservait une activité sur une plage plus large. À pH 3 et 4, la pepsine humaine gardait une activité substantielle, tandis que l’activité de la pepsine porcine chutait fortement. Fait intéressant, bien que la pepsine porcine fût plus puissante à son optimum, elle s’est révélée beaucoup plus sensible aux variations de pH, ce qui signifie que sa performance peut décliner plus rapidement lorsque les conditions deviennent moins favorables.
Ce que le nouvel outil de prédiction peut nous apprendre
En transformant ces mesures en équations conviviales intégrées à des feuilles de calcul, les chercheurs ont créé un moyen permettant d’estimer l’activité de la pepsine lors d’expériences de digestion en laboratoire. Ils ont réalisé plusieurs études de cas pour montrer les capacités de l’outil. Dans un modèle semi-dynamique de digestion du lait, les pepsines humaine et porcine simulées montraient des profils globaux similaires, mais la pepsine humaine conservait une activité utile plus longtemps lorsque le pH évoluait, conduisant à une plus grande « surface sous la courbe » d’activité cumulée. L’outil a également comparé les protocoles statiques traditionnels — où le pH est maintenu constant — aux protocoles semi-dynamiques qui s’acidifient progressivement, et simulé comment l’activité de la pepsine pourrait différer chez les adultes jeunes versus âgés, ces derniers sécrétant typiquement moins de pepsine. Ces exemples montrent comment un même repas et un même protocole peuvent produire des niveaux de dégradation des protéines différents selon le type d’enzyme et le modèle de digestion utilisés.
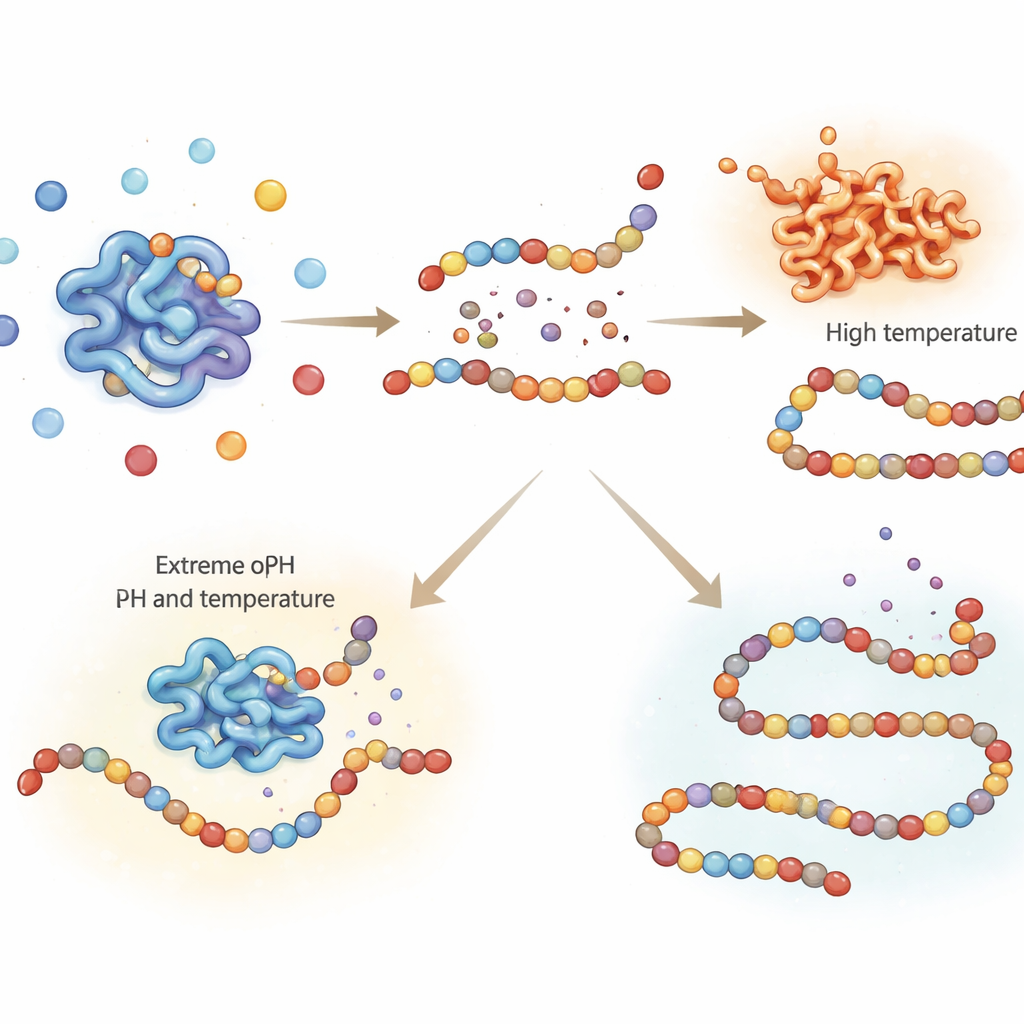
Trouver le point doux où la chaleur désactive la pepsine
Dans les expériences de digestion, il est essentiel d’arrêter la pepsine à des moments précis afin que les mesures ultérieures reflètent ce qui s’est passé dans « l’estomac » et non une continuation de la dégradation dans le tube d’essai. Un moyen courant d’inactiver les enzymes est la chaleur, mais un chauffage excessif peut endommager d’autres composants alimentaires et fausser les résultats. Cette étude a testé avec soin combien de temps et à quelle température la pepsine porcine doit être chauffée pour être définitivement inactivée. Un chauffage à 65 °C pendant jusqu’à 15 minutes n’a fait que réduire partiellement son activité, ce qui signifie que l’enzyme pouvait encore fonctionner ensuite. En revanche, un chauffage à 75 °C ou plus pendant seulement 5 minutes a complètement et irréversiblement inactivé la pepsine. La spectroscopie infrarouge de la structure de l’enzyme a montré que ces températures plus élevées provoquaient un dépliement durable et une agrégation de la protéine, corrélant avec la perte d’activité.
Ce que cela signifie pour la recherche alimentaire et la santé
Pour les non-spécialistes, le message clé est que la pepsine porcine couramment utilisée dans les modèles de laboratoire ne se comporte pas exactement comme la pepsine humaine lorsque l’on prend en compte les conditions réelles de l’estomac — acidité et température changeantes. Le nouvel outil de prédiction aide les chercheurs à estimer la puissance de découpe des protéines présente à chaque instant d’une expérience de digestion et à juger si leur protocole reflète vraiment ce qui pourrait se produire dans un estomac humain, y compris celui des adultes âgés. Parallèlement, l’étude identifie un traitement thermique à la fois doux et fiable — cinq minutes à 75 °C — pour arrêter la pepsine sans endommager inutilement d’autres composants alimentaires. Ensemble, ces avancées devraient rendre les études de digestion en laboratoire plus précises et plus comparables, améliorant notre compréhension de la façon dont différents aliments et procédés influent sur la digestion des protéines dans la vie quotidienne.
Citation: C. J., F., D., F., I., C. et al. A tool for predicting pH and temperature effects on porcine and human pepsin activity during in vitro gastric digestion. Sci Rep 16, 9176 (2026). https://doi.org/10.1038/s41598-026-38033-5
Mots-clés: pepsine, digestion gastrique, pH et température, modèles in vitro, digestion des protéines