Clear Sky Science · fr
Potentiel anticancéreux combinatoire synergique du tamoxifène avec la naringine et la diosmétine dans des cellules mammaires MCF-7 et leur administration liposomale
Pourquoi l’association d’un médicament courant et de composés d’agrumes importe
Le cancer du sein est souvent traité par le tamoxifène, un comprimé anti-hormonal qui a sauvé de nombreuses vies. Mais avec le temps, certaines tumeurs développent une résistance au médicament et les effets indésirables peuvent être difficiles à supporter. Cette étude explore une idée séduisante : peut-on améliorer l’efficacité du tamoxifène — et peut‑être réduire sa posologie — en l’associant à des substances naturelles présentes dans les agrumes, puis en les conditionnant ensemble dans de minuscules bulles lipidiques appelées liposomes pour qu’elles atteignent plus efficacement les cellules cancéreuses ?
Des alliés d’agrumes pour un médicament établi
Les chercheurs se sont intéressés à deux composés végétaux, la naringine et la diosmétine, des flavonoïdes courants des pamplemousses, oranges et autres agrumes. Dans des tests en laboratoire utilisant des cellules mammaires sensibles aux œstrogènes (MCF-7) et une autre lignée (T47D), ils ont d’abord mesuré la capacité de chaque composé pris isolément à ralentir ou tuer les cellules cancéreuses. Le tamoxifène était le plus puissant, mais la naringine et la diosmétine réduisaient aussi la survie cellulaire, en particulier dans les cellules MCF-7, suggérant que ces molécules naturelles possèdent elles‑mêmes une activité anticancéreuse. Cela a préparé le terrain pour tester si leur association avec le tamoxifène produirait un effet supérieur à la somme des effets individuels.
Plus forts ensemble : essais de combinaisons médicamenteuses
Pour comprendre l’interaction des médicaments, l’équipe a traité les cellules cancéreuses avec du tamoxifène plus naringine, du tamoxifène plus diosmétine, ou les trois ensemble, à différents ratios fixes. En utilisant une approche mathématique standard pour les paires médicamenteuses, ils ont montré que plusieurs combinaisons étaient synergétiques — c’est‑à‑dire que le mélange tuait plus de cellules que prévu d’après l’effet de chaque composé séparément. Un ratio comportant environ deux fois plus de flavonoïde que de tamoxifène (1:2) s’est avéré particulièrement efficace, notamment pour le tamoxifène associé à la naringine. Dans ces conditions, le même effet cytotoxique pouvait être atteint avec des quantités moindres de tamoxifène, un avantage clé si cela se traduit par moins d’effets indésirables chez les patients.
Déclencher l’auto‑destruction des cellules cancéreuses
Ensuite, les scientifiques ont cherché à savoir ce qui se passait à l’intérieur des cellules cancéreuses. Ils ont examiné le stress oxydatif — une accumulation d’espèces réactives de l’oxygène — et les signes d’apoptose, la mort cellulaire programmée. Les combinaisons, en particulier le trio tamoxifène ‑ naringine ‑ diosmétine, ont entraîné un stress oxydatif plus élevé et des signes d’apoptose plus marqués que le tamoxifène seul. Au microscope, davantage de cellules présentaient l’aspect rétréci et fortement coloré typique d’un stade avancé de mort cellulaire. Les analyses protéiques ont confirmé ces observations : les combinaisons diminuaient les niveaux de Bcl‑2 et Bcl‑xL, protéines qui aident normalement les cellules cancéreuses à résister à la mort, et augmentaient la caspase‑3 activée, un exécuteur clé de l’apoptose. En termes simples, les composés d’agrumes semblaient aider à pousser les cellules traitées au tamoxifène au‑delà du seuil vers l’autodestruction.
Conditionner les médicaments dans de minuscules transporteurs
Bien que les combinaisons paraissent prometteuses, la naringine et la diosmétine sont peu solubles dans l’eau et peuvent être mal absorbées. Pour remédier à cela, l’équipe a conçu des liposomes — des sphères à l’échelle nanométrique fabriquées à partir de lipides naturels — capables de porter ensemble le tamoxifène et les flavonoïdes. Ils ont optimisé la composition lipidique et le procédé de fabrication pour obtenir des particules d’environ 150–210 nanomètres de diamètre, relativement uniformes, et dotées d’une charge de surface favorisant leur stabilité en suspension. L’imagerie a confirmé que les liposomes étaient lisses et grossièrement sphériques. Les tests ont montré qu’une grande fraction de chaque médicament pouvait être encapsulée, et que leur libération dans un milieu environnant se faisait lentement sur 24 heures, selon une cinétique contrôlée par diffusion. Ce type de libération contrôlée est souhaitable car il peut maintenir des niveaux médicamenteux plus constants sur de plus longues périodes.
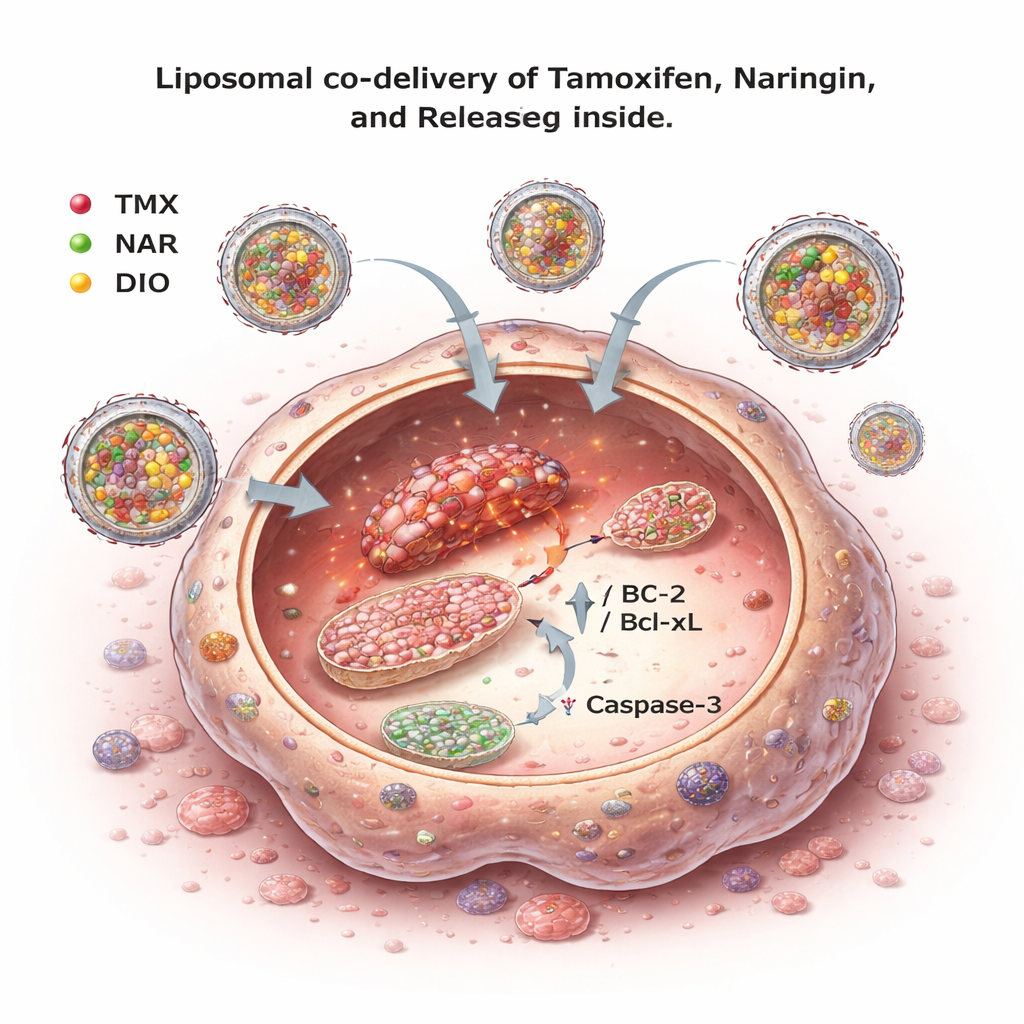
Frapper les tumeurs plus fort tout en épargnant les cellules saines
Lorsque ces formulations liposomales ont été testées sur des cellules cancéreuses du sein, les liposomes triple‑médicaments (tamoxifène, naringine et diosmétine ensemble) réduisaient la viabilité cellulaire plus efficacement que les liposomes ne contenant que le tamoxifène ou seulement deux des composés. Fait important, appliquées à une lignée cellulaire humaine non cancéreuse, ces mêmes formulations présentaient peu de toxicité dans la plage de doses testée, suggérant un certain degré de sélectivité pour les cellules cancéreuses. Dans l’ensemble, les résultats indiquent que combiner le tamoxifène avec des flavonoïdes dérivés d’agrumes et les administrer dans des liposomes peut renforcer l’élimination des cellules cancéreuses tout en permettant potentiellement des doses de tamoxifène plus faibles et plus sûres.
Ce que cela pourrait signifier pour les soins futurs du cancer du sein
Pour le non‑spécialiste, le message clé est que l’association d’un médicament standard contre le cancer du sein avec des composés naturels bien choisis, puis leur regrouper dans des transporteurs nano‑structurés, peut rendre le traitement plus efficace et possiblement plus doux. L’étude montre, en cultures cellulaires, que le tamoxifène fonctionne mieux en présence de naringine et de diosmétine : ils aident à faire basculer les cellules cancéreuses du mode survie vers la mort programmée, et ce de façon efficace lorsqu’ils sont co‑administrés dans des liposomes. Bien que ces travaux en soient encore au stade de laboratoire et doivent être confirmés chez l’animal puis en essais cliniques, ils dessinent une stratégie prometteuse : utiliser la thérapie combinée associée à la nanotechnologie pour contrer les tumeurs mammaires résistantes et améliorer les résultats à long terme.
Citation: Uniyal, P., Das Pramanik, S., Pandey, S. et al. Synergistic combinatorial anticancer potential of Tamoxifen with Naringin and Diosmetin in MCF-7 breast cancer cells and their liposomal delivery. Sci Rep 16, 7646 (2026). https://doi.org/10.1038/s41598-026-37954-5
Mots-clés: cancer du sein, tamoxifène, flavonoïdes, administration liposomale, thérapie combinée