Clear Sky Science · fr
Identification computationnelle et caractérisation mécanistique de ligands issus de produits naturels ciblant le tunnel de liaison prényle de PDE6D
Retourner contre lui l’interrupteur préféré du cancer
Beaucoup des cancers les plus mortels — du pancréas au côlon en passant par le poumon — dépendent d’un unique « interrupteur » moléculaire appelé RAS. Quand cet interrupteur reste bloqué en position ON, les cellules se divisent de façon incontrôlée. Les développeurs de médicaments peinent depuis des décennies à éteindre RAS directement. Cette étude explore une autre tactique : chercher des composés naturels capables de bloquer discrètement la protéine auxiliaire dont RAS a besoin pour atteindre son lieu d’action, diminuant potentiellement son signal sans attaquer RAS de front. 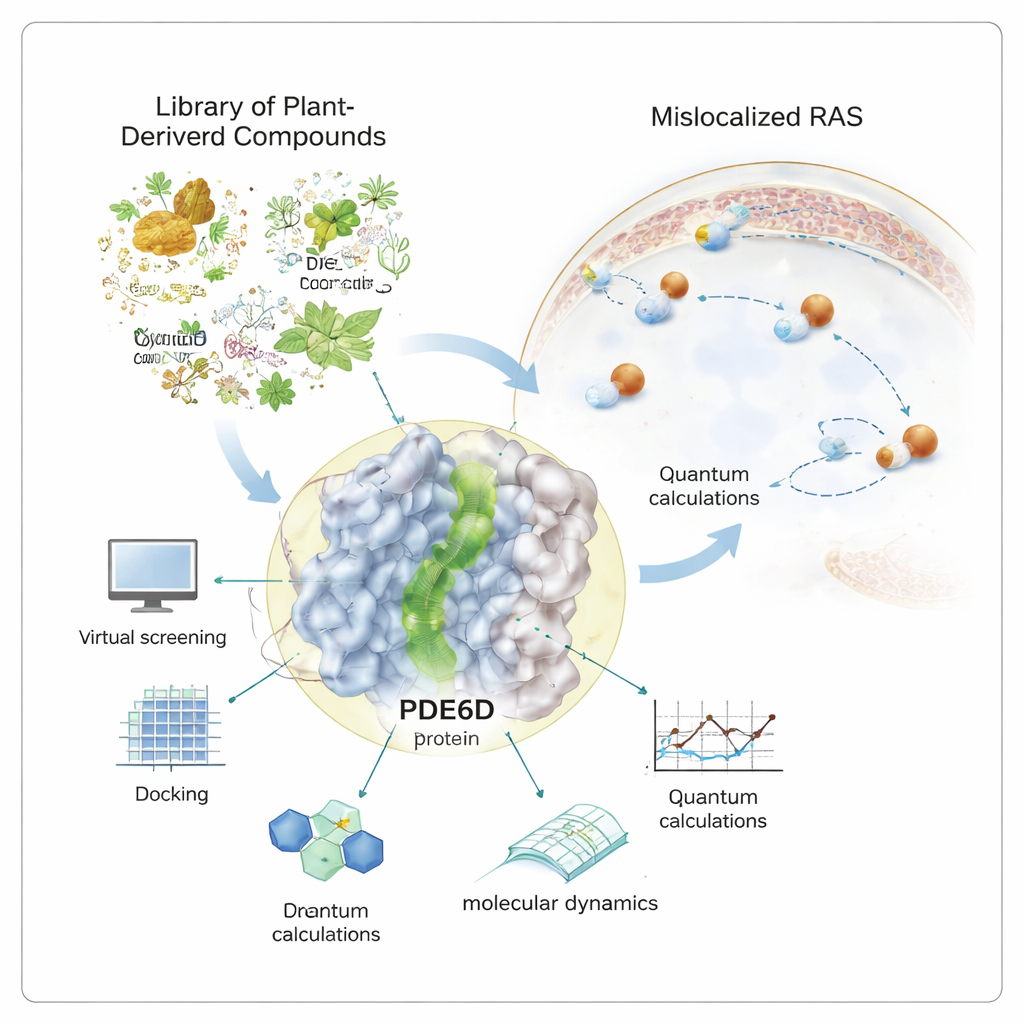
Un assistant caché dans les cellules cancéreuses
Les protéines RAS doivent se trouver à la face interne de la membrane cellulaire pour transmettre des signaux de croissance. Pour y parvenir, elles portent une queue hydrophobe qui leur permet de s’ancrer dans la membrane. Une protéine chaperonne appelée PDE6D agit comme un taxi, protégeant cette queue pendant que RAS traverse l’intérieur aqueux de la cellule. PDE6D possède un tunnel étroit tapissé d’une surface huileuse qui saisit la queue de RAS. Si ce tunnel est bouché, RAS a plus de chances d’aboutir au mauvais endroit, ce qui affaiblit sa capacité à promouvoir le cancer. Comme de nombreux médicaments ciblant RAS ne fonctionnent que pour un sous-ensemble limité de mutations, les chercheurs s’intéressent à PDE6D comme cible indirecte mais potentiellement plus largement pertinente.
Utiliser l’informatique pour fouiller la bibliothèque chimique de la nature
Plutôt que de compter uniquement sur des composés synthétiques, l’auteur s’est tourné vers une bibliothèque soigneusement sélectionnée de plus d’un millier de produits naturels achetables — des molécules d’origine végétale, microbienne ou issues d’autres sources vivantes. Des outils informatiques puissants ont été utilisés pour cribler cette bibliothèque face à la structure 3D de PDE6D. Dans ce test virtuel, chaque molécule a été « dockée » dans le tunnel pour évaluer la qualité et la faveur de son éventuelle liaison. Les candidats les mieux notés ont ensuite été examinés de plus près par des calculs quantiques, qui sondent la répartition électronique de chaque molécule et leur propension à participer à des interactions stabilisantes dans la poche protéique.
Soumettre les candidats prometteurs à l’épreuve du mouvement
Les protéines et les petites molécules ne restent pas immobiles dans les cellules, aussi l’étude est-elle allée au-delà des instantanés statiques. À l’aide de longues simulations de dynamique moléculaire suivant les mouvements atomiques sur une demi-microseconde, le chercheur a observé le comportement de chaque composé naturel prometteur à l’intérieur du tunnel de PDE6D au fil du temps. Deux candidats, désignés MolPort-039-052-621 et MolPort-002-507-186, sont restés logés dans le tunnel avec des réseaux de contacts stables, tandis qu’une troisième molécule a dérivé vers la sortie du tunnel et s’est attachée plus faiblement. Des analyses supplémentaires ont cartographié quelles parties de la structure de PDE6D se sont mises à fléchir ou à se calmer lors de la liaison, et comment le complexe a exploré son « paysage énergétique » — essentiellement quelles conformations étaient les plus confortables et durables. 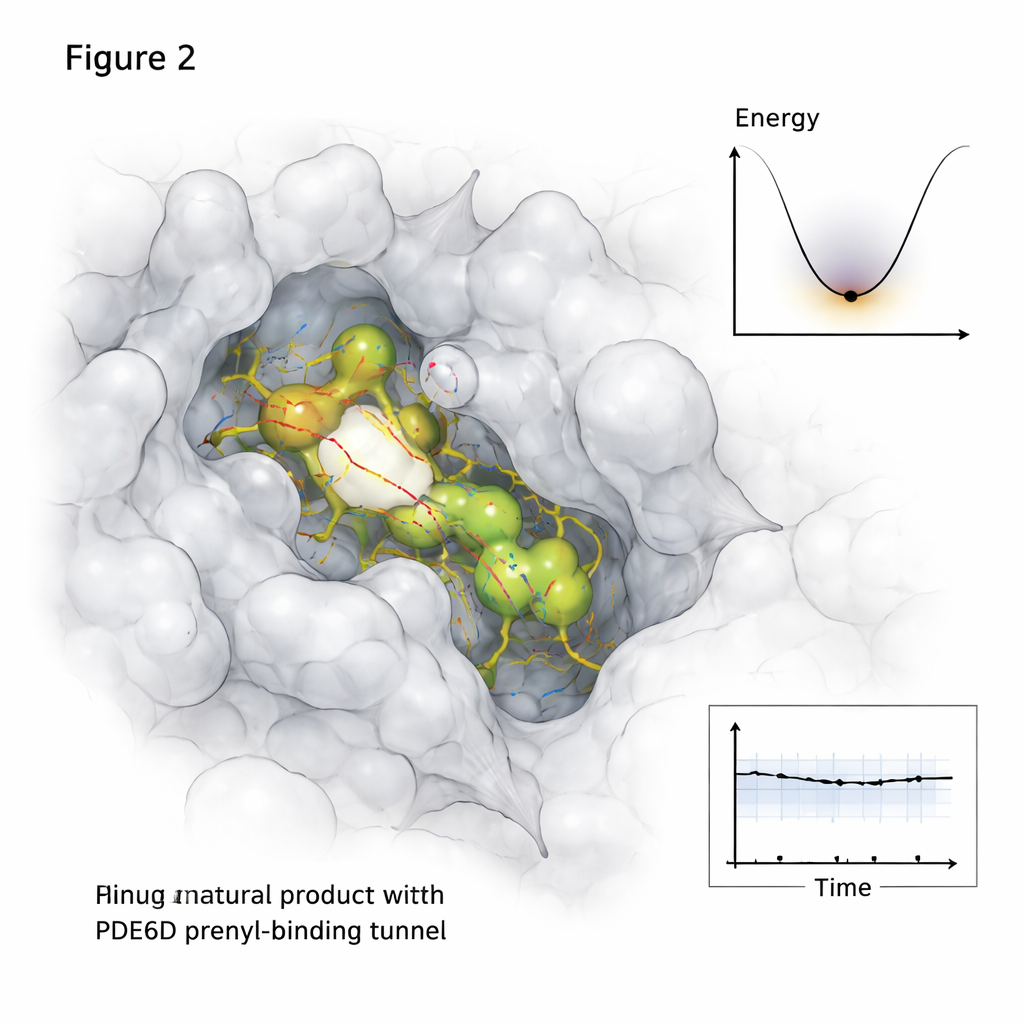
Équilibrer force de liaison et propriétés compatibles avec un médicament
L’étude a également utilisé des outils de prédiction en ligne pour évaluer si ces composés naturels ressemblent à des points de départ réalistes pour des médicaments. Les trois meilleures découvertes présentaient des caractéristiques chimiques compatibles avec une « drug-likeness » de base, mais chacune comportait des signaux d’alerte. Certaines étaient prévues comme ayant une mauvaise absorption ou une faible solubilité ; d’autres montraient des indices de toxicité potentielle, comme des effets sur le rythme cardiaque ou sur l’ADN. Ces problèmes signifient que les molécules, en l’état, sont peu susceptibles d’être des médicaments prêts à l’emploi. Elles constituent plutôt des gabarits structuraux que des chimistes pourraient modifier, conservant les caractéristiques d’ajustement au tunnel tout en éliminant les parties problématiques.
Ce que cela signifie pour les futurs traitements contre le cancer
En termes simples, ce travail ne livre pas un nouveau médicament anticancéreux, mais trace une voie prometteuse. En combinant plusieurs niveaux de calcul — du docking rapide aux simulations détaillées et aux calculs quantiques — l’étude réduit un vaste ensemble de molécules naturelles à un petit groupe qui semblent bien adaptés pour boucher le tunnel de PDE6D. Si des expériences en laboratoire futures confirment que ces composés dévient réellement RAS à l’intérieur des cellules et ralentissent la croissance de tumeurs pilotées par RAS, ils pourraient inspirer une nouvelle classe de traitements ciblant la « logistique » du cancer plutôt que son moteur principal de manière directe.
Citation: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
Mots-clés: Signalisation RAS, Inhibiteurs de PDE6D, produits naturels, découverte de médicaments par calcul, thérapie du cancer