Clear Sky Science · fr
Expression de surface de CD63 et HLA-DR sur les éosinophiles circulants corrèle avec une amélioration du contrôle clinique après optimisation du traitement de l’asthme
Pourquoi ces petites cellules sanguines comptent dans l’asthme
Pour de nombreuses personnes souffrant d’un asthme sévère, des inhalateurs puissants et d’autres médicaments laissent malgré tout un essoufflement persistant et un risque d’exacerbations. Les médecins suivent généralement la maladie avec des numérations de base, des tests d’air expiré et des mesures d’allergie, mais ces indicateurs ne reflètent pas toujours la réalité ressentie par les patients. Cette étude se demande si un examen plus fin d’un type particulier de globule blanc dans le sang — l’éosinophile — peut offrir aux médecins une meilleure fenêtre sur l’efficacité réelle du traitement de l’asthme.
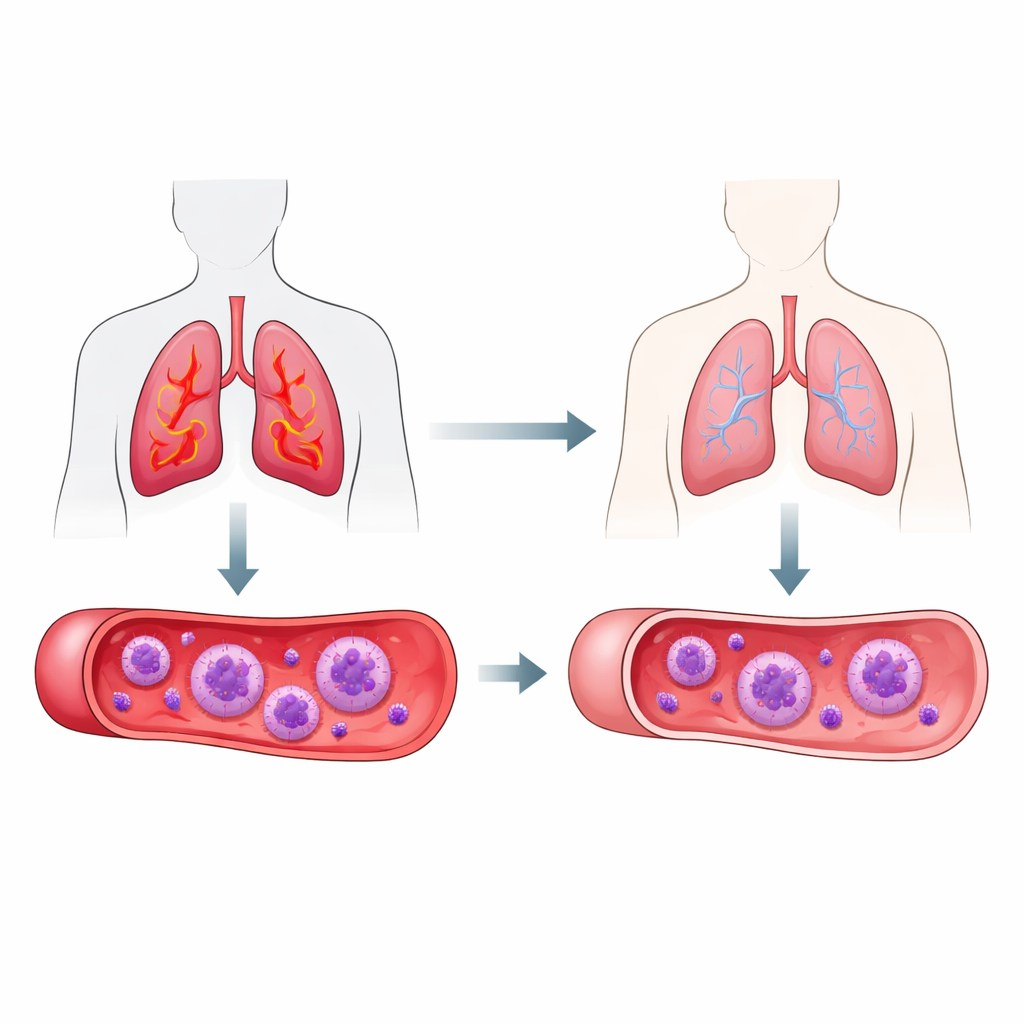
Au‑delà des bilans habituels de l’asthme
L’asthme est animé par une inflammation chronique des voies respiratoires, et les éosinophiles font partie des cellules principales impliquées, notamment dans une forme fréquente appelée asthme de type 2 élevé. Les tests standard comptent principalement combien d’éosinophiles sont présents, mais pas leur niveau d’activation. Les chercheurs se sont focalisés sur deux molécules qui peuvent apparaître à la surface des éosinophiles, nommées CD63 et HLA‑DR. Lorsque ces molécules sont présentes ou augmentées, elles indiquent que les cellules sont plus « activées » et engagées dans la réponse immunitaire. L’idée était que, même si le nombre d’éosinophiles reste identique, des changements dans ces marqueurs de surface pourraient refléter si l’asthme d’un patient devient mieux contrôlé.
Comment l’étude a suivi les patients lors de l’ajustement du traitement
L’équipe a étudié des adultes atteints d’asthme sévère qui étaient évalués en vue de recevoir des injections biologiques ciblant les éosinophiles. Avant de commencer ces médicaments biologiques, les patients ont traversé une période de « run‑in » de trois mois dans une clinique spécialisée, durant laquelle leur traitement habituel a été ajusté avec soin selon les recommandations internationales. Cela comprenait la vérification de la technique d’inhalation et l’intensification des médicaments tels que les corticoïdes inhalés, les bronchodilatateurs longue durée d’action, les antagonistes des leucotriènes et le tiotropium si nécessaire. Au début et à la fin de cette période, les chercheurs ont mesuré les symptômes avec l’Asthma Control Test, enregistré les exacerbations, contrôlé la fonction pulmonaire et prélevé du sang pour analyser les éosinophiles par une technique détaillée appelée cytométrie en flux.
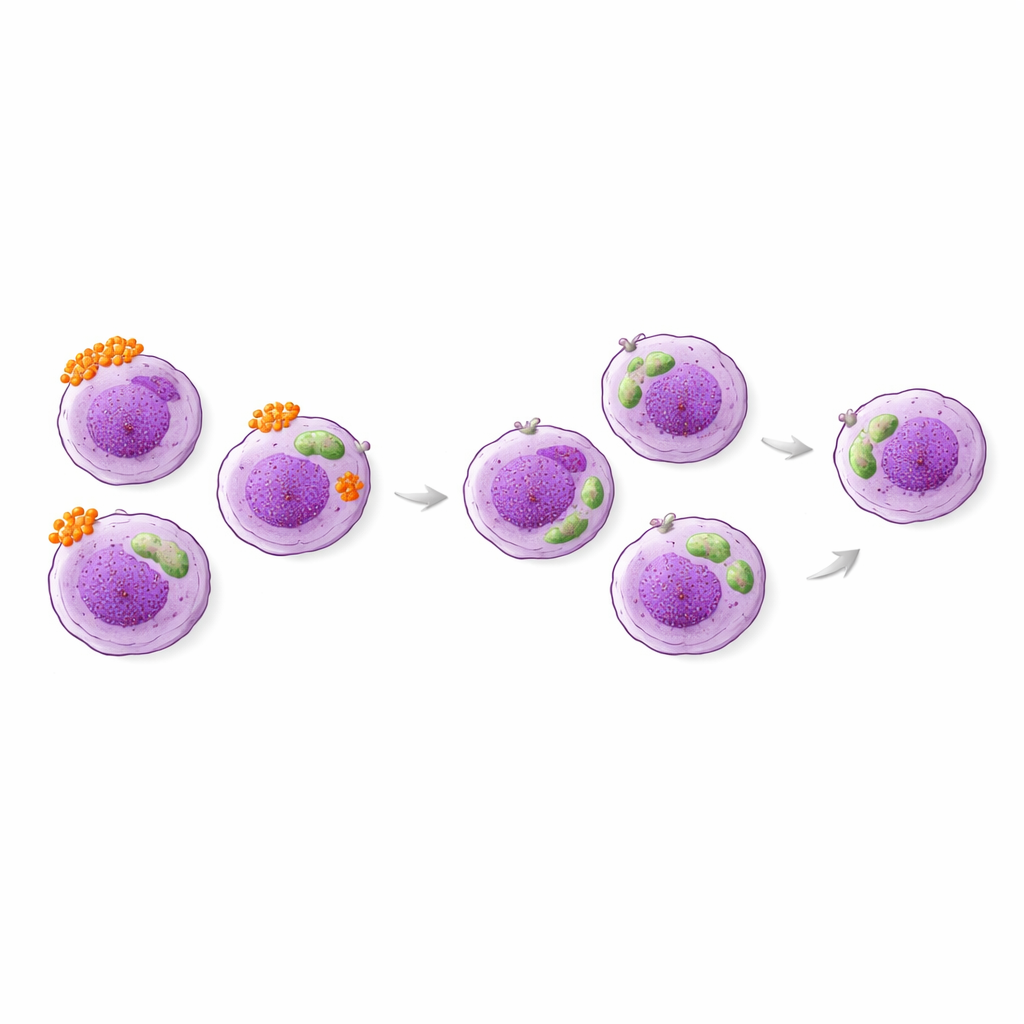
Ce qui a changé dans le sang et ce qui est resté stable
Après trois mois d’optimisation thérapeutique, les patients se sentaient en moyenne mieux : leurs scores de contrôle ont augmenté, et la part de personnes avec un asthme mal contrôlé est passée d’environ la moitié à environ une sur six. L’utilisation de corticoïdes oraux a diminué et les exacerbations sont devenues moins fréquentes. De façon surprenante, les simples numérations d’éosinophiles dans le sang n’ont pas beaucoup bougé, et des marqueurs courants comme le monoxyde d’azote expiré et l’IgE totale n’étaient pas fortement corrélés aux changements de symptômes. En revanche, l’un des marqueurs de surface des éosinophiles — HLA‑DR — a clairement diminué au cours de cette période, tant en proportion de cellules le portant qu’en intensité d’expression. CD63, l’autre marqueur d’activation, n’a pas changé en moyenne mais avait tendance à rester plus élevé chez les patients dont l’asthme demeurait mal contrôlé.
Relier le comportement cellulaire au ressenti des patients
En examinant plus finement, les scientifiques ont constaté que les patients qui présentaient encore des niveaux élevés de HLA‑DR et de CD63 sur leurs éosinophiles après l’ajustement du traitement étaient plus susceptibles d’avoir des symptômes persistants. Des modèles statistiques ont suggéré que les variations de HLA‑DR, en particulier, suivaient modestement les améliorations des scores de symptômes, même si le nombre total d’éosinophiles restait inchangé. Aucun des deux marqueurs ne se raccordait parfaitement aux numérations sanguines habituelles, aux niveaux d’air expiré ou aux mesures d’allergie, ce qui implique que ces caractéristiques de surface captent un aspect différent et plus qualitatif de la maladie. Les auteurs soulignent que ces marqueurs ne doivent pas encore être utilisés pour prédire qui répondra à un médicament donné, mais qu’ils peuvent servir de signes « associés » indiquant que l’inflammation sous‑jacente s’apaise — ou reste active — malgré une thérapie standard.
Ce que cela pourrait signifier pour les personnes souffrant d’un asthme difficile à traiter
L’étude suggère que surveiller le comportement des éosinophiles, plutôt que de se limiter à leur nombre, pourrait aider à personnaliser la prise en charge de l’asthme. Une diminution de HLA‑DR lors d’un ajustement thérapeutique de routine peut indiquer que les médicaments inhalés conventionnels réduisent avec succès l’activité immunitaire, parfois avant l’apparition de changements majeurs dans les symptômes. À l’inverse, des éosinophiles qui continuent d’exprimer des niveaux élevés de HLA‑DR ou de CD63 pourraient signaler des patients dont la maladie reste sourde et qui pourraient bénéficier d’un passage aux thérapies biologiques ou du choix de médicaments ciblant d’autres voies. Bien que des recherches supplémentaires soient nécessaires avant que ces tests n’entrent dans la pratique clinique courante, examiner la « personnalité » des éosinophiles ajoute une couche prometteuse à la compréhension et à la prise en charge de l’asthme sévère.
Citation: Scarlata, S., Mazzuca, C., Vitiello, L. et al. Surface expression of CD63 and HLA-DR in circulating eosinophils correlates with improved clinical control after treatment optimization in asthma. Sci Rep 16, 8289 (2026). https://doi.org/10.1038/s41598-026-37906-z
Mots-clés: asthme sévère, éosinophiles, biomarqueurs, médecine personnalisée, cytométrie en flux