Clear Sky Science · fr
La modélisation à l’échelle cellulaire prédit des stratégies alternatives d’allocation du protéome chez l’archée Methanococcus maripaludis
Pourquoi ces petits producteurs de méthane comptent
Methanococcus maripaludis est une archée microscopique qui transforme des composés simples comme le dioxyde de carbone et le formiate en méthane, un composant majeur du gaz naturel. Comprendre comment ce microbe répartit ses ressources internes — en particulier ses protéines — peut révéler des règles générales de la vie en conditions de limitation énergétique et orienter les efforts pour l’exploiter comme usine biologique de méthane ou comme plateforme de chimie verte.
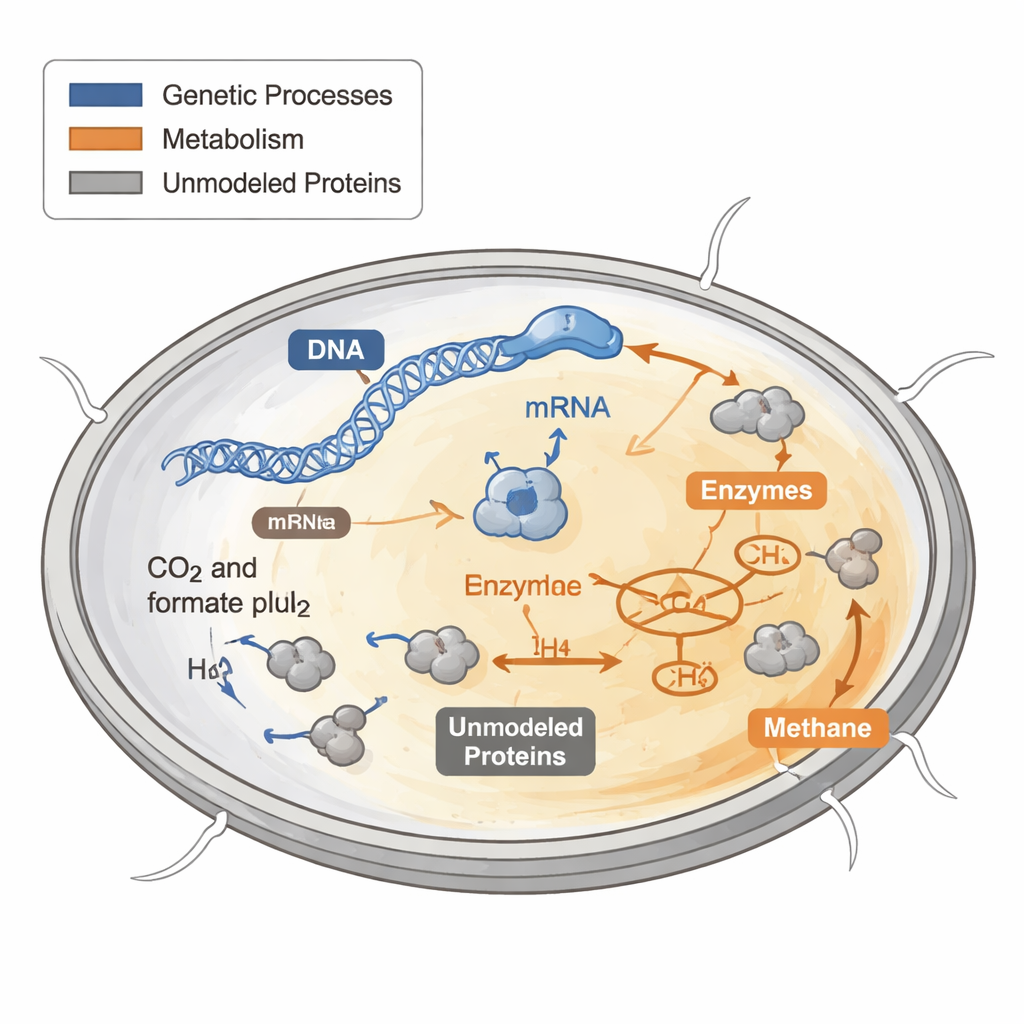
Comment les cellules dépensent leur budget protéique
Toute cellule doit décider comment dépenser son « budget » protéique limité. Certaines protéines construisent de nouvelles parties cellulaires, d’autres récoltent de l’énergie, et d’autres assurent l’entretien. Les modèles informatiques antérieurs du métabolisme traitaient ces protéines comme si elles étaient gratuites et illimitées, ce qui rend les prédictions peu fiables en conditions stressantes ou pauvres en nutriments. Chez les bactéries et les levures, des expériences ont montré que les cellules à croissance rapide consacrent une part plus importante de leur budget protéique aux ribosomes — les machines moléculaires qui fabriquent les protéines — tandis que les cellules à croissance lente réorientent leurs ressources ailleurs.
Une archée qui enfreint les règles
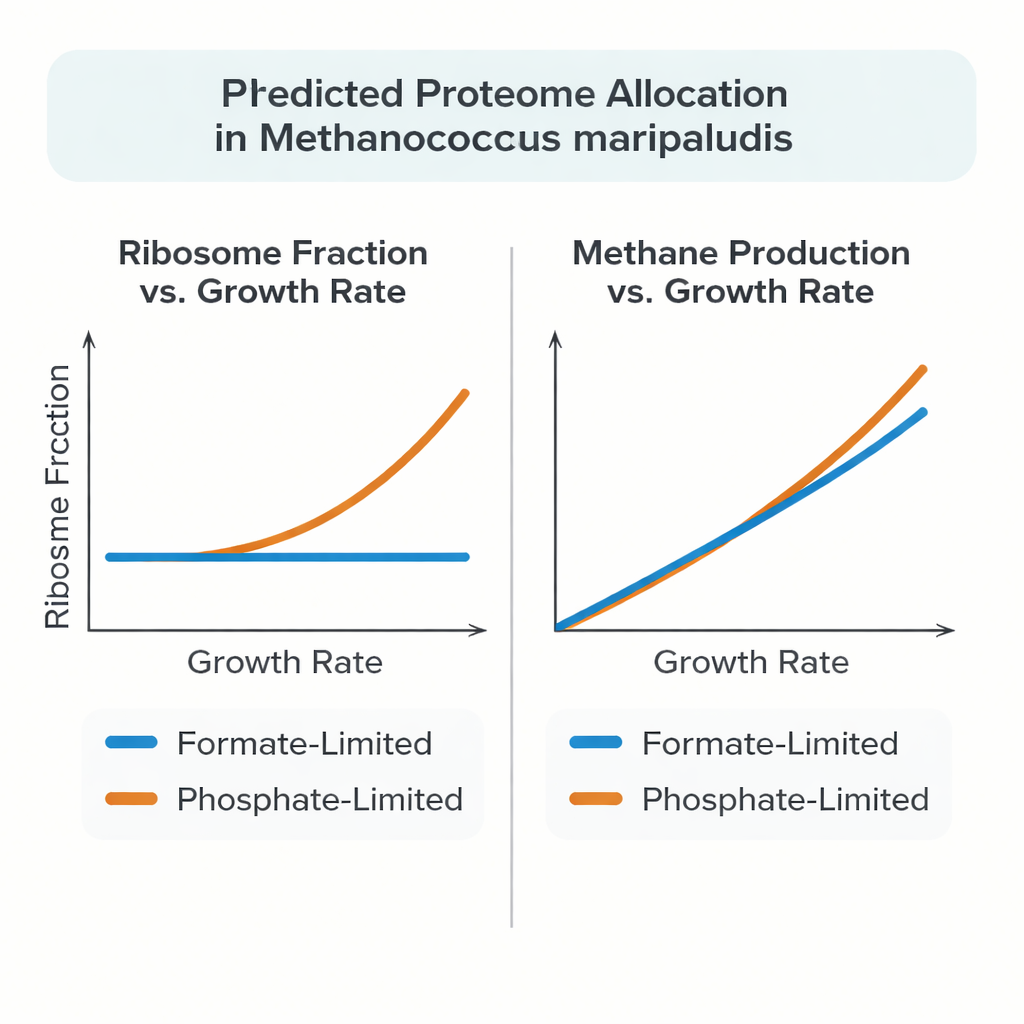
Des expériences récentes ont révélé que M. maripaludis ne suit pas toujours ce schéma. Lorsqu’elle croît en utilisant le formiate comme source à la fois de carbone et d’énergie, la fraction de son budget protéique investie dans les ribosomes reste presque constante lorsque la croissance ralentit. En revanche, sous limitation en phosphate, l’archée adopte un comportement plus conventionnel : la fraction ribosomale augmente avec le taux de croissance, à l’instar d’Escherichia coli et de la levure. Pour expliquer ce comportement inhabituel, les auteurs ont construit un modèle détaillé de type « whole-cell » reliant le métabolisme au processus coûteux de fabrication et d’assemblage des protéines et des ARN, plutôt que de traiter les protéines comme de simples paramètres de vitesse de réaction.
Construire un modèle de type whole-cell
Les chercheurs sont partis d’une carte métabolique existante de M. maripaludis et ont superposé des milliers de réactions supplémentaires décrivant l’expression génique : la transcription de l’ADN en ARN, le chargement des ARNt, l’assemblage des ribosomes et des complexes enzymatiques, et la dilution de ces composants lors de la division cellulaire. Ils ont recueilli les vitesses maximales des enzymes dans des bases de données biochimiques et la littérature, et estimé quelle part de la masse protéique est composée de protéines « non modélisées » qui ne sont pas directement liées aux réactions de la carte. Ils ont ensuite imposé des contraintes globales limitant la masse totale de protéines et d’ARN, reliant les vitesses de réaction à la quantité d’enzyme disponible, et liant la production protéique à la capacité des ribosomes. Avec ces contraintes, le modèle doit choisir comment allouer un budget protéique fixe pour soutenir la croissance.
Ce que révèlent les simulations
Testé sur des expériences de chémostat de haute qualité, le modèle a reproduit avec précision les masses protéiques et d’ARN mesurées, les taux de production de méthane et les rendements de croissance sur une plage de faibles vitesses de croissance. Sous limitation en formiate, la cellule simulée adoptait naturellement une fraction de protéines ribosomales presque constante lorsque la croissance variait, reflétant les données expérimentales. Sous limitation en phosphate, le modèle concordait avec l’augmentation observée de la fraction ribosomale seulement si l’on permettait aux ribosomes de travailler plus vite à faibles taux de croissance, ce qui est cohérent avec des mesures montrant plus de ribosomes actifs dans la synthèse protéique. Le modèle a aussi suggéré qu’une part importante des protéines chez M. maripaludis n’est pas strictement nécessaire à la croissance minimale, et que le carbone et l’énergie excédentaires peuvent être stockés ou détournés vers d’autres macromolécules comme le glycogène ou les acides aminés libres, selon la ressource limitante.
Sonder des mutants et les limites de croissance
Parce que le modèle tient explicitement compte du coût protéique de chaque voie, il peut prédire non seulement si des mutants génétiques croissent, mais aussi comment leur croissance se compare à celle du type sauvage. Les auteurs ont simulé des souches déficientes en différentes enzymes de traitement de l’hydrogène et ont comparé la fitness prédite aux mesures en laboratoire dans plusieurs conditions de croissance, y compris en présence ou en absence d’hydrogène et de monoxyde de carbone. Dans de nombreux cas, le modèle a capté si les mutants pouvaient croître et a fourni des estimations raisonnables de leurs taux de croissance relatifs, améliorant les modèles antérieurs qui ne donnaient que des réponses oui/non. Le même cadre a été utilisé pour estimer les taux de croissance maximaux possibles en conditions batch pour différentes combinaisons de substrats.
Ce que cela signifie pour la science et la technologie
Concrètement, cette étude montre que M. maripaludis utilise une stratégie alternative pour gérer sa main-d’œuvre protéique, maintenant ses « usines » protéiques à une part constante du budget dans certaines conditions plutôt que de les réduire au fur et à mesure que la croissance ralentit. En intégrant ce comportement dans un modèle détaillé et guidé par les données, le travail fournit un banc d’essai pour explorer comment les microbes limités en énergie équilibrent croissance, maintenance et stockage. Pour la recherche appliquée, le modèle offre une feuille de route pour modifier cette archée afin d’augmenter la production de méthane ou d’autres produits en identifiant quelles enzymes et voies sont les plus coûteuses en termes d’investissement protéique. Plus largement, il étend la modélisation de type whole-cell, jusqu’ici centrée sur les bactéries et les levures, au domaine des archées, aidant à combler le fossé entre les détails moléculaires et le comportement à grande échelle des communautés microbiennes impliquées dans le climat, l’énergie et la biotechnologie industrielle.
Citation: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Mots-clés: Methanococcus maripaludis, allocation du protéome, modélisation à l’échelle cellulaire, méthanogenèse, métabolisme des archées