Clear Sky Science · fr
Interleukine-7 induit la transition EMT pour favoriser la croissance tumorale et les métastases dans le NSCLC via la voie Notch1/TGF-β
Pourquoi une protéine de signalisation compte en cancérologie pulmonaire
Le cancer du poumon reste l’un des cancers les plus meurtriers au monde, en grande partie parce qu’il est souvent découvert après s’être déjà propagé. Cette étude se concentre sur un messager immunitaire naturel, l’interleukine‑7 (IL‑7), et pose une question cruciale : dans le cancer du poumon non à petites cellules (NSCLC), l’IL‑7 aide‑t‑elle l’organisme à combattre la tumeur ou favorise‑t‑elle au contraire la croissance et la dissémination tumorales ? En suivant l’effet de l’IL‑7 sur des cellules de cancer du poumon issues de patients, sur des cultures cellulaires et chez la souris, les chercheurs mettent en évidence une voie qui semble pousser les tumeurs vers une croissance, une dissémination et une résistance au traitement accrues.
Un examen attentif des tumeurs pulmonaires et des résultats pour les patients
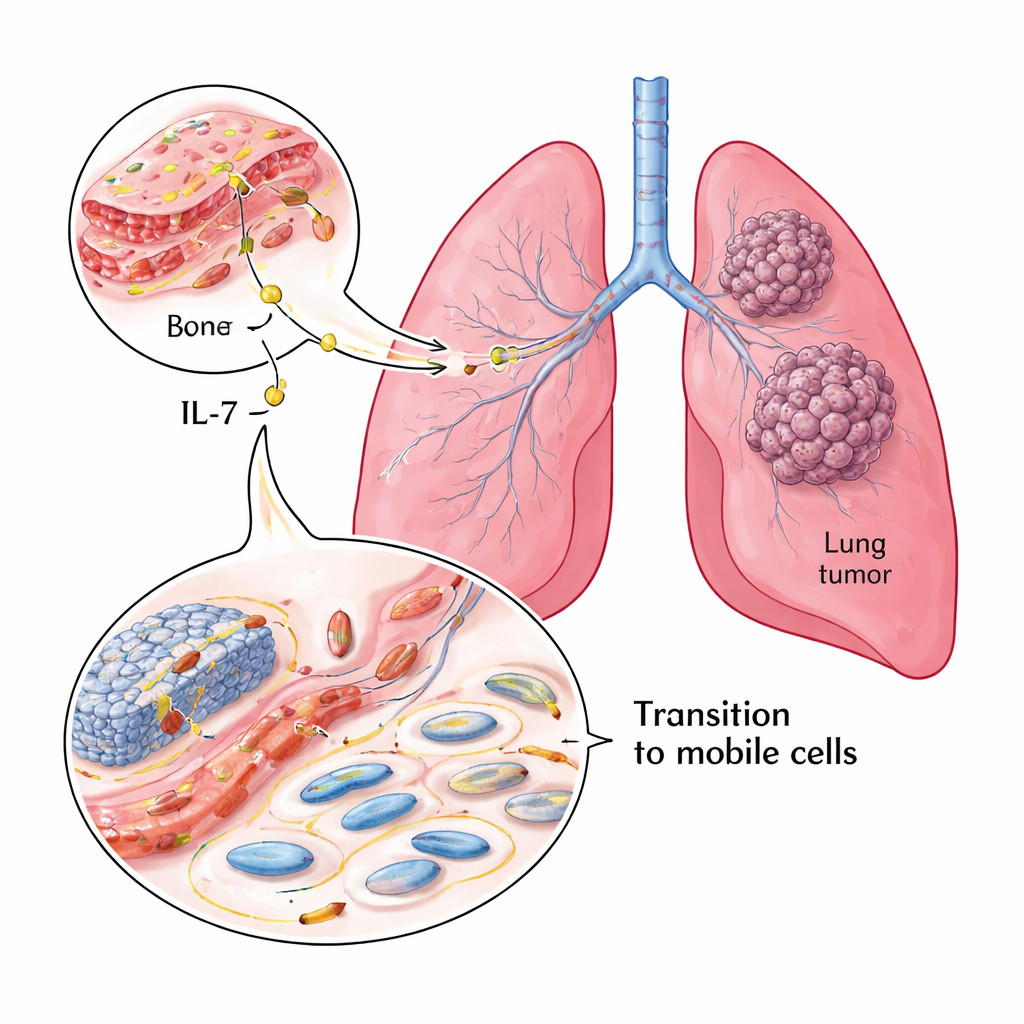
L’équipe a commencé par analyser des échantillons tumoraux de 119 patients atteints de NSCLC. En utilisant des techniques de coloration sur tissus fixés, ils ont mesuré les niveaux d’IL‑7, de son récepteur (IL‑7R) et de deux marqueurs clés qui décrivent à quel point les cellules cancéreuses sont « ancrées » ou « mobiles ». L’E‑cadherine est associée à des cellules fortement connectées et moins mobiles, tandis que la Vimentine est liée à des cellules plus flexibles et invasives. La plupart des tumeurs présentaient des niveaux élevés d’IL‑7 et d’IL‑7R. Quand IL‑7 et IL‑7R étaient abondants, l’E‑cadherine tendait à être faible et la Vimentine élevée : un profil défavorable. Les patients dont les tumeurs conservaient davantage d’E‑cadherine survivaient plus longtemps, tandis que ceux avec une forte expression d’IL‑7R avaient une survie plus courte, faisant de l’IL‑7R un indicateur pronostique puissant.
Comment les cellules cancéreuses passent de l’attachement au détachement
Pour dépasser la simple corrélation, les chercheurs ont testé l’effet direct de l’IL‑7 sur des cellules de NSCLC cultivées en laboratoire. Lorsque deux lignées cellulaires NSCLC ont été exposées à l’IL‑7, les cellules sont passées d’un aspect compact, en pavés, à une forme plus allongée et mobile. À l’intérieur des cellules, les niveaux de protéines ont évolué en conséquence : l’E‑cadherine a diminué, tandis que des marqueurs de « cellules mobiles » tels que la N‑cadherine, la Vimentine et Snail1 ont augmenté. Le cytosquelette d’actine, qui facilite le déplacement cellulaire, est aussi devenu plus proéminent et a formé des protrusions. Le blocage du récepteur IL‑7 a inversé ces effets, indiquant que l’IL‑7 conduit ce changement de morphologie — connu sous le nom de transition épithélio‑mésenchymateuse (EMT) — via son propre récepteur sur les cellules de cancer du poumon.
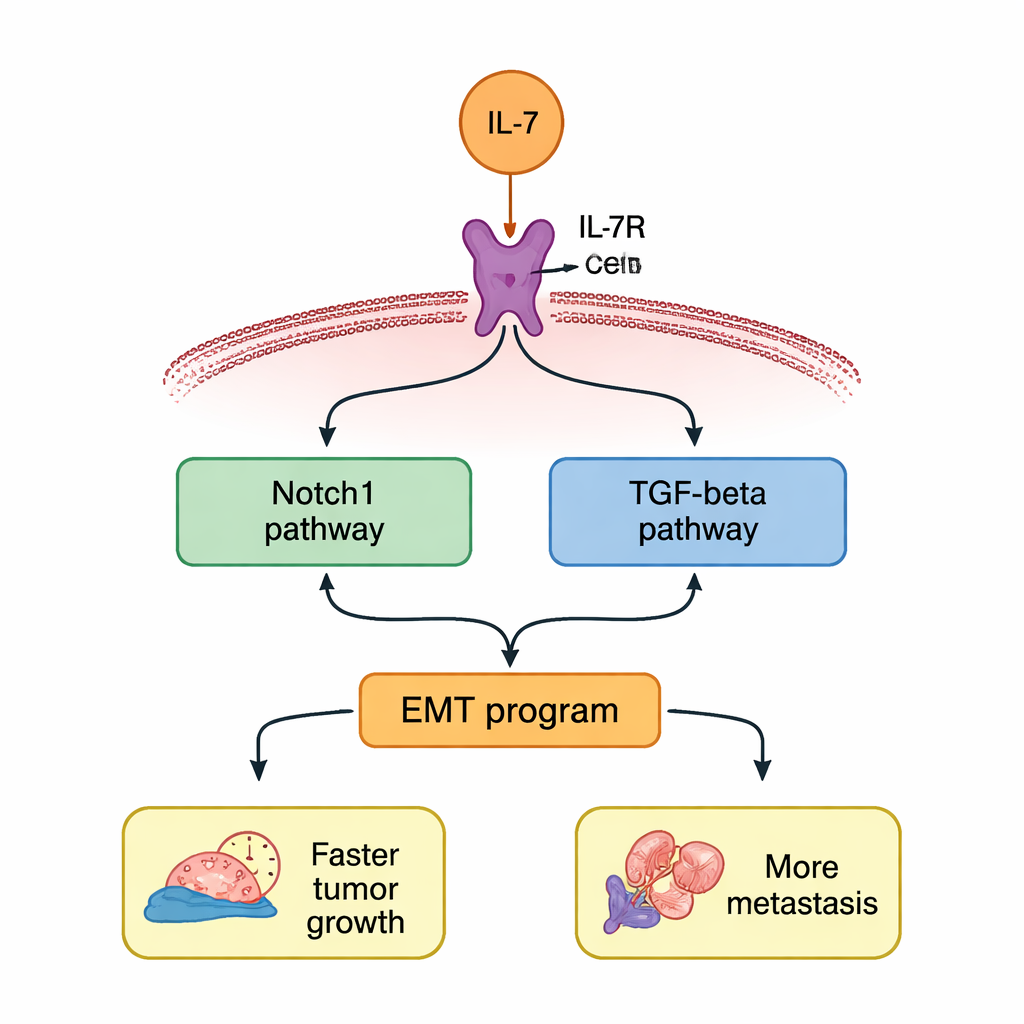
Deux voies liées qui amplifient le danger
L’étude a ensuite cherché à savoir comment l’IL‑7 transmet ces instructions à l’intérieur de la cellule. Les auteurs se sont concentrés sur deux voies de signalisation bien connues, souvent actives dans les cancers agressifs : Notch1 et TGF‑β. Après traitement par l’IL‑7, tant Notch1 que TGF‑β augmentaient au niveau des gènes et des protéines dans les cellules de NSCLC. Si les chercheurs bloquaient IL‑7R, ces augmentations disparaissaient. Lorsque des inhibiteurs spécifiques étaient employés pour cibler Notch1 ou TGF‑β, les deux voies s’atténuaient simultanément, suggérant une boucle de rétroaction positive où chaque voie contribue à entretenir l’autre. Inhiber l’une des voies réduisait partiellement le programme EMT et diminuait le gain en prolifération, migration et invasion induit par l’IL‑7.
Du disque de Petri aux poumons vivants
Pour vérifier si ces observations in vitro se confirmaient in vivo, l’équipe a utilisé des modèles murins. Dans un jeu d’expériences, des cellules de cancer du poumon ont été implantées sous la peau. Les souris traitées par l’IL‑7 développaient des tumeurs plus volumineuses et plus lourdes que les témoins. Les tissus tumoraux de ces animaux présentaient une E‑cadherine plus faible, une Vimentine et Snail1 plus élevées, ainsi qu’une activité accrue de Notch1 et TGF‑β. Quand les souris recevaient en plus des inhibiteurs de Notch1 ou de TGF‑β, la croissance tumorale et ces marqueurs agressifs étaient fortement réduits. Dans un second modèle, des cellules cancéreuses ont été injectées dans la circulation sanguine via la veine caudale. Là aussi, les souris traitées par l’IL‑7 présentaient plus de métastases pulmonaires et des poumons plus lourds, tandis que les médicaments bloquant ces voies limitaient de nouveau la dissémination.
Ce que cela signifie pour la prise en charge future du cancer du poumon
Pris ensemble, ces travaux présentent l’IL‑7 non pas comme un simple auxiliaire immunitaire, mais comme une épée à double tranchant dans le NSCLC. Dans ce contexte, l’IL‑7 semble pousser les cellules tumorales à desserrer leurs liaisons, à adopter une identité plus mobile et à migrer vers de nouveaux sites, via un réseau auto‑entretenu centré sur les voies Notch1 et TGF‑β. Pour les patients, ces résultats suggèrent qu’une forte expression d’IL‑7R dans les tumeurs peut signaler un pronostic plus mauvais et que des thérapies ciblant soigneusement l’axe IL‑7/IL‑7R ou ses voies en aval pourraient aider à ralentir la croissance tumorale et les métastases. Si des recherches supplémentaires sont nécessaires pour cartographier précisément les liens moléculaires et tester la sécurité chez l’homme, cette étude met en lumière un nouvel ensemble de leviers prometteurs pour faire pencher la balance contre le cancer du poumon.
Citation: Shao, Y., Cheng, H., Ni, W. et al. Interleukin-7 induces EMT to promote tumor growth and metastasis in NSCLC via Notch1/TGF-β pathway. Sci Rep 16, 7326 (2026). https://doi.org/10.1038/s41598-026-37876-2
Mots-clés: cancer du poumon non à petites cellules, interleukine-7, transition épithélio-mésenchymateuse, voie Notch1, signalisation TGF-bêta