Clear Sky Science · fr
La voie de signalisation mTOR régule temporellement des étapes clés de la genèse d’organoïdes de la glande mammaire
Pourquoi de petits modèles mammaires comptent
Les seins font partie des rares organes qui se reconstruisent à plusieurs reprises : ils se développent pendant la puberté et la grossesse, produisent du lait, puis diminuent après l’allaitement. Comprendre comment ce remodelage complexe est contrôlé est crucial pour la santé des femmes, que ce soit pour la réussite de l’allaitement ou le risque de cancer. Cette étude utilise de mini « mini-seins » tridimensionnels, appelés organoïdes, cultivés à partir de cellules de souris pour révéler comment un interrupteur maître de croissance à l’intérieur des cellules, connu sous le nom de voie mTOR, chronomètre et façonne le développement du tissu mammaire.
Un feu tricolore cellulaire pour la croissance
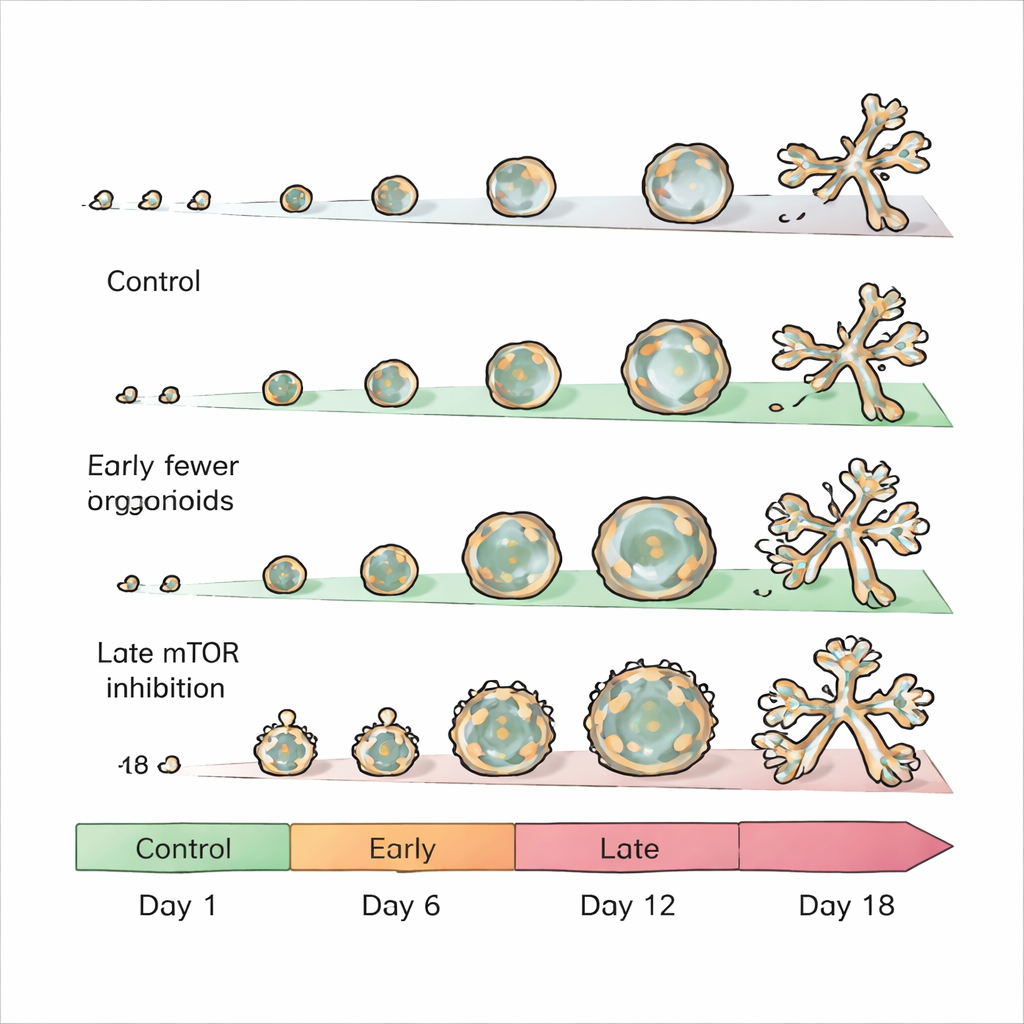
mTOR est un contrôleur central qui aide les cellules à décider quand croître, se diviser et modifier leur métabolisme. Les chercheurs ont étudié comment couper cet interrupteur à différents moments affecterait le développement des organoïdes. Ils ont cultivé des cellules épithéliales mammaires de souris dans un gel qui leur permet de s’auto-organiser en structures ressemblant à de petits conduits mammaires avec un centre creux et, parfois, des amas branchés en « grappe ». Ils ont ensuite ajouté des médicaments bien connus bloquant mTOR, le rapamycine et le torin 1, soit très tôt, au milieu de la croissance, soit plus tard, au moment où la ramification commence habituellement.
Interférence précoce : des mini-organes qui ne se forment jamais vraiment
Lorsque mTOR a été bloqué dès le premier jour, les organoïdes ont à peine poussé. Leur diamètre a été réduit d’environ les deux tiers ou plus, montrant que mTOR actif est essentiel pour l’expansion précoce du tissu mammaire. Cela concorde avec la réputation de mTOR comme moteur de la croissance cellulaire et de la production protéique. Parce que ces organoïdes restaient si petits et peu développés, l’équipe s’est concentrée sur des fenêtres de traitement plus tardives, où les effets étaient plus nuancés et éclairaient davantage la manière dont l’architecture interne du tissu est contrôlée.
Changement en cours de route : sphères creuses et perte de plasticité
Bloquer mTOR à partir d’environ le jour 6 — après la formation des structures initiales mais avant la ramification — a produit des organoïdes étonnamment grands et majoritairement creux. Ceux-ci étaient dominés par des cellules luminales, les cellules internes qui tapissent normalement les conduits sécréteurs de lait, tandis que la couche cellulaire basale externe était presque complètement perdue. Dans un développement sain, des cellules luminales ou basales individuelles peuvent chacune donner naissance à des organoïdes contenant les deux types cellulaires, une propriété connue sous le nom de plasticité de lignée. L’inhibition de mTOR à ce stade intermédiaire a essentiellement figé cette flexibilité, forçant les cellules vers une identité luminale et empêchant l’équilibre habituel des couches. Les analyses moléculaires ont montré des changements étendus dans l’expression génique et protéique, en particulier des réductions des composants de la machinerie métabolique cellulaire et des protéines qui aident à remodeler la matrice de soutien environnante — des modifications qui expliquent en partie la forme et la composition cellulaire altérées.
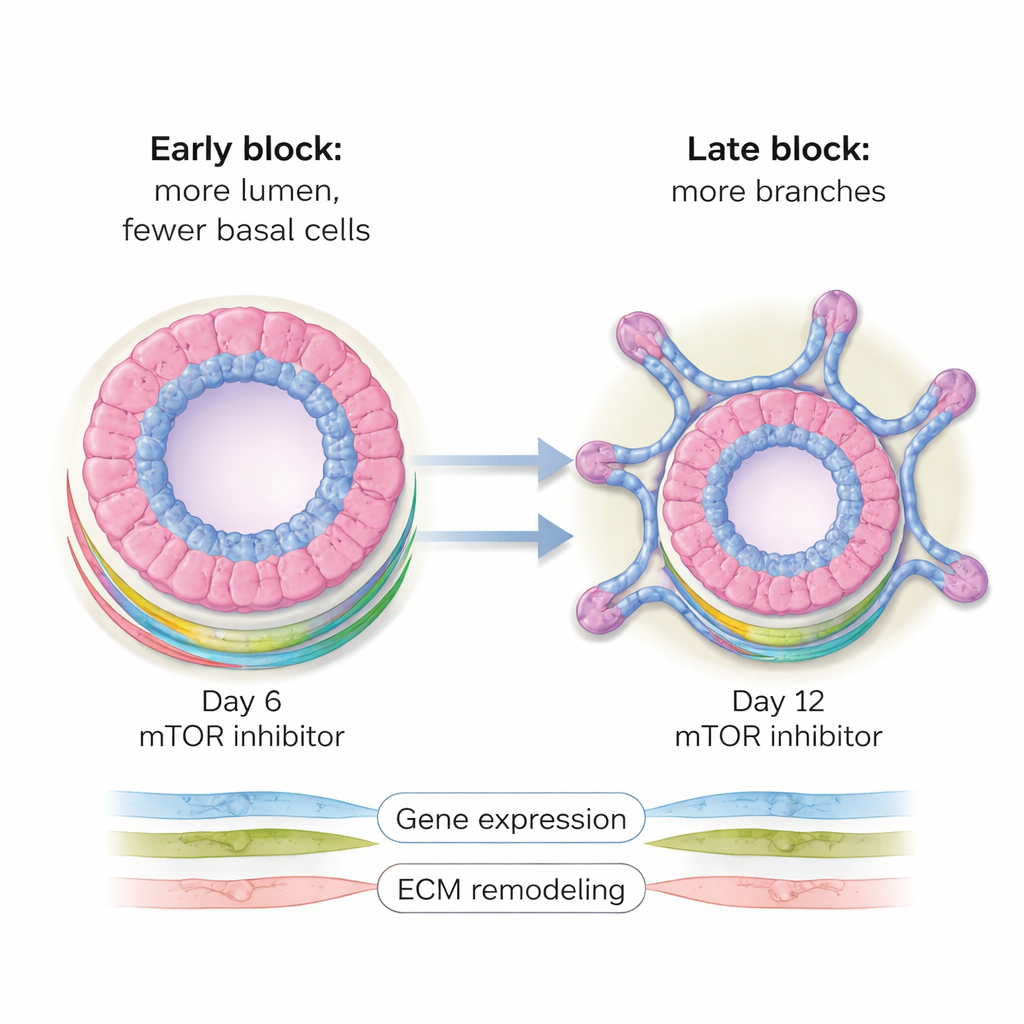
Interruption tardive : plus de branches, un câblage différent
Lorsque les mêmes médicaments ont été ajoutés plus tard, autour du jour 12, au moment où la ramification commence typiquement, le résultat s’est inversé. Au lieu de sphères creuses agrandies, les organoïdes ont alors formé plus de structures branchées et plus complexes, en forme de bourgeons, qui ressemblaient aux petites vésicules où le lait est produit. Dans ce contexte, l’équilibre entre cellules luminales et basales était largement préservé, mais le nombre de branches et de bourgeons a augmenté de façon substantielle par rapport aux contrôles non traités. Les profils d’activité génique reflétaient ce basculement : de nombreux gènes liés à la mise en forme des tissus et à la ramification étaient up-régulés, tandis que beaucoup impliqués dans le métabolisme étaient down-régulés. Les mesures au niveau des protéines confirmaient ces observations, mettant en évidence des changements dans des composants de la matrice extracellulaire et des voies métaboliques, notamment le métabolisme des acides aminés et de l’énergie.
Ce que cela signifie pour les seins réels
Pris ensemble, ces travaux montrent que mTOR n’est pas un simple interrupteur de croissance marche/arrêt mais un coordinateur sensible au temps de l’identité cellulaire et de l’architecture tissulaire dans la glande mammaire. Au début, mTOR actif est nécessaire pour que les cellules croissent et conservent la flexibilité de devenir soit des cellules luminales internes soit des cellules basales externes. Plus tard, la modulation de l’activité de mTOR reconfigure la façon dont les cellules interagissent avec leur environnement pour soit atténuer soit renforcer la formation de structures ramifiées productrices de lait. Pour un non-spécialiste, le message principal est que la même voie moléculaire peut avoir des rôles très différents selon le moment où elle agit — d’abord en contribuant à fabriquer les bons types cellulaires, puis en les sculptant dans la bonne forme tridimensionnelle. Cette vision nuancée sera importante pour comprendre le développement mammaire normal, l’impact des médicaments ciblant mTOR et, possiblement, comment des altérations précoces de cette voie pourraient contribuer aux maladies du sein.
Citation: Lacouture, A., Sylla, M.S., Germain, L. et al. The mTOR signaling pathway regulates key steps of mammary gland organoid genesis in a temporal manner. Sci Rep 16, 6751 (2026). https://doi.org/10.1038/s41598-026-37825-z
Mots-clés: développement de la glande mammaire, signalisation mTOR, organoïdes, <keyword>biologie du sein