Clear Sky Science · fr
Modélisation et application de la prédiction de traits complexes de la maladie d’Alzheimer basée sur l’apprentissage multitâche
Pourquoi cette recherche compte pour les familles et les patients
La maladie d’Alzheimer est l’un des diagnostics les plus redoutés de notre époque, et pourtant les médecins peinent encore à prédire qui déclinera rapidement, qui restera stable pendant des années et quels signes précoces sont vraiment significatifs. Cette étude pose une question simple mais puissante : si l’on considère plusieurs résultats de tests et scans cérébraux liés à la maladie d’Alzheimer simultanément, et que l’on combine ces mesures avec les informations génétiques d’une personne, l’intelligence artificielle moderne peut-elle apprendre des motifs qui aident à prévoir l’évolution de la maladie de manière plus précise ?
Les multiples visages d’une même maladie
L’Alzheimer n’est pas uniquement une perte de mémoire. Les patients diffèrent dans leurs performances aux tests cognitifs, dans leur capacité à gérer les activités quotidiennes et dans l’apparence de leurs images cérébrales. Ces différentes mesures — comme les échelles courantes de mémoire et de cognition, les questionnaires sur le fonctionnement quotidien et les scans PET du métabolisme cérébral ou de l’accumulation d’amyloïde — sont partiellement influencées par la génétique. De façon importante, elles partagent aussi certains déterminants génétiques. Les méthodes de prédiction traditionnelles se concentrent généralement sur une mesure à la fois, négligeant le fait utile que ces traits sont liés. Les auteurs défendent l’idée que, comme un clinicien qui considère l’ensemble plutôt qu’un seul test, les modèles devraient apprendre à partir de plusieurs traits simultanément.
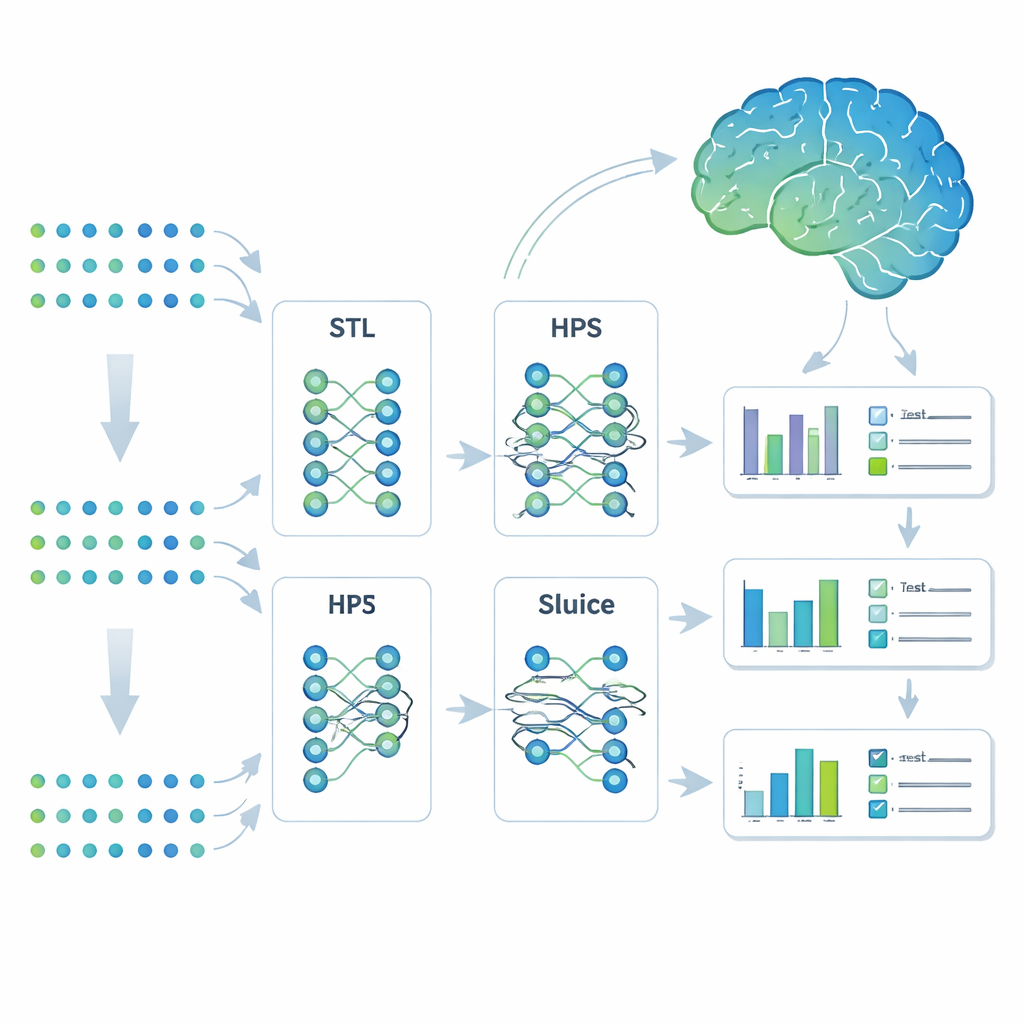
Apprendre plusieurs tâches avec un seul modèle
Les chercheurs ont recours à une stratégie d’apprentissage automatique appelée apprentissage multitâche. Plutôt que de construire des modèles séparés pour chaque résultat, ils ont entraîné un seul système pour prédire simultanément sept traits liés à l’Alzheimer. Ils ont comparé quatre approches : des modèles entièrement séparés (apprentissage mono-tâche), un modèle partagé simple ne divergeant qu’en fin de réseau (partage dur des paramètres), une architecture de branchement plus souple permettant de scinder les tâches en sous-groupes, et un dispositif très adaptable nommé Sluice Network qui peut affiner la quantité d’information partagée à chaque couche du réseau. Les quatre modèles ont reçu les mêmes entrées génétiques ; la différence tenait à la manière dont ils partageaient ce qu’ils apprenaient entre les traits.
Tester les idées sur des génomes simulés
Avant de faire confiance à un modèle sur des patients réels, l’équipe a construit des simulations détaillées en s’appuyant sur des schémas génétiques réels issus de l’Alzheimer’s Disease Neuroimaging Initiative (ADNI) mais avec des résultats qu’ils pouvaient entièrement contrôler. Ils ont créé des scénarios où tous les traits partageaient les mêmes causes génétiques, où les traits formaient des groupes qui se chevauchent, et où chaque trait avait des causes distinctes. Ils ont également fait varier la force des signaux génétiques et le niveau de bruit, reproduisant la réalité bruitée des données humaines. Dans presque toutes les conditions, le Sluice Network a fourni les prédictions les plus précises et est resté stable même lorsque les traits n’étaient que faiblement liés. Les modèles partagés plus simples fonctionnaient bien lorsque les traits avaient de nombreux facteurs génétiques en commun mais faiblissaient quand ce partage était faible, tandis que les modèles complètement séparés étaient constants mais globalement moins précis.
Données réelles et puissance du regroupement des gènes
Les auteurs ont ensuite appliqué ces modèles aux données réelles de l’ADNI provenant de 463 individus, en utilisant près de 3 800 marqueurs génétiques issus de 56 gènes précédemment associés à l’Alzheimer. Ils ont introduit une nuance biologiquement inspirée : au lieu d’entrer des milliers de marqueurs individuels séparément, ils ont d’abord groupé les marqueurs par gène et laissé le réseau apprendre un signal « résumé » compact pour chaque gène avant de prédire les sept résultats. Cette agrégation au niveau des gènes a amélioré les performances pour la plupart des modèles et en particulier pour le Sluice Network, qui a presque doublé sa corrélation moyenne avec les résultats réels. Les gains étaient les plus nets pour les mesures d’imagerie PET et certaines scores cognitifs et fonctionnels, suggérant que des effets génétiques subtils deviennent plus détectables lorsqu’ils sont combinés au niveau du gène plutôt que traités comme des marqueurs isolés.
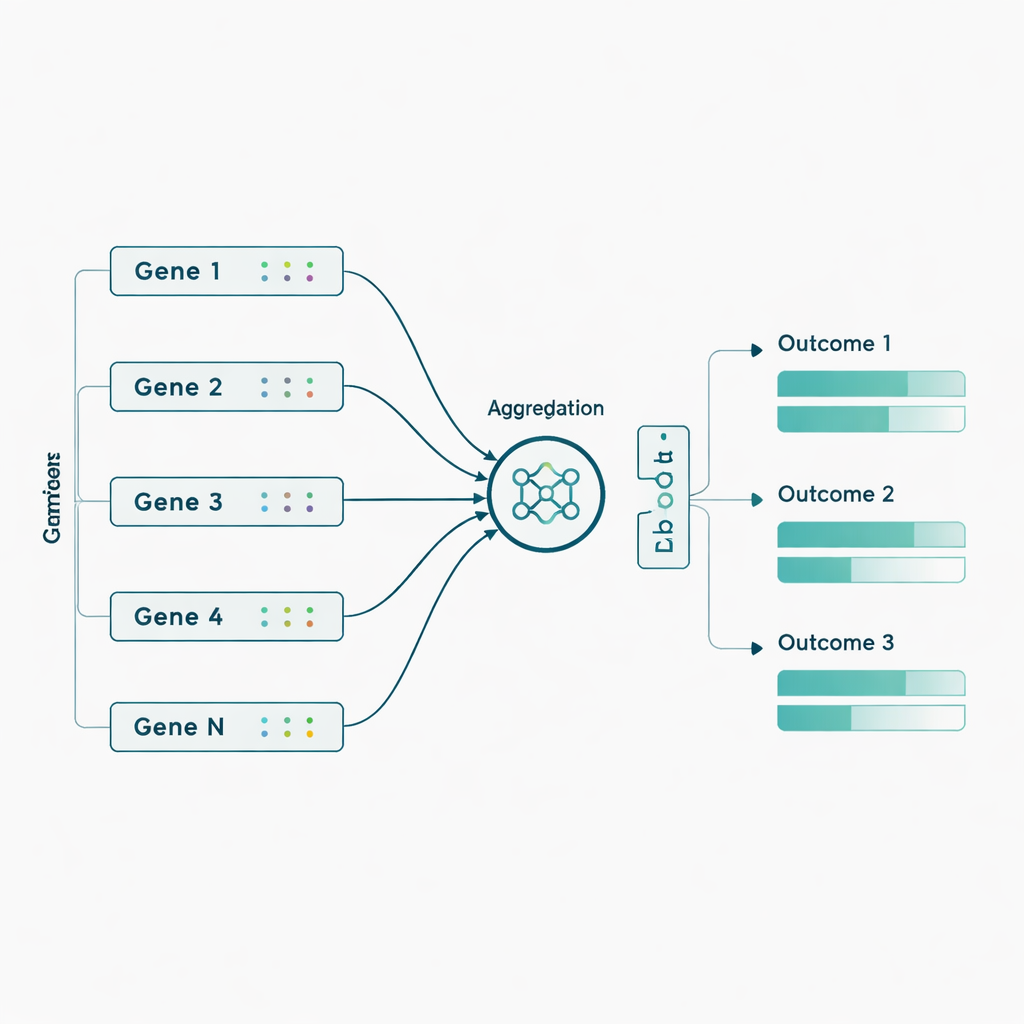
Ce que cela signifie pour la prédiction et les soins futurs
Pour un non-spécialiste, le message est que des modèles d’IA plus intelligents et plus flexibles peuvent extraire davantage d’informations des mêmes données génétiques et cliniques en apprenant à partir de plusieurs résultats liés simultanément et en respectant l’organisation biologique en gènes. Bien que les gains actuels soient modestes et loin d’un test clinique, l’approche ouvre la voie à des outils plus fiables pour estimer le profil de risque d’une personne, suivre la progression probable et peut‑être adapter la surveillance ou les interventions. Dans des maladies complexes comme l’Alzheimer, où de nombreux petits effets génétiques interagissent, les méthodes qui partagent l’information entre traits et agrègent des signaux faibles peuvent offrir une image plus claire et plus informative que les scores traditionnels analysés trait par trait.
Citation: Zhou, W., Xue, Z., Liang, J. et al. Modeling and application of alzheimer’s disease complex trait prediction based on multi-task learning. Sci Rep 16, 7749 (2026). https://doi.org/10.1038/s41598-026-37820-4
Mots-clés: Génétique de la maladie d’Alzheimer, apprentissage multitâche, prédiction par apprentissage profond, biomarqueurs en neuroimagerie, agrégation au niveau des gènes