Clear Sky Science · fr
Les exosomes dérivés de cellules épithéliales amniotiques humaines contenant le miR-25-3p augmentent l’expression de mucine dans les cellules caliciformes conjonctivales via la régulation négative de BCL2L11
Pourquoi une surface oculaire plus lisse compte
Quiconque a souffert d’yeux secs et irrités sait combien un film lacrymal sain est essentiel pour une vision nette et confortable. Une composante clé de cette couche protectrice est le mucus produit par de petites « usines » appelées cellules caliciformes, qui tapissent la sclère et la face interne des paupières. Lorsque ces cellules sont endommagées ou perdues, comme dans la sécheresse oculaire ou lors d’états inflammatoires sévères, la surface de l’œil devient vulnérable. Cette étude explore une thérapie émergente « sans cellules » qui utilise de minuscules paquets libérés par des tissus placentaires donnés pour aider les cellules caliciformes à survivre et à produire davantage du mucus qui maintient nos yeux humides et protégés.
De minuscules colis livrés par le tissu de naissance
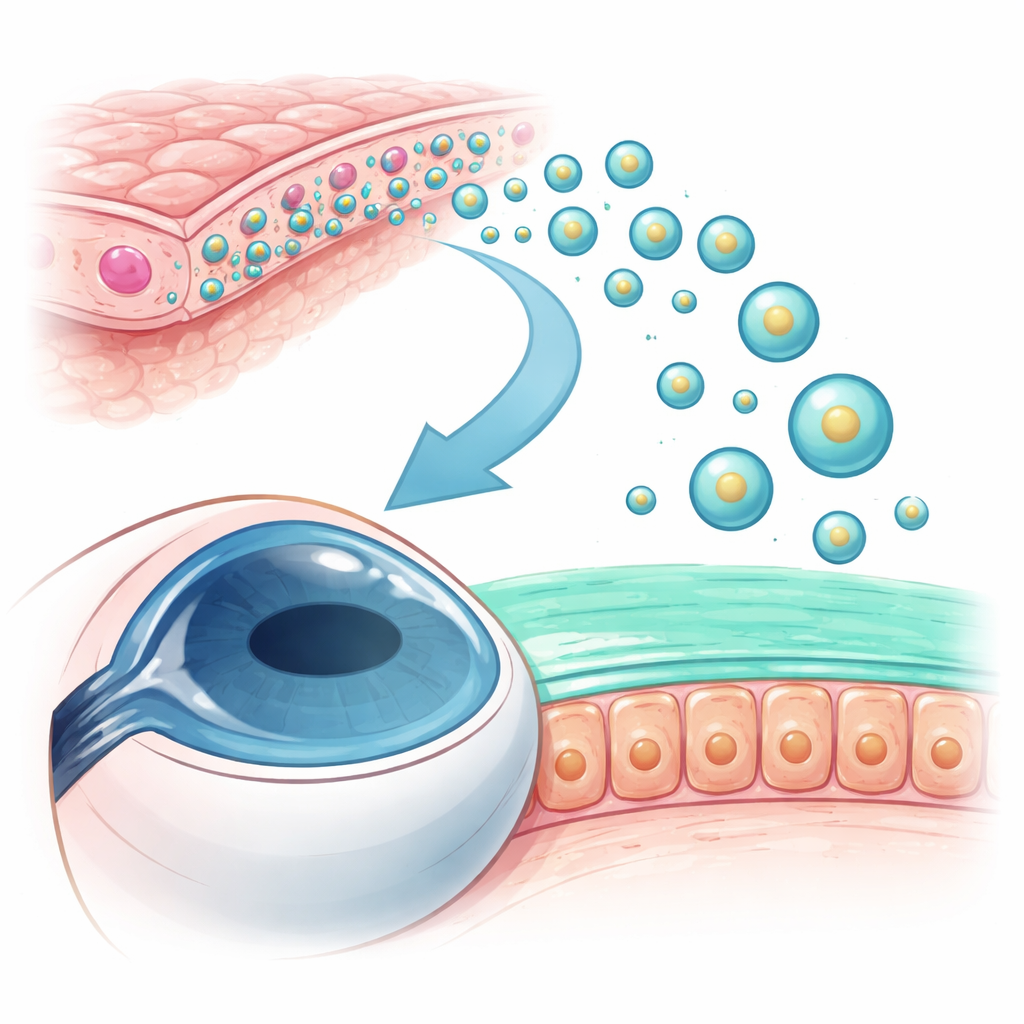
Les chercheurs se sont concentrés sur les cellules épithéliales amniotiques humaines, issues de la fine membrane entourant le fœtus pendant la grossesse et déjà reconnues pour leurs propriétés cicatrisantes et anti-inflammatoires. Ces cellules libèrent des bulles de taille nanométrique, appelées exosomes, qui transportent protéines et régulateurs génétiques d’une cellule à l’autre. L’équipe a isolé ces vésicules à partir de cultures de cellules amniotiques, confirmé leur aspect typique en forme de coupe et leur gamme de tailles au microscope électronique, et vérifié la présence de protéines marqueurs d’exosomes bien connues. Cette étape de caractérisation a montré qu’ils avaient obtenu une préparation propre des petits colis qu’ils souhaitaient tester.
Un message microscopique pour les cellules de surface oculaire
La question suivante était de savoir si ces exosomes pouvaient atteindre et influencer les cellules caliciformes conjonctivales, ces cellules productrices de mucus si importantes pour le confort oculaire. Les scientifiques ont marqué les exosomes avec un colorant fluorescent et les ont ajoutés à des cellules caliciformes humaines cultivées en plaque. Au microscope, ils ont observé des signaux lumineux à l’intérieur des cellules, en particulier à des doses d’exosomes plus élevées, confirmant que les cellules caliciformes absorbent aisément ces petits colis. À l’intérieur des exosomes, ils ont identifié une petite molécule d’ARN particulière, le miR-25-3p, protégée des enzymes dégradantes, et ont montré que le blocage de la production d’exosomes dans les cellules sources réduisait fortement la libération de cette molécule. Ensemble, ces tests ont révélé que le miR-25-3p est principalement exporté dans les exosomes et peut être délivré directement aux cellules caliciformes.
Aider les « usines à mucus » à mieux fonctionner et à survivre
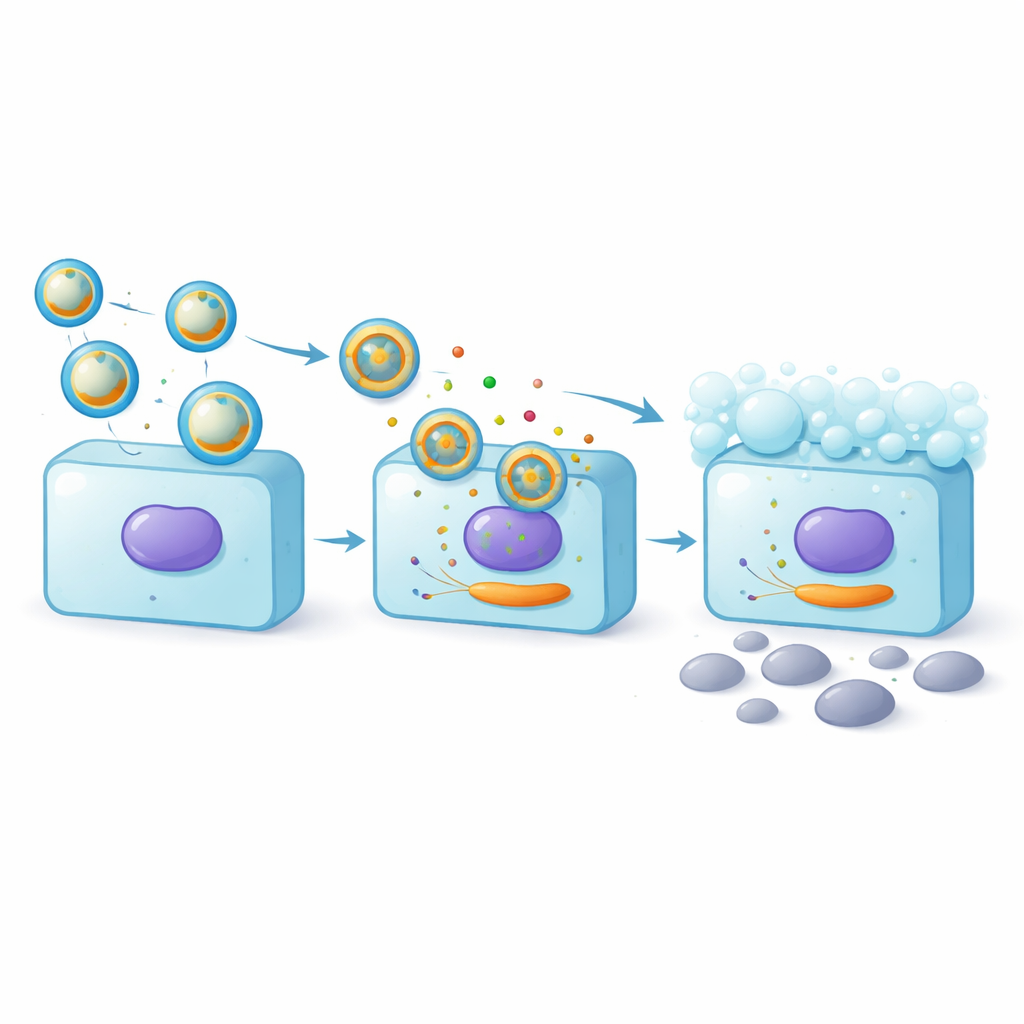
Une fois cette voie de livraison établie, les auteurs ont examiné ce qui arrivait aux cellules caliciformes après réception d’exosomes d’origine amniotique. Les cellules traitées par exosomes produisaient davantage de MUC5AC, un composant majeur du mucus qui forme le film glissant et protecteur à la surface de l’œil. Les mesures de la protéine à l’intérieur des cellules et de la quantité sécrétée dans le milieu ont montré une augmentation nette, dépendante de la dose. Parallèlement, moins de cellules caliciformes présentaient des signes de mort cellulaire programmée, ce qui signifie que le traitement aidait à leur survie. Lorsque les chercheurs ont augmenté directement les niveaux de miR-25-3p, ces effets bénéfiques se sont renforcés, désignant ce petit ARN comme un ingrédient actif clé à l’intérieur des exosomes.
Désactiver un déclencheur de mort cellulaire
Pour comprendre comment le miR-25-3p protège les cellules caliciformes, l’équipe a recherché sa cible moléculaire et s’est focalisée sur BCL2L11, un gène promoteur de la mort cellulaire. À l’aide d’un système rapporteur, ils ont confirmé que le miR-25-3p peut se lier au message de BCL2L11 à l’intérieur de la cellule et en atténuer l’activité. Les cellules caliciformes exposées aux exosomes amniotiques présentaient des niveaux réduits de BCL2L11, en particulier lorsque les exosomes étaient enrichis en miR-25-3p. Lorsque les chercheurs ont artificiellement augmenté l’expression de BCL2L11, une partie des effets protecteurs du miR-25-3p a disparu : la mortalité cellulaire a de nouveau augmenté et la production de mucus a diminué. Cette lutte d’équilibre démontre qu’une part importante du bénéfice des exosomes provient du miR-25-3p qui réprime BCL2L11 et soutient ainsi à la fois la survie des cellules caliciformes et la production de mucus.
Que cela pourrait signifier pour les personnes souffrant de sécheresse oculaire
En termes simples, cette étude montre que de minuscules colis libérés par des tissus de naissance donnés peuvent délivrer un message génétique protecteur aux cellules productrices de mucus de l’œil. Ce message, porté par le miR-25-3p, aide à désactiver un commutateur d’autodestruction et encourage les cellules caliciformes à produire davantage du mucus qui maintient la surface oculaire lisse et protégée. Bien que ces expériences aient été réalisées en laboratoire et que des travaux supplémentaires sur des modèles animaux et des patients soient nécessaires, les résultats décrivent une stratégie prometteuse sans cellules : utiliser des exosomes purifiés plutôt que des cellules entières pour restaurer un film lacrymal sain et potentiellement soulager les pathologies où la surface oculaire devient sèche, enflammée et fragile.
Citation: Zhang, Y., Wu, W., Meng, T. et al. Human amnion epithelial cell-derived exosomal miR-25-3p enhances mucin expression in conjunctival goblet cells via downregulating BCL2L11. Sci Rep 16, 7958 (2026). https://doi.org/10.1038/s41598-026-37794-3
Mots-clés: sécheresse oculaire, film lacrymal et mucus, exosomes, thérapie de la surface oculaire, cellules caliciformes