Clear Sky Science · fr
Évaluation préliminaire de la biodistribution et du ciblage de la sonde moléculaire fluorescente Cy7-SYL3C dans un modèle murin de cancer colorectal positif pour EpCAM
Pourquoi ceci compte pour la détection du cancer
Le cancer colorectal figure parmi les causes de mortalité par cancer les plus importantes dans le monde, en partie parce que de nombreuses tumeurs sont diagnostiquées tardivement. L’outil de dépistage actuel majeur, la coloscopie, est efficace mais invasive et désagréable, ce qui décourage beaucoup de personnes. Cette étude explore un nouveau type de « traceur intelligent » fluorescent qui pourrait, un jour, aider les médecins à voir les tumeurs intestinales plus tôt et plus clairement, en utilisant la lumière plutôt qu’un scalpel ou un tube long.
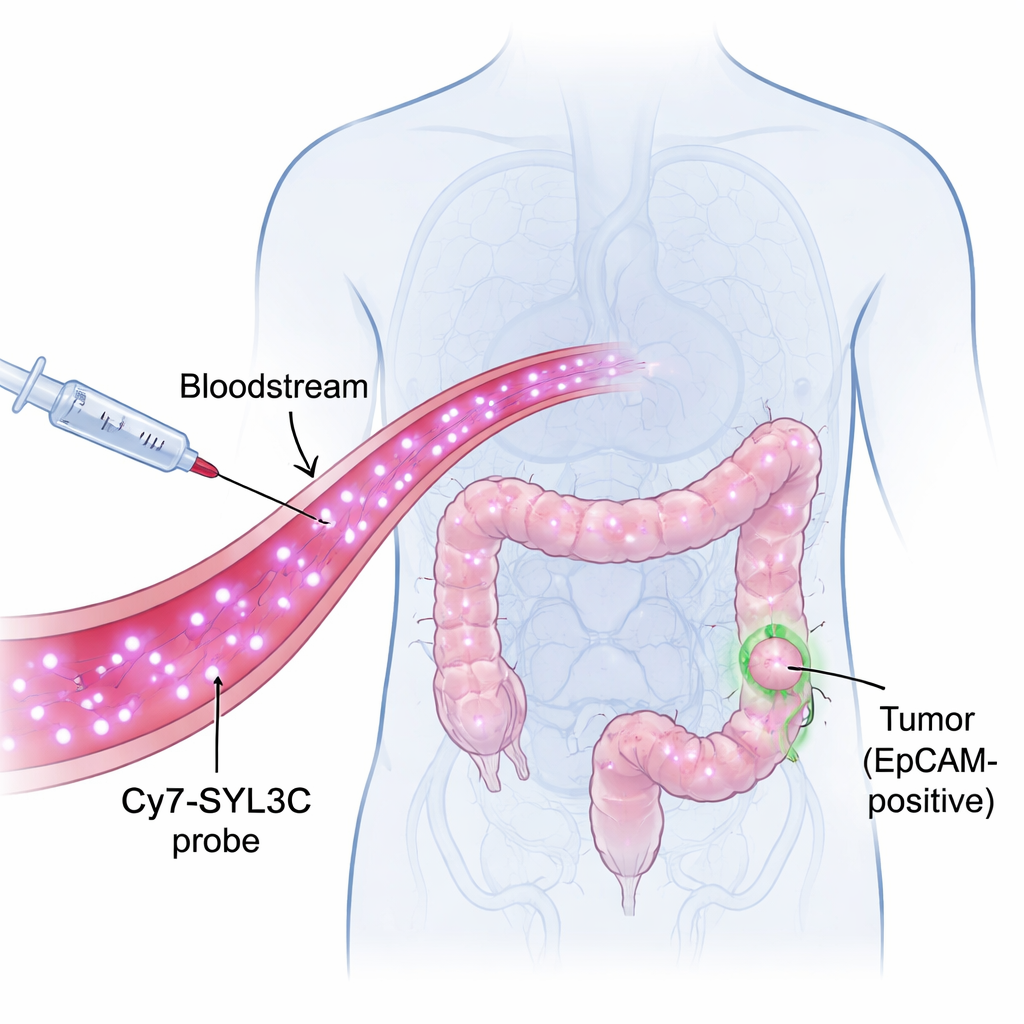
Une étiquette lumineuse qui reconnaît les cellules tumorales
Les chercheurs se sont concentrés sur une molécule appelée EpCAM, présente à la surface de nombreuses cellules de cancer colorectal mais rare dans les tissus sains. Ils ont construit une sonde nommée Cy7-SYL3C en fixant un colorant proche infrarouge (Cy7) à un court brin d’ADN appelé aptamère (SYL3C) qui peut reconnaître EpCAM comme une clé dans une serrure. La lumière proche infrarouge est invisible à l’œil mais peut pénétrer plusieurs millimètres dans les tissus, permettant aux caméras de capter des signaux depuis l’intérieur du corps avec un fort contraste. L’idée est simple : injecter Cy7-SYL3C dans la circulation sanguine, laisser la sonde cibler les cellules tumorales riches en EpCAM, puis utiliser une caméra spéciale pour faire apparaître ces cellules en luminosité sur un fond plus sombre.
Tester la sécurité et la stabilité en laboratoire
Avant d’essayer la sonde chez des animaux vivants, l’équipe a vérifié si elle était stable et sûre. Ils ont mélangé Cy7-SYL3C avec du sérum sanguin de souris et de bovin et ont constaté que la majeure partie de la sonde restait intacte pendant au moins huit heures, suffisamment longtemps pour l’imagerie durant une procédure médicale. Ils ont ensuite exposé des cellules humaines de cancer colorectal et des cellules normales du côlon à différentes concentrations de sonde. La croissance cellulaire est restée essentiellement inchangée, et lorsque la sonde a été mise en contact avec des globules rouges, elle n’a pas provoqué leur hémolyse. Ces tests suggèrent que Cy7-SYL3C est à la fois chimiquement stable et peu agressive pour les cellules — des exigences clés pour tout agent d’imagerie destiné à un usage clinique.
Où la sonde circule dans le corps
Les scientifiques ont ensuite suivi le trajet de Cy7-SYL3C chez des souris saines à l’aide d’un système d’imagerie pour petits animaux. Peu après l’injection, le signal le plus fort est apparu dans le foie et les reins, organes qui filtrent et éliminent les substances du sang. Le signal hépatique atteignait un pic vers une heure puis diminuait, tandis que les reins sont restés lumineux plus longtemps, indiquant que l’urine est une voie principale d’élimination de la sonde. Après deux jours, seule une petite fraction du signal initial subsistait, et l’examen microscopique des organes majeurs n’a montré aucun dommage tissulaire évident. Cela signifie que la sonde est éliminée assez rapidement et ne semble pas endommager visiblement les organes vitaux dans cette étude à court terme.
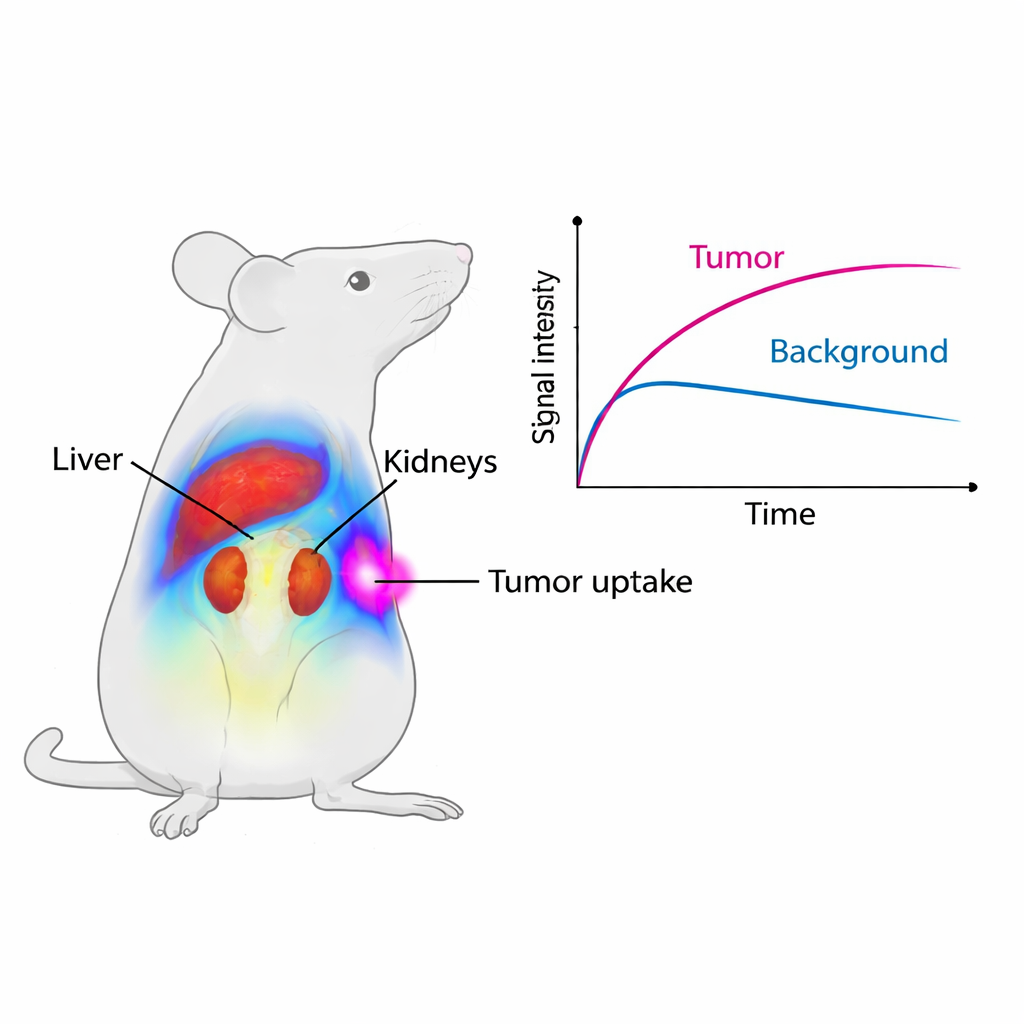
Se concentrer sur les tumeurs colorectales
Pour vérifier que Cy7-SYL3C cible réellement le cancer, l’équipe a utilisé des souris implantées de tumeurs humaines colorectales exprimant EpCAM. Dès cinq minutes après l’injection, les tumeurs ont commencé à briller sur le système d’imagerie. Au cours des quatre premières heures, le signal moyen dans les tumeurs était presque deux fois plus fort que chez des souris dont les tumeurs avaient été « pré-bloquées » par un excès d’aptamère SYL3C non marqué, qui occupait temporairement les sites EpCAM et empêchait la sonde fluorescente de se fixer. Le rapport signal de la tumeur sur le muscle adjacent est passé au-dessus de un et a atteint un pic vers huit heures, indiquant que les tumeurs étaient nettement plus lumineuses que leur environnement pendant une fenêtre d’imagerie utile. Des études microscopiques détaillées ont confirmé que la sonde fluorescente co-localisait avec la coloration d’EpCAM sur les cellules tumorales, tandis que les organes normaux montraient peu ou pas d’expression d’EpCAM.
Comment cela pourrait guider la chirurgie et le diagnostic futurs
Pour un non-spécialiste, le message principal est que Cy7-SYL3C se comporte comme une encre intelligente qui cherche les cellules du cancer colorectal puis est majoritairement éliminée par les reins. Elle semble stable, peu agressive pour les cellules et capable de faire briller les tumeurs rapidement et pendant plusieurs heures, ce qui pourrait aider les chirurgiens à voir les bords tumoraux plus clairement en temps réel ou aider les radiologues à repérer des zones suspectes lors de procédures peu invasives. Bien que ces résultats proviennent d’expériences préliminaires chez la souris et qu’il reste du travail avant une utilisation chez l’humain, l’étude pose des bases importantes pour une nouvelle classe de traceurs optiques susceptibles de rendre la détection et la chirurgie du cancer colorectal plus précises et moins invasives.
Citation: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
Mots-clés: imagerie du cancer colorectal, fluorescence proche infrarouge, ciblage d’EpCAM, sonde à aptamère, guidage chirurgical des tumeurs