Clear Sky Science · fr
Une stratégie multidimensionnelle permet d’accroître de manière évolutive la diversité du métabolome dans les fermentations microbiennes
Pourquoi de petits ajustements d’usine comptent pour de nouveaux médicaments
Beaucoup des médicaments actuels proviennent de composés naturels produits par des bactéries et des champignons. Mais transformer une découverte prometteuse en laboratoire en un véritable candidat-médicament échoue souvent à une étape étonnamment terre-à-terre : cultiver le même microbe dans un autre récipient ou à plus grande échelle. Cette étude pose une question simple mais cruciale : comment conserver la stabilité et la diversité de la production chimique d’un microbe lorsqu’on le transfert des petites boîtes de test à des flacons et des bioréacteurs plus grands ? La réponse pourrait accélérer la recherche de la prochaine génération d’antibiotiques et d’autres thérapies.
Trois manières de cultiver le même microbe
Les chercheurs se sont concentrés sur une bactérie du sol, Streptomyces griseochromogenes, connue pour produire de nombreux « métabolites secondaires » : de petites molécules potentiellement utiles comme médicaments. Ils ont comparé trois systèmes de culture courants utilisés en phase de découverte : flacons à agitation munis de déflecteurs, plaques microtitration « flower » à 48 puits, et un bioréacteur à cuve agitée. Dans chaque système, ils ont mesuré la croissance, la morphologie et la structure cellulaire et, de façon cruciale, le profil des signaux chimiques détectés par spectrométrie de masse, employée ici comme empreinte du métabolome sécrété par la bactérie. Ils ont d’abord appliqué une règle classique d’ingénierie : maintenir la disponibilité en oxygène identique entre systèmes et s’attendre à un comportement similaire. Au lieu de cela, ils ont constaté que les courbes de croissance, les formes cellulaires et les empreintes chimiques différaient fortement d’un récipient à l’autre.
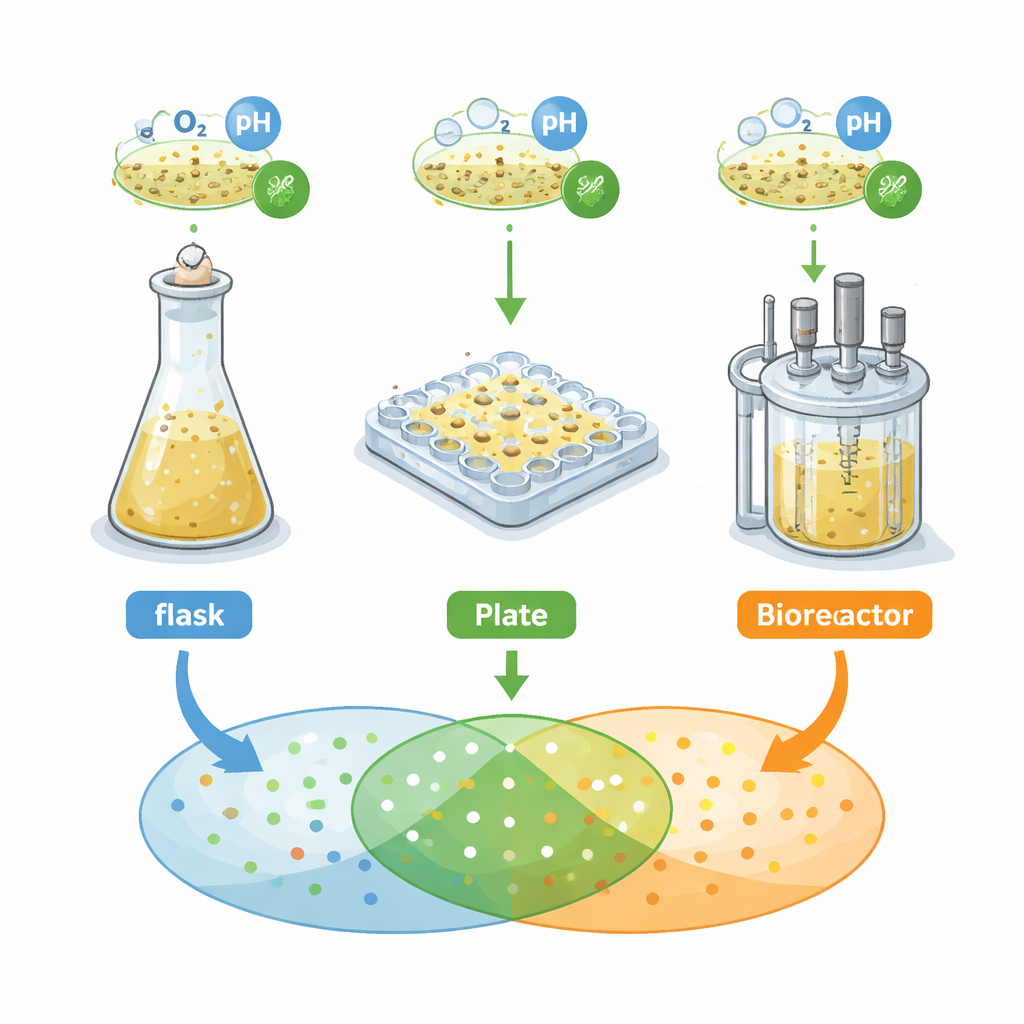
Quand une règle ne suffit pas
Se contenter d’égaliser l’oxygène a produit des « empreintes métaboliques » très différentes : les ensembles de caractéristiques de masse correspondant à des molécules individuelles. Environ seulement 18 % de ces caractéristiques étaient partagées entre les trois systèmes. Les plaques microtitration ont généré beaucoup plus de signaux distincts que les flacons ou le bioréacteur. L’équipe a ensuite testé une autre approche mono‑facteur, en modifiant soit la quantité d’éthanol dans le milieu (une petite molécule susceptible d’inciter les bactéries à produire plus de métabolites), soit la vitesse d’agitation, qui modifie l’apport en oxygène à la culture. Ces ajustements unidimensionnels ont amélioré modestement le recoupement des empreintes chimiques, mais seulement d’environ 18 % supplémentaires. Autrement dit, des recettes simples comme « ajouter plus d’oxygène » ou « ajouter plus d’éthanol » ne garantissent pas qu’un métabolite observé dans un minuscule puits apparaîtra de façon fiable dans un fermenteur plus grand.
Comment la forme cellulaire oriente la diversité chimique
Pour démêler ce qui importe réellement, les auteurs ont regroupé les données de 80 cultures différentes et utilisé une méthode statistique cherchant des facteurs cachés modelant les résultats. Cette analyse a mis en évidence deux thèmes principaux : le système de culture lui‑même et la morphologie des cellules – si les bactéries croissent en pellets compacts, en tapis mycéliens lâches ou en filaments finement dispersés. Les conditions produisant des morphologies similaires avaient tendance à produire des empreintes métaboliques plus proches et facilitaient la « mise à l’échelle » des molécules des petits systèmes vers la cuve agitée. En sélectionnant délibérément des ensembles de conditions donnant des formes cellulaires comparables dans les trois systèmes, les chercheurs ont augmenté le recoupement des caractéristiques chimiques d’environ 50 % par rapport à l’égalisation classique de l’oxygène seule.
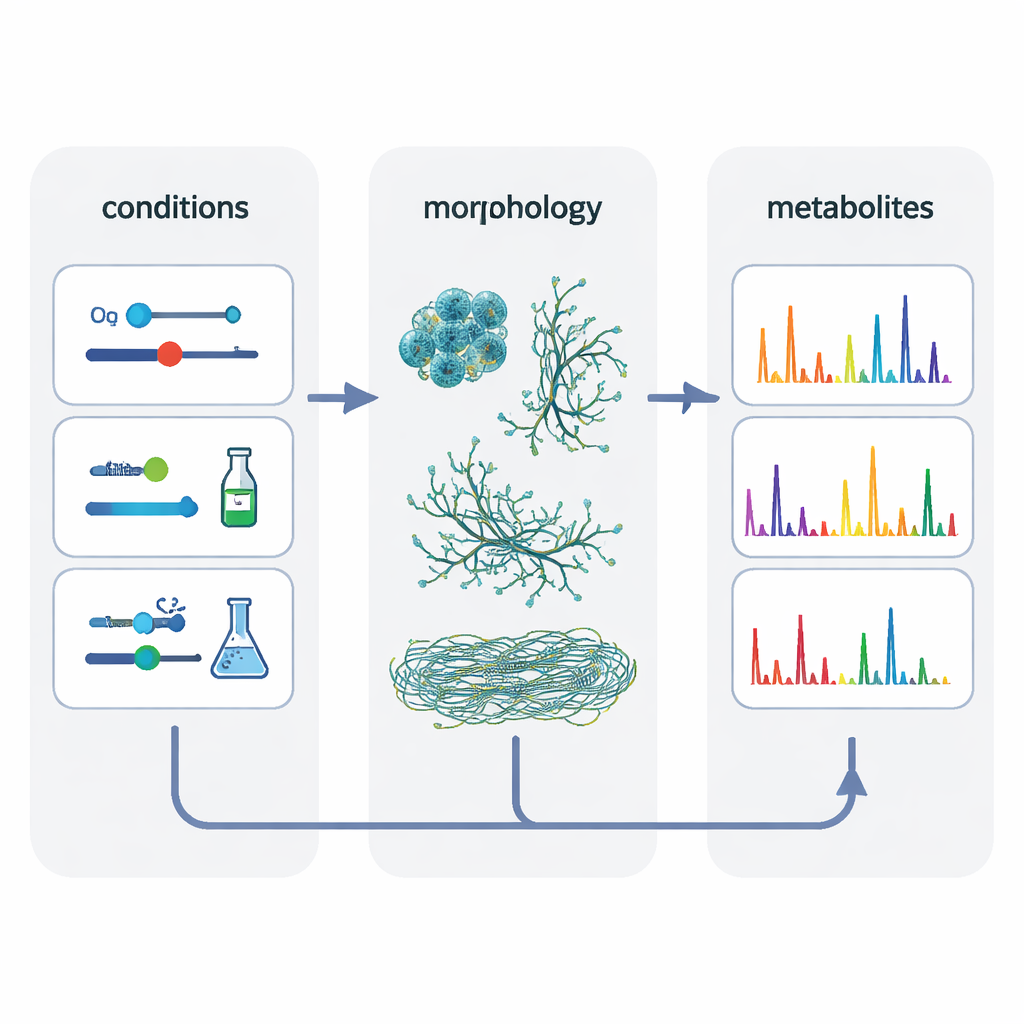
Familles chimiques cachées et molécules spécifiques à un système
Au‑delà du simple décompte des signaux, l’équipe a construit des réseaux moléculaires regroupant des caractéristiques de masse apparentées en familles de métabolites structurellement similaires. Les grandes familles contenaient souvent au moins un membre présent dans chaque système de culture, suggérant une chimie de base robuste aux changements d’échelle. Mais de nombreuses familles plus petites – et certaines molécules individuelles – n’apparaissaient que dans un type de récipient. Les plaques en polystyrène microtitration, en particulier, ont produit la plus grande diversité de composés, y compris de nombreuses variantes de sidérophores chélateurs du fer appelés desferrioxamines et plusieurs peptides non ribosomiques. Les auteurs suggèrent que des stress subtils présents dans ces plaques, tels que des niveaux plus élevés d’espèces réactives de l’oxygène, peuvent pousser les bactéries à diversifier leur chimie, tandis que le bioréacteur bien mélangé favorise un ensemble plus restreint de structures « de base ».
Ce que cela signifie pour la découverte de nouveaux produits naturels
Pour les équipes de découverte de médicaments, le message est clair : on ne peut pas se fier à une seule règle d’ingénierie ou à une condition « optimale » si l’on veut à la fois une riche diversité chimique et une mise à l’échelle fiable. À la place, il faut une stratégie multidimensionnelle qui prenne en compte le type de récipient, le transfert d’oxygène, les additifs comme l’éthanol et, surtout, le suivi en temps réel de la morphologie cellulaire. Utiliser des plaques microtitration qui reproduisent des caractéristiques clés des bioréacteurs et ajuster les conditions pour produire des formes de croissance similaires peut rendre beaucoup plus probable que des molécules prometteuses découvertes à l’échelle microlitre réapparaissent lors de cultures en litres. Cette approche aide à transformer des hits précoces fragiles en candidats robustes et reproductibles, augmentant les chances que de nouveaux produits naturels survivent au passage du banc de laboratoire à l’armoire à pharmacie.
Citation: Lindig, A., Fataeri, M., Hubmann, G. et al. Multidimensional strategy enables scalable metabolome diversity in microbial fermentations. Sci Rep 16, 4084 (2026). https://doi.org/10.1038/s41598-026-37748-9
Mots-clés: découverte de produits naturels, fermentation de Streptomyces, métabolomique, mise à l’échelle en bioréacteur, métabolites secondaires