Clear Sky Science · fr
Ciblage synergique de l’axe ARID2–MYC par le pomalidomide et le panobinostat surmonte la résistance intrinsèque aux IMiD dans le myélome multiple
Pourquoi cette recherche importe pour les patients
Le myélome multiple est un cancer des cellules productrices d’anticorps dans la moelle osseuse : il est devenu plus traitable, mais reste rarement guérissable. Beaucoup de patients finissent par ne plus répondre aux traitements standards, réduisant les options thérapeutiques. Cette étude examine pourquoi la combinaison de deux classes de médicaments existantes — les IMiD comme le pomalidomide et les inhibiteurs de l’histone désacétylase (HDAC) tels que le panobinostat, qui modifient l’organisation de l’ADN — peut agir de concert pour tuer les cellules myélomateuses, même lorsque la tumeur est déjà résistante aux IMiD seuls. Comprendre cette coopération au niveau moléculaire pourrait orienter de meilleures associations thérapeutiques et permettre à davantage de patients de bénéficier de médicaments déjà disponibles.
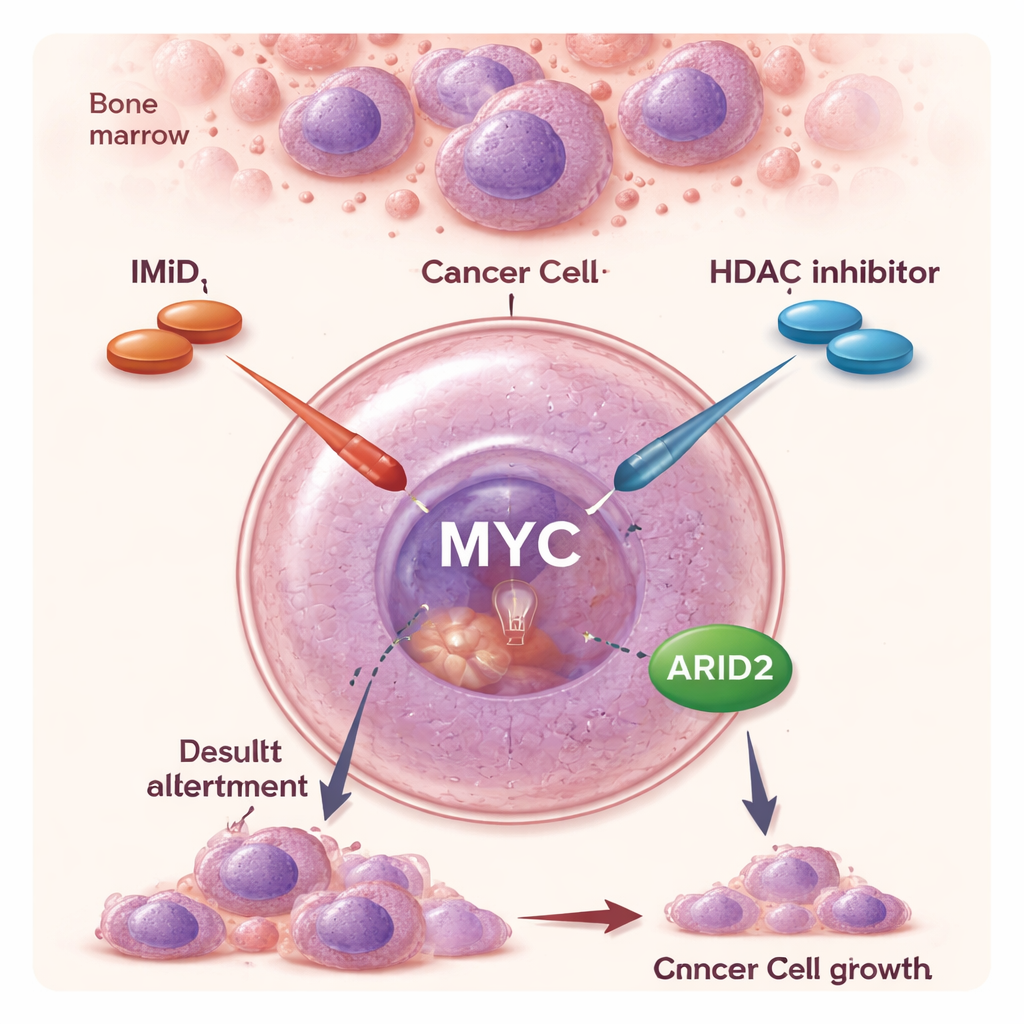
Deux classes de médicaments anciennes, un partenariat nouveau
Au cours des deux dernières décennies, les IMiD et d’autres médicaments ciblés ont considérablement prolongé la survie des personnes atteintes de myélome multiple. Les IMiD agissent de façon inhabituelle : au lieu de simplement bloquer une protéine, ils provoquent le marquage de certaines protéines en vue de leur destruction, les effaçant ainsi de la cellule. Ce mécanisme affaiblit des signaux de survie clés dont dépendent les cellules myélomateuses. Les inhibiteurs de HDAC comme le panobinostat agissent différemment : ils desserrent le compactage de l’ADN et modifient de façon large les gènes exprimés. Pris seuls, les inhibiteurs de HDAC ont des effets modestes et peuvent entraîner des effets indésirables, mais des essais cliniques ont suggéré que les associer aux IMiD produit une réponse anti‑cancéreuse nettement plus forte, y compris chez des patients dont la maladie ne répond plus aux IMiD seuls. La raison moléculaire de cette synergie restait toutefois peu claire.
Un point de pression commun : réduire l’activité de MYC
Les chercheurs ont testé de façon systématique des combinaisons de plusieurs IMiD avec différents inhibiteurs de HDAC sur un panel de lignées cellulaires de myélome, en utilisant un système de score standardisé pour mesurer l’effet synergique par rapport à chaque médicament seul. Ils ont constaté que le pomalidomide associé au panobinostat montrait une synergie particulièrement forte dans la plupart des modèles cellulaires, et que cet effet dépendait d’une protéine appelée céréblon, que les IMiD utilisent pour cibler leurs « victimes » protéiques en vue de leur destruction. En analysant l’activité génétique globale, l’équipe a découvert que le panobinostat et un inhibiteur de HDAC à large spectre apparenté éteignaient fortement MYC, un gène maître de croissance souvent décrit comme un « moteur oncogénique » dans les cellules cancéreuses, et que les IMiD exerçaient une pression supplémentaire sur ce même nœud. Lorsque les scientifiques ont forcé les cellules myélomateuses à continuer de produire MYC à partir d’une source insensible au médicament, l’effet puissant de la paire médicamenteuse a en grande partie disparu, montrant que la répression de MYC est centrale à leur coopération.
Briser la résistance par une voie alternative
Certaines cellules de myélome sont intrinsèquement résistantes aux IMiD : même si les cibles initiales attendues sont détruites, MYC et d’autres signaux de survie ne sont pas correctement éteints, de sorte que les cellules continuent de croître. Dans un de ces modèles résistants, la voie standard reliant les premières cibles aux effets sur MYC était « découplée ». L’équipe a cherché si une voie alternative pouvait encore relier les IMiD à MYC. Ils se sont concentrés sur ARID2, un composant d’une vaste machinerie de remodelage de l’ADN appelée complexe SWI/SNF. Des travaux antérieurs avaient montré que le pomalidomide peut marquer ARID2 pour destruction et que cela contribue à abaisser MYC. Dans les cellules résistantes, le pomalidomide seul réduisait ARID2 de façon limitée, en partie parce que la cellule augmentait sa production d’ARID2 en réponse. L’ajout de panobinostat supprimait le gène ARID2 lui‑même, contrecarrant cette boucle de rétroaction. Ensemble, les deux médicaments réduisaient fortement la protéine ARID2 puis MYC, entraînant une destruction puissante des cellules cancéreuses, même dans des lignées résistantes aux IMiD.
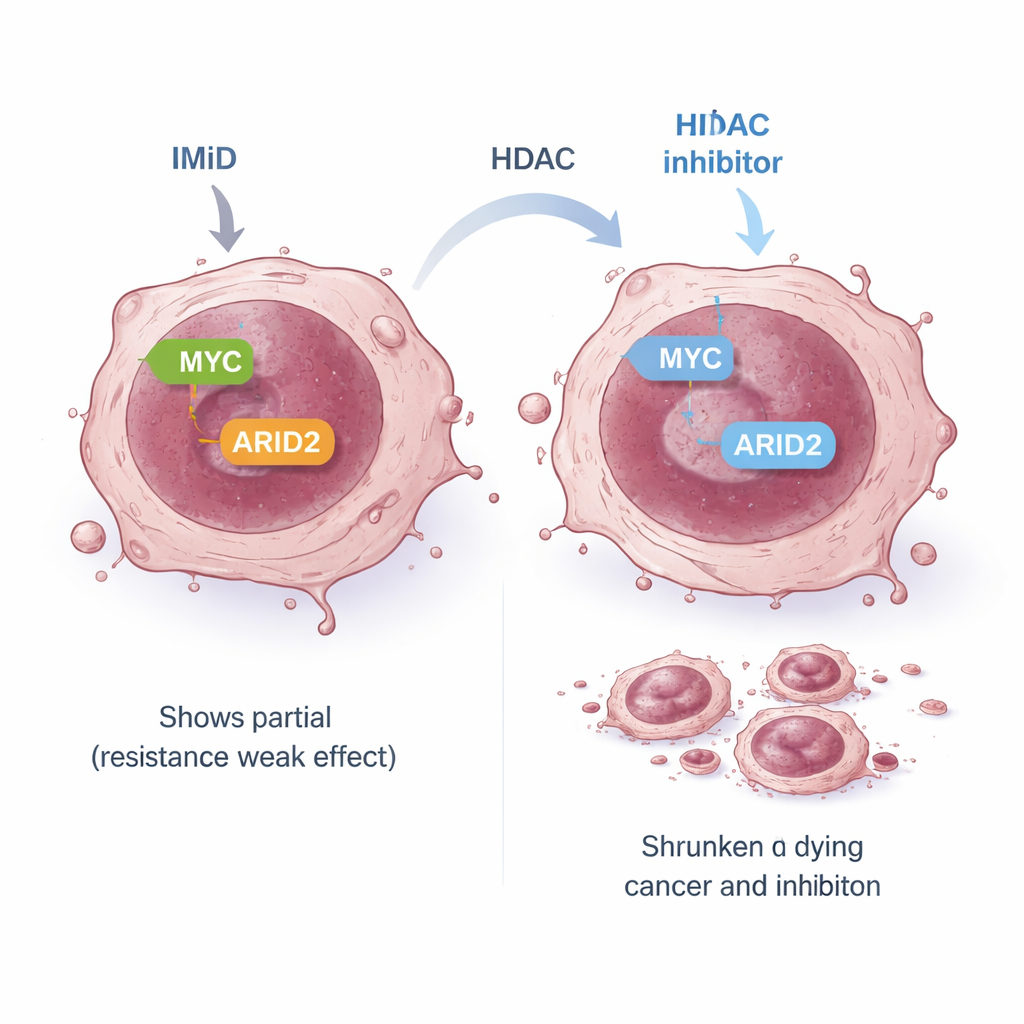
Mettre à nu une faiblesse plus large des cellules cancéreuses
Parce qu’ARID2 n’est qu’un membre du complexe SWI/SNF, les auteurs se sont demandé si l’ensemble du complexe pourrait constituer un point faible thérapeutique. Ils ont constaté que les inhibiteurs de HDAC réduisent les niveaux de plusieurs composants de SWI/SNF, et qu’une autre petite molécule conçue pour bloquer les moteurs centraux du complexe (BRG1/BRM) peut à elle seule ralentir la croissance des cellules de myélome et diminuer MYC. Fait important, cet inhibiteur de SWI/SNF fonctionnait aussi en synergie avec le pomalidomide et le panobinostat, et une combinaison à trois médicaments abaissait encore plus ARID2 et MYC tout en suppriment fortement la prolifération cellulaire. En identifiant quelles HDAC spécifiques étaient impliquées, les chercheurs ont mis en évidence HDAC1 comme acteur clé qui aide à soutenir la voie ARID2–MYC, tandis que d’autres HDAC semblent influencer MYC par des voies parallèles.
Ce que cela signifie pour le traitement futur du myélome
Pour les non‑spécialistes, le message central est que les cellules de myélome semblent dépendre d’un « carrefour de contrôle de la croissance » partagé, centré sur MYC, et qu’il existe plus d’une route menant à ce carrefour. La thérapie IMiD standard frappe principalement une route ; dans certains cancers résistants, cette route est bloquée, et MYC reste actif. Cette étude montre qu’une route alternative — via ARID2 et le complexe SWI/SNF — reste ouverte, et que l’utilisation du panobinostat en association avec le pomalidomide peut la fermer. En combinant délibérément des médicaments qui poussent sur MYC depuis plusieurs directions, les cliniciens pourraient surmonter certaines formes de résistance intrinsèque tout en pouvant utiliser des doses plus faibles de chaque médicament. Bien que des travaux précliniques et cliniques supplémentaires soient nécessaires, ces résultats fournissent un modèle plus clair pour concevoir des associations mécanistes plus intelligentes pour les patients atteints de myélome multiple difficiles à traiter.
Citation: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Mots-clés: myélome multiple, résistance aux médicaments, pomalidomide, panobinostat, MYC