Clear Sky Science · fr
Modifications altérées des histones dans les intestins moyens d’Aedes aegypti après exposition au virus de la fièvre de la Vallée du Rift
Pourquoi les gènes des moustiques comptent pour la santé humaine
La fièvre de la Vallée du Rift est un virus qui rend malades le bétail et les personnes dans certaines régions d’Afrique, et il est transmis par des moustiques. Pour contenir les flambées, les scientifiques doivent comprendre non seulement le virus lui‑même, mais aussi la manière dont les moustiques réagissent lorsqu’ils ingèrent du sang infecté. Cette étude scrute l’intérieur de l’intestin moyen du moustique à un niveau inhabituellement fin, pour savoir comment le virus influe sur l’emballage de l’ADN du moustique afin d’activer ou de réprimer des gènes critiques — des changements qui pourraient déterminer si l’insecte devient un bon ou un mauvais vecteur de la maladie.
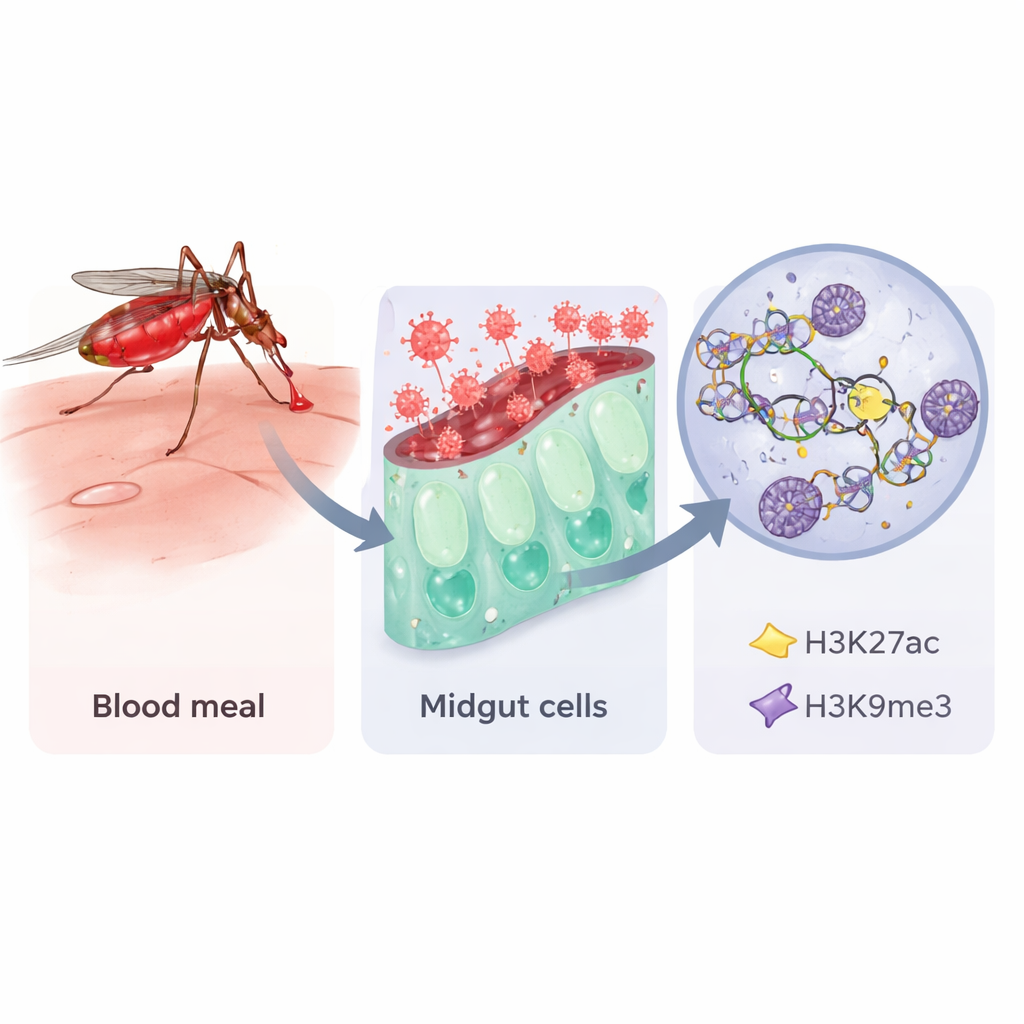
Ouvrir le livre de l’ADN du moustique
Comme chez les humains, les moustiques ne modifient pas les lettres de leur ADN lorsqu’ils rencontrent une infection, mais ils peuvent modifier la façon dont cet ADN est compacté. Les auteurs se sont concentrés sur deux marques chimiques sur les protéines histones, qui servent de bobines pour l’ADN. Une marque, appelée H3K27ac, signale généralement des régions ouvertes et actives de l’ADN ; l’autre, H3K9me3, est associée à des régions éteintes ou silencieuses. En utilisant une méthode sensible connue sous le nom de CUT&RUN, combinée au séquençage de l’ARN, l’équipe a examiné ces marques et l’activité génique dans les intestins moyens d’Aedes aegypti après trois types de repas : du sucre simple, un repas sanguin normal, ou du sang contenant une souche vaccinale du virus de la fièvre de la Vallée du Rift. Ils ont prélevé des intestins un, trois et sept jours après l’alimentation pour saisir les stades précoce, intermédiaire et tardif de l’infection.
Comment un simple repas sanguin reprogramme l’intestin
Un repas sanguin seul, même sans virus, a provoqué des changements importants dans l’activité génique de l’intestin moyen. Des milliers de gènes ont modifié leur activité un jour après l’alimentation, en particulier ceux impliqués dans la digestion des protéines, la gestion de l’énergie et la construction de nouveaux composants cellulaires. Beaucoup de ces gènes se trouvaient à proximité de régions marquées par H3K27ac, ce qui concorde avec l’idée que le sang amène l’intestin à ouvrir des quartiers d’ADN spécifiques nécessaires à la digestion et à la production d’œufs. Au cours des jours suivants, à mesure que le sang était digéré, le profil a évolué : les machines de production d’énergie sont restées actives et, plus tard, des gènes impliqués dans l’organisation des chromosomes et le cycle cellulaire ont été affectés. Les moustiques nourris au sucre, en revanche, ont montré des profils plus stables, suggérant que l’absence de repas sanguin peut conduire à un paysage d’ADN différent, possiblement lié au vieillissement.
Quand le virus rencontre les défenses de l’intestin
L’ajout du virus de la fièvre de la Vallée du Rift au sang a modifié la donne. Au début, un et trois jours après l’alimentation, les intestins moyens des moustiques exposés au virus ont renforcé l’expression de gènes liés à la défense immunitaire et à la signalisation cellulaire, au‑delà des changements induits par le sang seul. Dans le même temps, les relations habituelles entre les marques histones et les gènes voisins se sont compliquées. Le jour trois en particulier, de nombreuses régions marquées par la marque généralement répressive H3K9me3 ont perdu cette marque, et des centaines de gènes proches sont devenus plus actifs, y compris des gènes impliqués dans le contrôle d’autres gènes, la transmission de signaux à l’intérieur de la cellule et la gestion de la forme et de la polarité cellulaires. Au jour sept, quand environ la moitié des moustiques portaient un virus infectieux, l’activité génique globale dans les intestins exposés avait diminué, les gènes liés à l’immunité étaient réduits, et les marques activatrices H3K27ac étaient largement appauvries par rapport aux témoins nourris au sang seulement.
Indices de ruses virales et de défenses moustiques
En associant l’activité génique aux changements histones à proximité, les chercheurs ont identifié un petit ensemble de gènes dont le comportement est particulièrement suggestif. Certains gènes qui aident à organiser les structures membranaires ou à déplacer des matériaux à l’intérieur des cellules ont vu leur activité augmenter alors même que leurs marques activatrices locales diminuaient, ce qui en fait des candidats pour aider le virus à s’assembler ou à circuler dans la cellule. D’autres, tels que des gènes liés à la détoxification de molécules réactives ou à la reconnaissance de pathogènes, ont montré des profils cohérents avec des rôles antiviraux. Un gène remarquable, portant un domaine protéique connu chez des facteurs antiviraux humains, a vu ses ARN augmenter tout en perdant à la fois des marques histones activatrices et répressives, suggérant une forte pression de régulation pendant l’infection. L’étude a aussi mis en évidence une voie de polarité cellulaire, appelée smoothened/hedgehog, dont les composants ont été atténués tard dans l’infection, ce qui s’accorde avec des preuves que de nombreux virus préfèrent les cellules fortement polarisées.
Ce que cela signifie pour le contrôle des maladies transmises par les moustiques
Pour un non‑spécialiste, le message clé est que les cellules de l’intestin du moustique n’acceptent pas passivement l’invasion virale. Elles remodelent rapidement la façon dont leur ADN est empaqueté, d’abord pour alimenter la digestion et la reproduction après un repas sanguin, puis pour monter — ou parfois relâcher — des défenses contre le virus de la fièvre de la Vallée du Rift. Deux marques d’histones, H3K27ac et H3K9me3, évoluent de manière complexe au cours de ce bras de fer, influençant quels gènes peuvent répondre. Bien qu’une fraction seulement des changements géniques puisse être directement liée à ces marques, le travail montre que les marques épigénétiques constituent une couche importante de la réponse du moustique à l’infection. À long terme, comprendre ces bascules pourrait aider les scientifiques à concevoir de nouvelles stratégies pour rendre les moustiques moins aptes à transporter des virus, ajoutant un outil de plus à la lutte contre les maladies émergentes transmises par les moustiques.
Citation: Ogg, H.A., Mikol, Z.M., King, D.C. et al. Altered histone modifications in Aedes aegypti midguts following Rift Valley fever virus exposure. Sci Rep 16, 6605 (2026). https://doi.org/10.1038/s41598-026-37729-y
Mots-clés: Virus de la fièvre de la Vallée du Rift, Aedes aegypti, épigénétique des moustiques, modifications des histones, compétence vectorielle