Clear Sky Science · fr
Mécanisme et divergence évolutive d’une nouvelle hydrolase du polyvinylalcool oxydé chez Stenotrophomonas rhizophila QL-P4
Pourquoi un plastique « vert » courant persiste encore dans la nature
L’alcool polyvinylique, ou PVA, se retrouve partout, des doses de lessive aux revêtements textiles et au papier. Il est souvent présenté comme respectueux de l’environnement parce que, en principe, des microbes peuvent le dégrader. Pourtant, dans les rivières, les sols et les océans, ce matériau plastique se décompose très lentement et peut persister pendant des décennies sous forme de micro- et nanoplastiques. Cette étude examine de près l’un des outils naturels pour s’attaquer au PVA : une enzyme nouvellement découverte chez une bactérie du sol capable de fragmenter ce polymère tenace en morceaux plus petits et plus sûrs.
Un petit aide-soil avec une lourde mission
Des chercheurs ont précédemment isolé une bactérie nommée Stenotrophomonas rhizophila QL-P4 dans un sol de montagne en Chine et constaté qu’elle pouvait croître en utilisant le PVA comme source de carbone. Dans ce travail, ils se sont concentrés sur un seul gène suspect, nommé BAY15_0160, qui semblait pouvoir coder pour une enzyme capable de couper le PVA oxydé. En supprimant soigneusement ce gène, en le réintroduisant et en forçant la bactérie à le surexprimer, ils ont montré que BAY15_0160 est essentiel à une dégradation efficace du PVA. Lorsque le gène était supprimé, le microbe perdait environ 40 % de sa capacité à consommer le PVA ; restaurer le gène rétablissait les performances, confirmant que son produit joue un rôle clé dans la voie de dégradation.
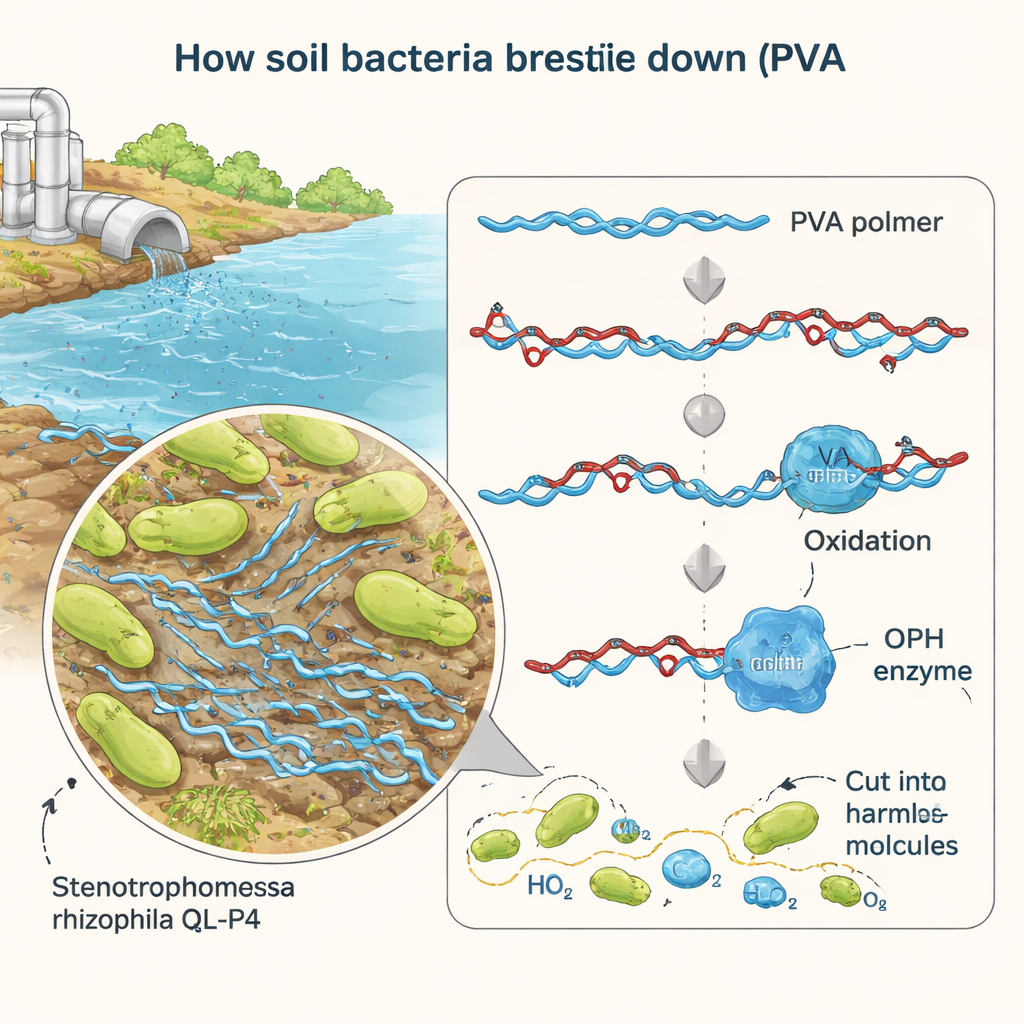
Mesurer comment l’enzyme accomplit son travail
Pour étudier l’enzyme en détail, l’équipe l’a produite en grande quantité en utilisant des souches de laboratoire d’Escherichia coli. Ils ont purifié la protéine, qui s’est révélée d’environ 35 kilodaltons, et testé son activité dans différentes conditions. En utilisant une molécule-test simple qui libère un colorant jaune lorsqu’elle est coupée, ils ont suivi la vitesse d’action de l’enzyme à diverses températures et degrés d’acidité. L’enzyme était la plus active autour de la température ambiante (30 °C) et à un pH neutre semblable à celui de nombreuses eaux naturelles. Dans ces conditions douces, elle présentait une grande efficacité catalytique, ce qui signifie que chaque molécule d’enzyme peut traiter de nombreuses molécules de substrat par seconde — une nouvelle encourageante pour des applications réelles de dépollution.
Zoom sur les ciseaux moléculaires
Les enzymes sont de petites machines naturelles dont la forme détermine la fonction. Les chercheurs ont utilisé des programmes de prédiction de pointe, RoseTTAFold et AlphaFold, pour construire des modèles tridimensionnels de l’enzyme coupant le PVA, désormais reconnue comme une nouvelle hydrolase du PVA oxydé, ou OPH. Les deux outils ont convergé vers l’idée que l’enzyme présente le repli classique « alpha/bêta hydrolase » retrouvé dans de nombreuses « ciseaux » biologiques. Au cœur se trouve un motif court — souvent noté Gly–X–Ser–X–Gly — qui aide à positionner un trio d’acides aminés (sérine, aspartate et histidine) pour attaquer les liaisons chimiques. Des simulations informatiques ont montré des fragments de PVA oxydé nichant dans cette gouttière, la sérine-clé réalisant probablement la première coupure de la chaîne.
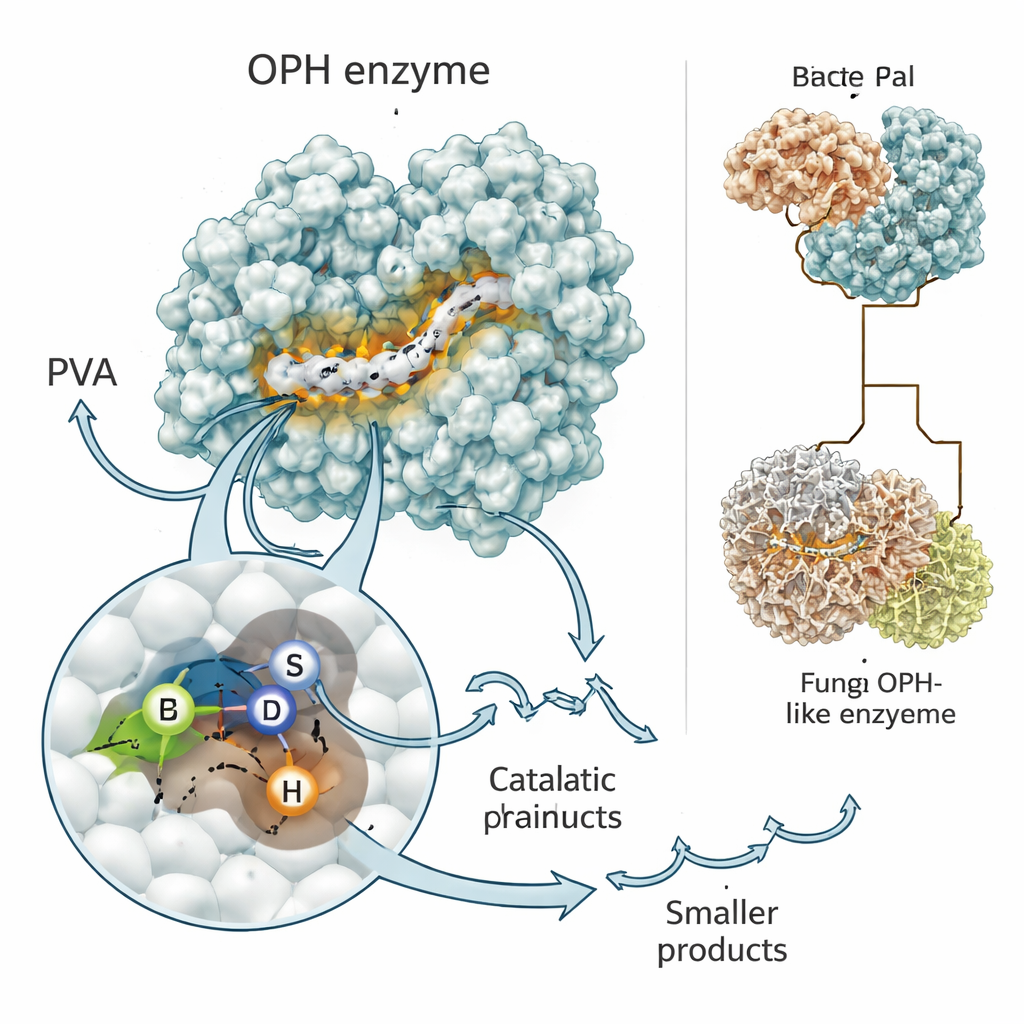
Signaux, interrupteurs et détours évolutifs
L’équipe a également exploré quelles parties de l’enzyme sont absolument nécessaires à son fonctionnement dans la bactérie. Une région proche de l’extrémité N-terminale agit comme un code postal, dirigeant l’enzyme à l’extérieur de la cellule où se trouve effectivement le polymère PVA. Une autre région contient le motif actif qui saisit et clive les liaisons carbone–carbone du plastique. Lorsque les scientifiques ont construit des versions du gène dépourvues soit du segment signal, soit du motif du site actif, la bactérie produisait toujours l’ARN du gène mais n’était plus capable de digérer efficacement le PVA. En comparant de nombreuses bactéries et champignons, ils ont trouvé des homologues de cette enzyme partageant la même région « coupante » centrale mais différant par des modules additionnels, y compris une version fongique remarquable qui fusionne le domaine de coupe à un transporteur intégré, suggérant une stratégie d’« importer‑et‑digérer » encore plus efficace dans des environnements extrêmes comme les rochers antarctiques.
Ce que cela signifie pour le nettoyage de la pollution plastique
Pour les non-spécialistes, le message principal est que les scientifiques apprennent comment certains microbes mâchent naturellement un plastique supposé biodégradable qui, autrement, persiste beaucoup trop longtemps. Cette étude identifie une seule enzyme, OPH de S. rhizophila QL-P4, comme une puissante paire de ciseaux moléculaires qui fonctionne dans des conditions douces et cible une étape cruciale de la dégradation du PVA. En comprenant sa structure, ses conditions de fonctionnement et ses cousins évolutifs, les chercheurs peuvent commencer à concevoir de meilleures souches microbiennes ou des mélanges d’enzymes adaptés aux stations d’épuration, aux effluents industriels ou aux sols contaminés. À long terme, de telles connaissances nous rapprochent de solutions pratiques basées sur la biologie pour gérer les déchets plastiques plutôt que de les laisser s’accumuler dans l’environnement.
Citation: Zhou, Y., Bold, N., Feng, J. et al. Mechanism and evolutionary divergence of a novel oxidized polyvinyl alcohol hydrolase in Stenotrophomonas rhizophila QL-P4. Sci Rep 16, 6411 (2026). https://doi.org/10.1038/s41598-026-37715-4
Mots-clés: alcool polyvinylique, biodégradation, pollution plastique, enzymes microbiennes, bioremédiation