Clear Sky Science · fr
Explorer l’impact du composé innovant 3-(3-(4-hydroxy-2-oxo-2H-chromen-3-yl)-5-(pyridin-3-yl)-1H-pyrazol-1-yl) indolin-2-one sur l’accélération de la cicatrisation
Pourquoi une cicatrisation plus rapide compte
Presque tout le monde a vécu une coupure qui a mis plus de temps à guérir que prévu, ou a entendu des histoires inquiétantes de plaies qui se sont infectées et ont refusé de se refermer. Alors que la résistance aux antibiotiques augmente, les médecins cherchent des pansements plus intelligents qui non seulement protègent la peau endommagée mais l’aident aussi à se reconstruire. Cette étude présente un nouveau composé synthétique, inspiré de molécules végétales, qui vise à faire les deux : éliminer les germes nuisibles et accélérer le processus de réparation propre au corps.
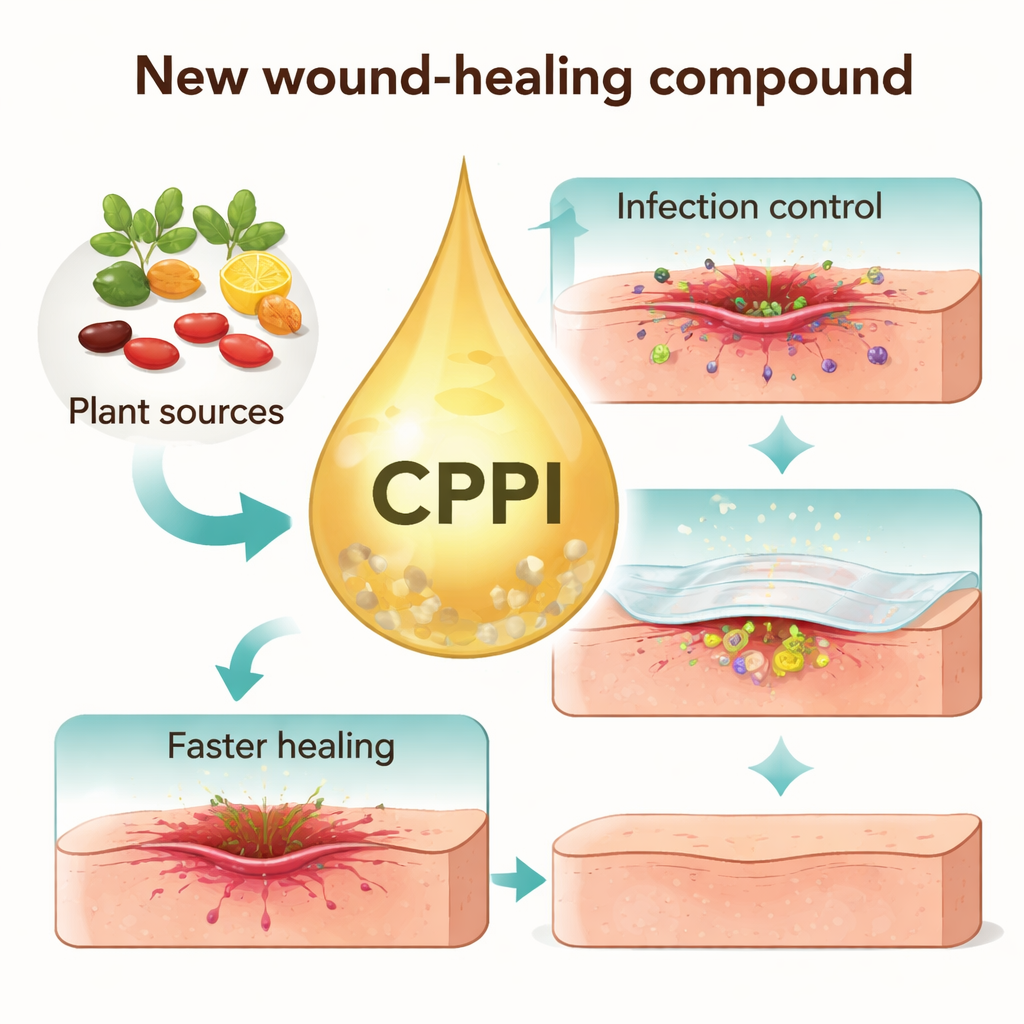
Un nouvel auxiliaire bâti à partir d’éléments d’inspiration végétale
Les chercheurs se sont concentrés sur la coumarine, une substance naturelle présente dans des plantes comme les haricots et certains fruits, connue depuis longtemps pour son potentiel antibactérien et cicatrisant. Ils ont conçu une molécule plus complexe nommée CPPI en combinant la coumarine avec trois autres blocs cycliques fréquemment utilisés en pharmacologie moderne. Ces parties supplémentaires ont été choisies parce qu’elles interagissent bien avec des enzymes bactériennes et influencent l’inflammation ainsi que la croissance tissulaire. Après avoir synthétisé soigneusement le CPPI en plusieurs étapes chimiques, l’équipe a utilisé des techniques de laboratoire standard pour confirmer qu’elle avait bien obtenu la structure prévue.
Combattre les germes dangereux
Les plaies ouvertes offrent des points d’entrée idéaux aux agents pathogènes, en particulier aux souches bactériennes qui ne répondent plus à de nombreux antibiotiques. Les scientifiques ont testé le CPPI contre plusieurs espèces problématiques, dont Staphylococcus aureus résistant à la méthicilline (SARM), Bacillus cereus et Pseudomonas aeruginosa résistante aux carbapénèmes. En éprouvettes, le CPPI a empêché la croissance de ces bactéries à des doses plus faibles que plusieurs antibiotiques couramment utilisés, bien qu’il soit moins puissant que le très fort ciprofloxacine. Il a montré peu d’effet sur des champignons comme Candida et Aspergillus, ce qui suggère que sa force réside principalement dans l’activité bactéricide plutôt que comme agent antifongique large spectre.
Aider les cellules cutanées à refermer la plaie
Arrêter l’infection n’est que la moitié du travail ; la peau doit aussi se reconstruire. Pour vérifier si le CPPI pouvait soutenir ce processus, l’équipe a utilisé un test de « grattage » avec des fibroblastes cutanés humains. Ils ont cultivé une couche plate de cellules, tracé une étroite entaille au milieu, et observé la rapidité avec laquelle les cellules se déplacent pour combler l’écart. Au bout de 24 heures, les boîtes traitées au CPPI avaient fermé environ 91 % de l’écart, contre environ 71 % dans les boîtes non traitées. Ce résultat indique que le CPPI favorise les mouvements cellulaires essentiels à la soudure des plaies réelles.
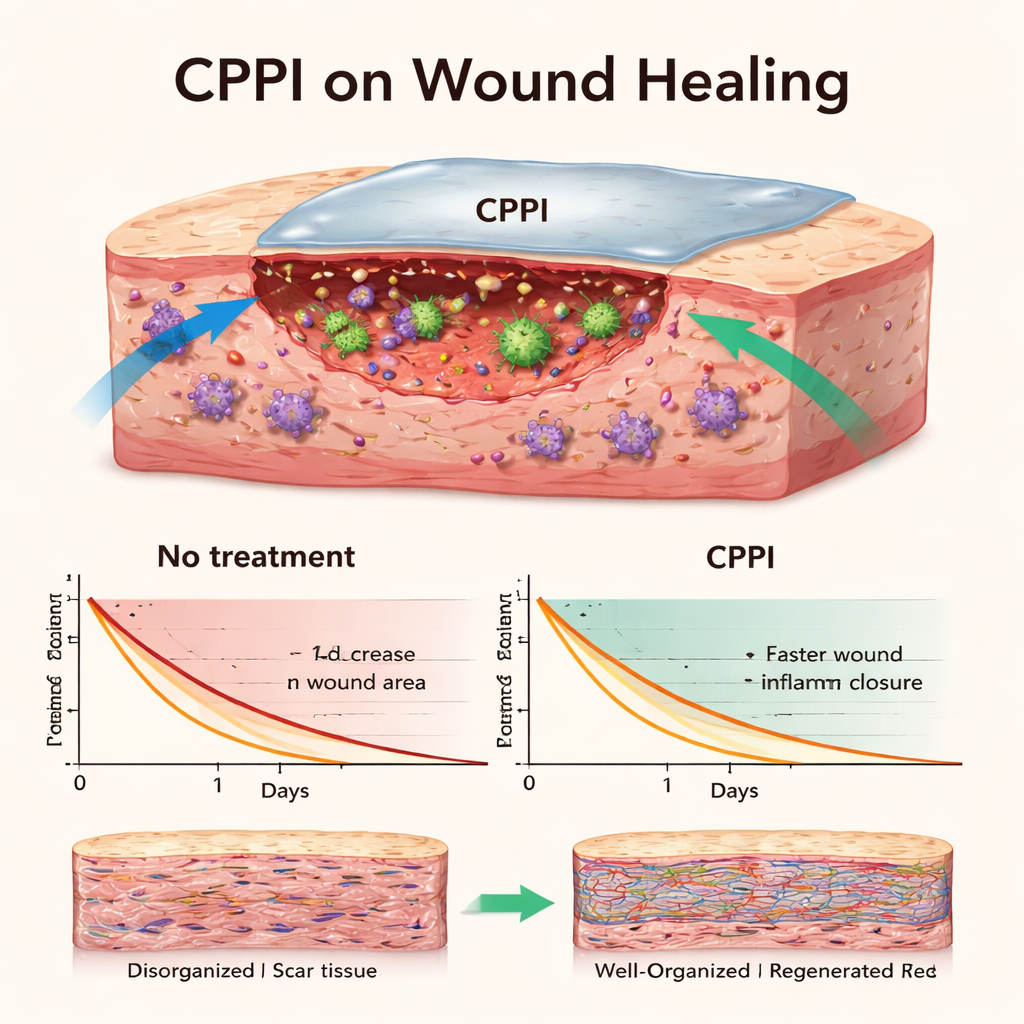
Accélérer la cicatrisation dans la peau vivante
Le test le plus parlant provient d’expériences sur des rats. Les chercheurs ont créé de petites plaies circulaires sur le dos des animaux, puis ont laissé un groupe non traité et appliqué le CPPI au groupe traité à plusieurs reprises sur deux semaines. Les photographies ont montré qu’au jour 14 les plaies non traitées restaient visiblement ouvertes, tandis que les plaies traitées au CPPI étaient presque entièrement refermées, avec environ 97 % de réduction de surface. Au microscope, la peau non traitée présentait des cicatrices importantes, une inflammation persistante et une mauvaise régénération de l’épiderme. En revanche, la peau traitée au CPPI présentait une nouvelle surface continue, des couches de tissu régénéré plus épaisses et de forts signaux du facteur de croissance endothélial vasculaire — une molécule associée à la formation de nouveaux vaisseaux sanguins qui nourrissent le tissu en cours de réparation.
Un coup d’œil sous le capot moléculaire
Pour comprendre pourquoi le CPPI pourrait être si efficace, l’équipe s’est tournée vers des simulations informatiques. Ils ont modélisé la façon dont le composé se loge dans des protéines impliquées dans l’inflammation et la réparation tissulaire, en particulier des membres de la famille des MAP kinases, qui contrôlent la croissance cellulaire et les réponses au stress. Les études de docking virtuel ont suggéré que le CPPI se lie de façon serrée et stable à l’une de ces protéines, MAPK1, formant plusieurs contacts chimiques susceptibles d’altérer son activité. Des simulations longues à l’échelle des nanosecondes ont indiqué que le complexe protéine‑composé reste stable sans perturber la structure globale de la protéine, ce qui appuie l’idée que le CPPI pourrait ajuster finement des voies de signalisation favorisant une cicatrisation ordonnée.
Ce que cela pourrait signifier pour les pansements de demain
Pris ensemble, les résultats suggèrent que le CPPI pourrait former la base de pansements de nouvelle génération qui protègent les blessures des bactéries dangereuses tout en encourageant activement la peau à se réparer plus vite et plus proprement. Bien que ces découvertes en soient encore au stade expérimental et loin d’une utilisation clinique chez l’homme, elles ouvrent la voie à une stratégie prometteuse : concevoir des molécules multifonctions, inspirées de produits naturels, qui combinent une puissance antimicrobienne et un soutien direct aux mécanismes de réparation du corps.
Citation: Sabt, A., Abdelmegeed, H., Abdel-Razik, AR.H. et al. Exploring the impact of the innovative compound 3-(3-(4-hydroxy-2-oxo-2H-chromen-3-yl)-5-(pyridin-3-yl)-1H-pyrazol-1-yl) indolin-2-one on accelerating wound recovery. Sci Rep 16, 7489 (2026). https://doi.org/10.1038/s41598-026-37714-5
Mots-clés: cicatrisation, antibactérien, coumarine, régénération cutanée, conception de médicaments