Clear Sky Science · fr
Classification des gliomes selon le métabolisme des lipides
Pourquoi les graisses importent dans les tumeurs cérébrales
Les tumeurs cérébrales appelées gliomes font partie des cancers les plus dangereux, pourtant des patients ayant apparemment le même diagnostic peuvent avoir des évolutions très différentes. Cette étude pose une question apparemment simple mais aux grandes implications : de quelles façons l’utilisation des graisses — les lipides de l’organisme — influe-t-elle sur l’agressivité des tumeurs, leur réponse aux traitements et sur notre capacité à détecter ces différences sur des examens cérébraux standards ? En suivant l’usage des lipides dans des centaines de tumeurs, les auteurs révèlent des sous-types cachés de gliome qui pourraient modifier la manière dont les médecins prédisent le pronostic et conçoivent des thérapies.
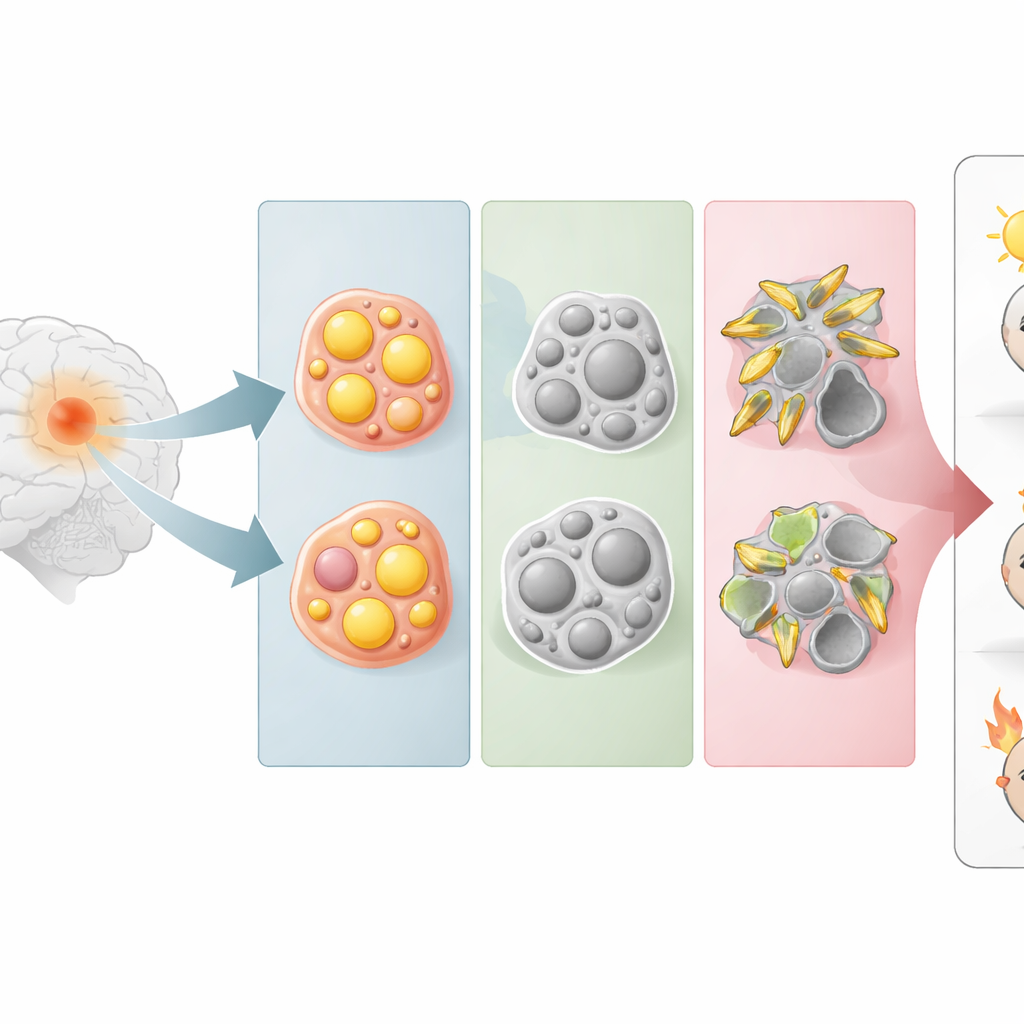
Trois visages cachés d’une même tumeur cérébrale
Plutôt que de partir de l’apparence des cellules tumorales au microscope, les chercheurs ont groupé les gliomes selon l’intensité d’activation de cinq grandes voies lipidiques, incluant celles qui traitent les lipides stéroïdes, les triglycérides et les sphingolipides (composants essentiels des membranes cellulaires). À partir des profils d’activité génique de larges bases de données publiques sur les tumeurs, ils ont constaté que les gliomes se répartissaient naturellement en trois groupes. Un groupe reposait fortement sur le métabolisme des stéroïdes (type ST), un autre sur celui des triglycérides (type TC) et un troisième sur le métabolisme des sphingolipides (type SP). Ces regroupements métaboliques traversent les catégories tumorales classiques, révélant que des cellules ayant des habitudes lipidiques similaires peuvent se trouver dans des gliomes d’aspect différent.
Du métabolisme au pronostic des patients
L’équipe a ensuite examiné comment ces trois styles d’utilisation des lipides se rapportent aux résultats cliniques. Les patients dont les tumeurs appartenaient au groupe ST avaient en général la survie la plus longue, et leurs tumeurs étaient plus souvent de bas grade et portaient des altérations génétiques connues comme favorables. À l’autre extrémité, les tumeurs de type SP étaient généralement des glioblastomes de haut grade, sans mutations protectrices et survenant plus fréquemment chez des patients âgés. Même après ajustement statistique sur le grade tumoral et les marqueurs génétiques clés, l’appartenance au type SP restait associée à un pronostic nettement plus mauvais, ce qui suggère que la façon dont la tumeur gère les sphingolipides capture une dimension de danger indépendante que les tests standards manquent.
Un voisinage hostile à l’intérieur du cerveau
En creusant, les auteurs ont étudié le microenvironnement tumoral — le mélange de cellules immunitaires, de vaisseaux sanguins et de tissus de soutien autour du cancer. Les tumeurs de type SP présentaient un paysage immunitaire encombré et conflictuel, avec à la fois des cellules immunitaires orientées vers l’attaque et des cellules suppressives, ainsi que des signaux puissants qui atténuent les réponses anti-tumorales efficaces. Les voies liées à une croissance cellulaire rapide, à l’invasion, à la néovascularisation, à la cicatrisation et à l’inflammation étaient toutes plus actives dans ce sous-type. Des estimations de la sensibilité des tumeurs à la radiothérapie suggéraient que les gliomes de type SP sont les plus résistants à la radiothérapie, ce qui concorde avec leur survie plus mauvaise. En revanche, les tumeurs de type ST semblaient plus « calmes », avec des niveaux plus faibles de ces caractéristiques agressives.
Lire le métabolisme tumoral à partir d’IRM
Parce que retirer chirurgicalement un échantillon tumoral est invasif et n’est pas toujours possible, les chercheurs ont exploré si l’imagerie par résonance magnétique (IRM) standard pouvait suggérer le comportement lipidique d’une tumeur. Ils ont extrait plus de deux mille caractéristiques subtiles de texture et de forme à partir de deux séquences d’IRM courantes et ont entraîné un modèle d’apprentissage automatique pour distinguer le type SP des autres tumeurs. Le modèle a bien performé à la fois sur un jeu d’entraînement hospitalier et sur un jeu de validation public indépendant, séparant correctement les tumeurs de type SP bien plus souvent que le hasard. Cela suggère que l’empreinte métabolique d’un sous-type de gliome particulièrement agressif laisse une marque détectable sur des examens cérébraux de routine.
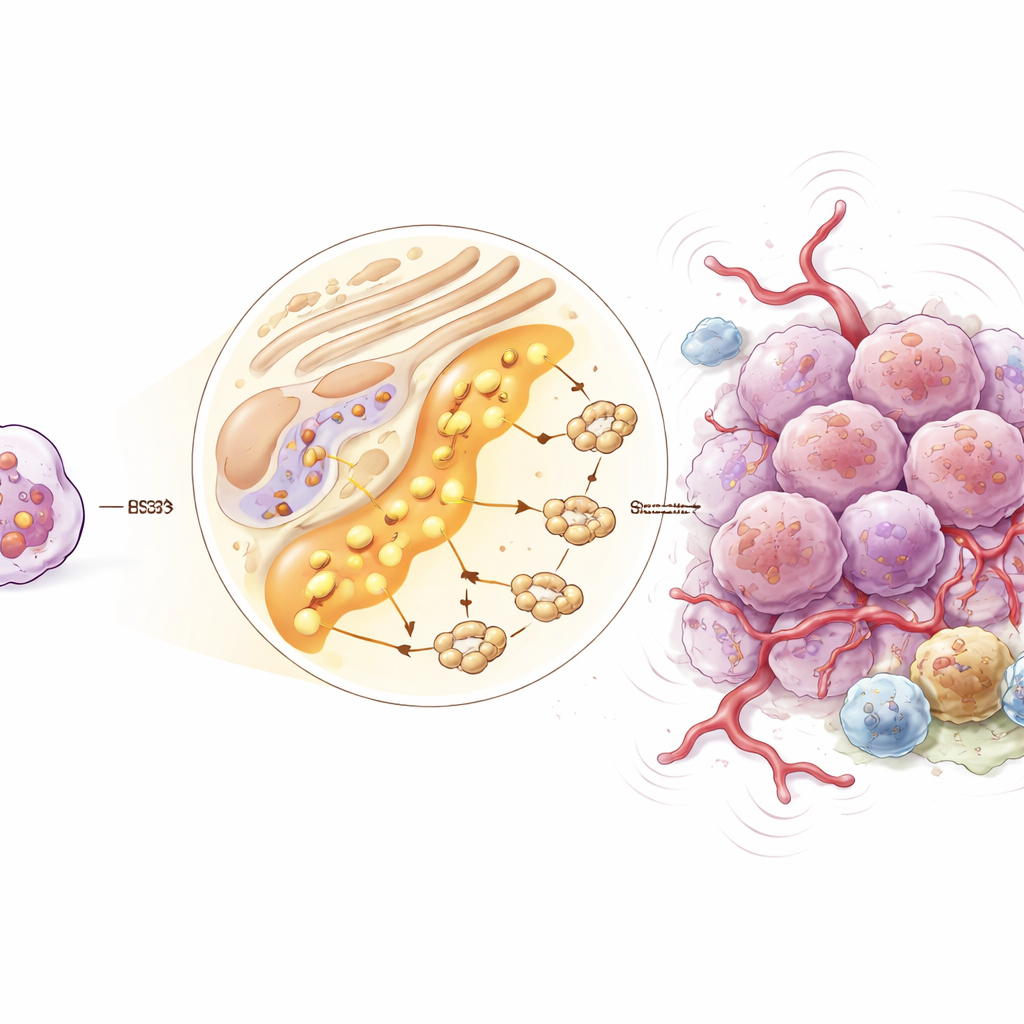
Un gène clé au centre d’un réseau agressif
Pour passer des voies générales à des cibles concrètes, l’équipe a recherché des gènes centraux dans les réseaux liés aux lipides, fortement surexprimés dans les tumeurs de type SP, associés à une survie plus mauvaise et précis pour distinguer les tumeurs SP des autres. Trois gènes — GLA, GLB1 et HSD3B7 — ont satisfait à tous ces critères. Ils étaient tous plus actifs dans les gliomes de type SP et formaient ensemble une signature diagnostique puissante. Les auteurs se sont concentrés sur HSD3B7, dont le rôle dans les tumeurs cérébrales avait été en grande partie inexploré. Des colorations tissulaires réalisées sur 100 patients atteints de gliome ont montré que la protéine HSD3B7 était plus élevée dans les tumeurs les plus avancées et les plus malignes, et les patients dont les tumeurs présentaient des niveaux élevés de cette protéine avaient une survie significativement plus courte.
Comment un gène lipidique réorganise l’écosystème tumoral
Des analyses en cellule unique, qui profilent des cellules individuelles au sein des tumeurs, ont révélé que HSD3B7 est actif non seulement dans les cellules cancéreuses mais aussi dans plusieurs types de cellules immunitaires et de soutien. Des niveaux élevés de ce gène étaient associés à un réseau de signaux favorisant la croissance vasculaire, l’inflammation chronique et l’échappement immunitaire. La communication entre certains types cellulaires protecteurs semblait affaiblie, tandis que des boucles auto-renforçantes au sein des cellules qui soutiennent la tumeur étaient renforcées. Ensemble, ces schémas suggèrent qu’une activité accrue de HSD3B7 contribue à créer et maintenir un microenvironnement hostile qui favorise la croissance tumorale et la résistance aux thérapies.
Ce que cela signifie pour les patients et les soins futurs
Sur le plan pratique, ce travail montre que les gliomes peuvent être utilement divisés en trois sous-types basés sur le métabolisme des lipides, le type SP riche en sphingolipides se distinguant comme particulièrement dangereux et résistant aux thérapies. Ces différences ne sont pas que théoriques : elles peuvent être lues sur des IRM de routine grâce à l’analyse d’images avancée et reliées à des gènes spécifiques comme HSD3B7 qui pourraient devenir des cibles médicamenteuses futures. Bien que des travaux expérimentaux supplémentaires soient nécessaires pour tester si bloquer ces voies lipidiques ralentirait les tumeurs ou améliorerait la radiothérapie, l’étude offre une nouvelle lentille métabolique pour envisager le cancer cérébral et rapproche la recherche d’applications plus personnalisées et fondées sur la biologie pour la prise en charge des patients.
Citation: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
Mots-clés: gliome, métabolisme des lipides, imagerie des tumeurs cérébrales, radiomique, microenvironnement tumoral