Clear Sky Science · fr
Un régime riche en graisses remodèle les réseaux régulateurs de gènes dans la zone préoptique
Pourquoi votre cerveau compte dans le diabète
La plupart des gens considèrent le diabète comme un problème du pancréas et du taux de sucre sanguin, mais le cerveau y joue aussi un rôle majeur. Cette étude examine comment un régime riche en graisses et un traitement expérimental puissant modifient l’activité des gènes dans une petite région cérébrale pourtant importante, la zone préoptique. En cartographiant quelles cellules cérébrales « se réinitialisent » lorsque le diabète entre en rémission, les chercheurs espèrent ouvrir la voie à de nouvelles thérapies qui tirent parti de la capacité intrinsèque du cerveau à aider au contrôle de la glycémie.
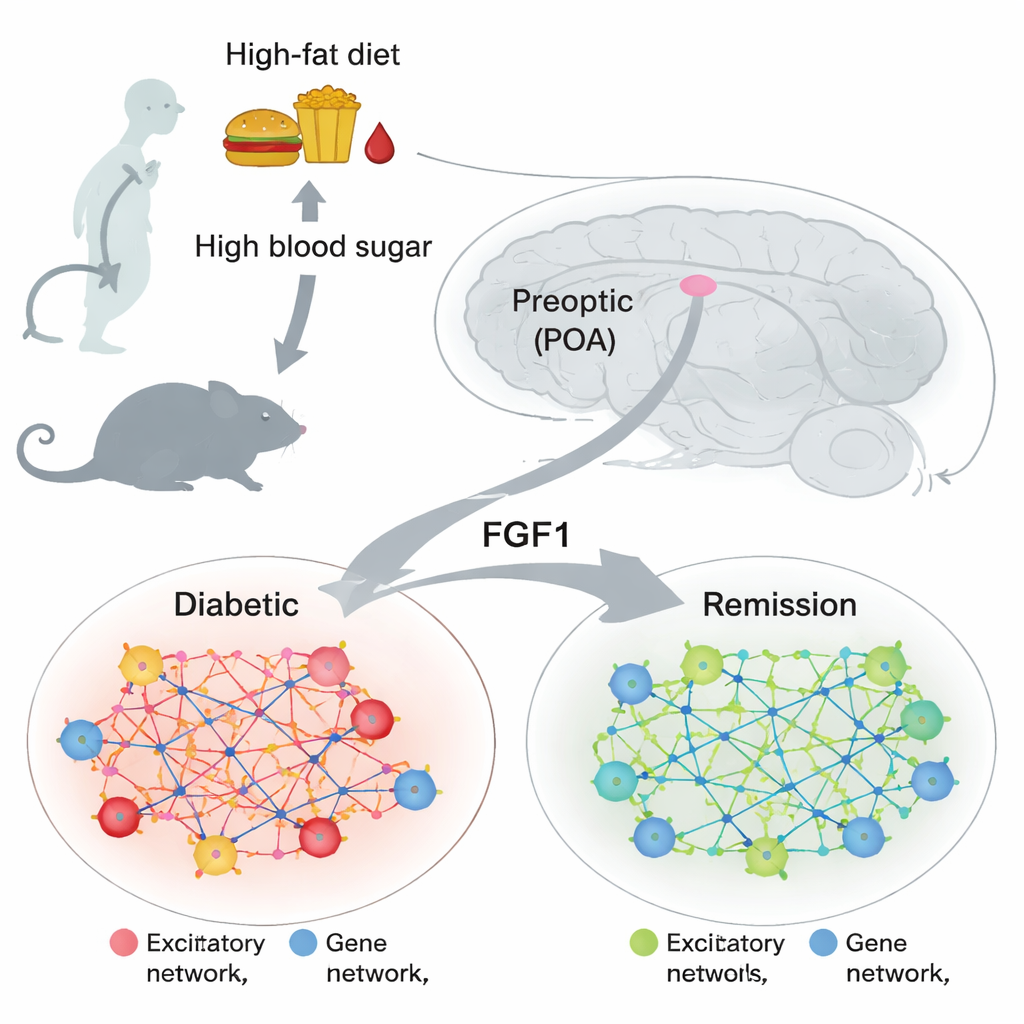
Un petit centre cérébral à grande influence métabolique
La zone préoptique se situe à l’avant de l’hypothalamus, une partie du cerveau qui aide à réguler la température corporelle, le sommeil, l’alimentation et les signaux hormonaux. Des travaux antérieurs ont montré que les cellules de cette région peuvent influencer la gestion du glucose et la réponse à la chaleur, mais leur rôle dans le diabète restait mal compris. Parallèlement, d’autres études ont trouvé qu’une seule injection d’une protéine appelée facteur de croissance des fibroblastes 1 (FGF1), administrée dans le cerveau, peut plonger des souris obèses et diabétiques en rémission prolongée. Cela posait une question clé : quelles cellules cérébrales et quels programmes géniques changent lorsque la glycémie se normalise, et des changements similaires apparaissent-ils dans la zone préoptique ?
Lire l’activité des gènes cellule par cellule
Pour répondre à cela, l’équipe a utilisé le séquençage d’ARN unicellulaire, une technique qui mesure quels gènes sont activés dans des milliers de cellules individuelles simultanément. Ils ont réanalysé un ensemble de données existant provenant de souris dont le diabète était entré en rémission après un traitement par FGF1, en se concentrant sur les neurones de l’hypothalamus. À l’aide d’outils statistiques, ils ont identifié des groupes de gènes qui augmentaient ou diminuaient ensemble lorsque les animaux passaient d’un état diabétique à la rémission. Ces « modules de rémission » agissent comme des empreintes de la récupération : au lieu de suivre un gène à la fois, ils captent des variations coordonnées à travers de nombreux gènes au sein de types neuronaux particuliers.
Régime riche en graisses, cellules cérébrales et réduction de l’usage énergétique
Les chercheurs ont ensuite comparé ces modules de rémission à l’activité génique dans un autre jeu de données qui échantillonnait des cellules de la zone préoptique de souris normales. Ils ont d’abord séparé les neurones en deux grandes classes : les cellules excitatrices, qui tendent à augmenter l’activité dans leurs circuits, et les cellules inhibitrices, qui la réduisent. Chez les souris diabétiques traitées par FGF1, les deux types neuronaux ont montré de larges diminutions des gènes liés à la production d’énergie — en particulier ceux impliqués dans la phosphorylation oxydative, la respiration cellulaire et la machinerie mitochondriale qui alimente les cellules actives. Dans les neurones excitateurs, un important module génique « turquoise » lié à l’usage énergétique et à l’activité synaptique était fortement réprimé en rémission, ce qui suggère que ces cellules deviennent moins exigeantes sur le plan métabolique lorsque la glycémie est maîtrisée.
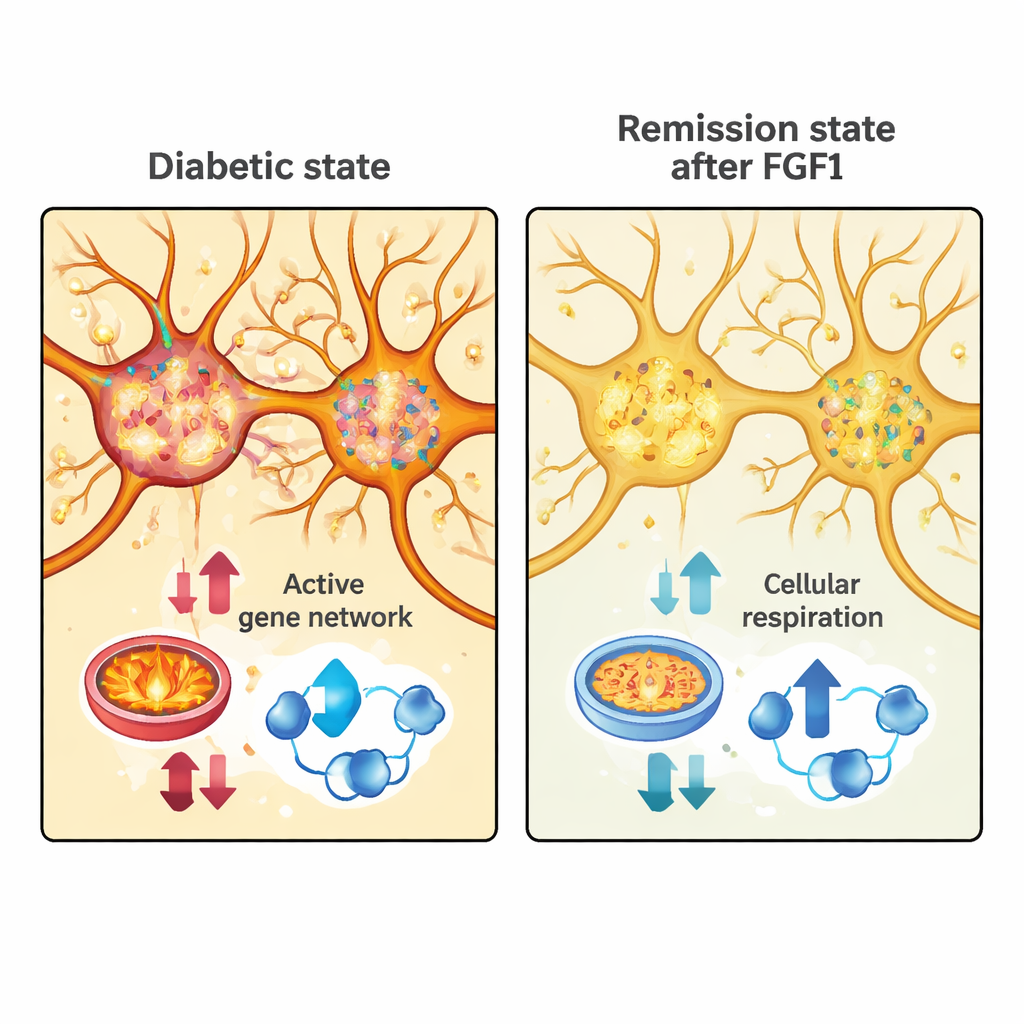
Relier les signatures de rémission à des groupes neuronaux spécifiques
Ensuite, l’équipe a cherché à savoir si ces schémas géniques liés à la rémission correspondaient à des populations cellulaires particulières dans la zone préoptique. En fusionnant informatiquement les deux ensembles de données, ils ont trouvé que certains clusters de neurones préoptiques exprimaient beaucoup des mêmes gènes qui changeaient lors de la rémission induite par le FGF1. Ils ont mis en avant plusieurs gènes — tels que Trpc4, Dgkg et Ryr3 — qui se trouvaient au croisement de ces analyses. En utilisant une méthode de microscopie très sensible appelée RNAscope, ils ont montré que ces gènes sont effectivement exprimés dans des zones distinctes de la zone préoptique de la souris, principalement dans des sous-régions dorsales. Cela les valide comme marqueurs réels de groupes neuronaux spécifiques susceptibles de participer à la réponse cérébrale aux maladies métaboliques.
Ce que cela signifie pour les traitements futurs du diabète
Pour les non-spécialistes, la conclusion est que le diabète n’est pas seulement un problème de glycémie — c’est aussi un problème de réseaux cérébraux. L’étude montre que lorsque le diabète entre en rémission chez la souris, certains neurones préoptiques basculent vers un état de moindre dépense énergétique et modifient de manière coordonnée leur activité génique. En définissant ces modules de rémission et en les reliant à des types cellulaires concrets et à des gènes marqueurs, ce travail fournit une feuille de route pour des expériences futures : les chercheurs peuvent désormais cibler ces neurones spécifiques pour tester comment ils influencent le contrôle du glucose, l’obésité et les complications associées. À long terme, une meilleure compréhension de ces circuits cérébraux pourrait inspirer des traitements qui complètent ou même contournent des organes défaillants en exploitant le contrôle métabolique intrinsèque du cerveau.
Citation: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Mots-clés: cerveau et diabète, zone préoptique, régime riche en graisses, réseaux de gènes, rémission par FGF1