Clear Sky Science · fr
Identification dans le transcriptome complet de variantes délétères dans des gènes candidats liés à la paratuberculose bovine
Gènes cachés derrière une maladie bovine coûteuse
La paratuberculose bovine, également appelée maladie de Johne, affaiblit discrètement la santé et la productivité des troupeaux laitiers dans le monde, coûtant aux éleveurs des centaines de millions de dollars chaque année et suscitant des inquiétudes quant à des liens avec des troubles intestinaux humains. Cette étude soulève le capot génétique des vaches Holstein pour poser une question simple mais cruciale : quelles différences génétiques pourraient aider certains animaux à résister à l’infection alors que d’autres succombent ? En lisant l’ARN — les copies actives des gènes — dans le sang et le tissu intestinal, les chercheurs ont tracé comment de subtils changements d’ADN dans des gènes immunitaires clés peuvent orienter le cours de la maladie.
Pourquoi cette maladie bovine compte
La paratuberculose est causée par la bactérie Mycobacterium avium sous‑espèce paratuberculosis (MAP). Les vaches sont généralement infectées tôt dans la vie, mais les signes cliniques apparaissent souvent des années plus tard. Aux stades silencieux et subcliniques, les animaux paraissent sains tout en pouvant excréter de faibles niveaux de bactéries et produire moins de lait. Aux stades cliniques, elles présentent une diarrhée chronique, une perte de poids sévère et une chute importante de la production laitière. Les taux d’infection au niveau des troupeaux peuvent dépasser 50 % dans de nombreuses régions, notamment en Europe et en Amérique du Nord, posant un défi économique et de bien‑être animal. Comme la bactérie peut aussi agir comme un déclencheur environnemental pour des maladies inflammatoires humaines telles que la maladie de Crohn, la pression s’accroît pour améliorer les stratégies de contrôle chez les bovins.
Lire le génome opérationnel
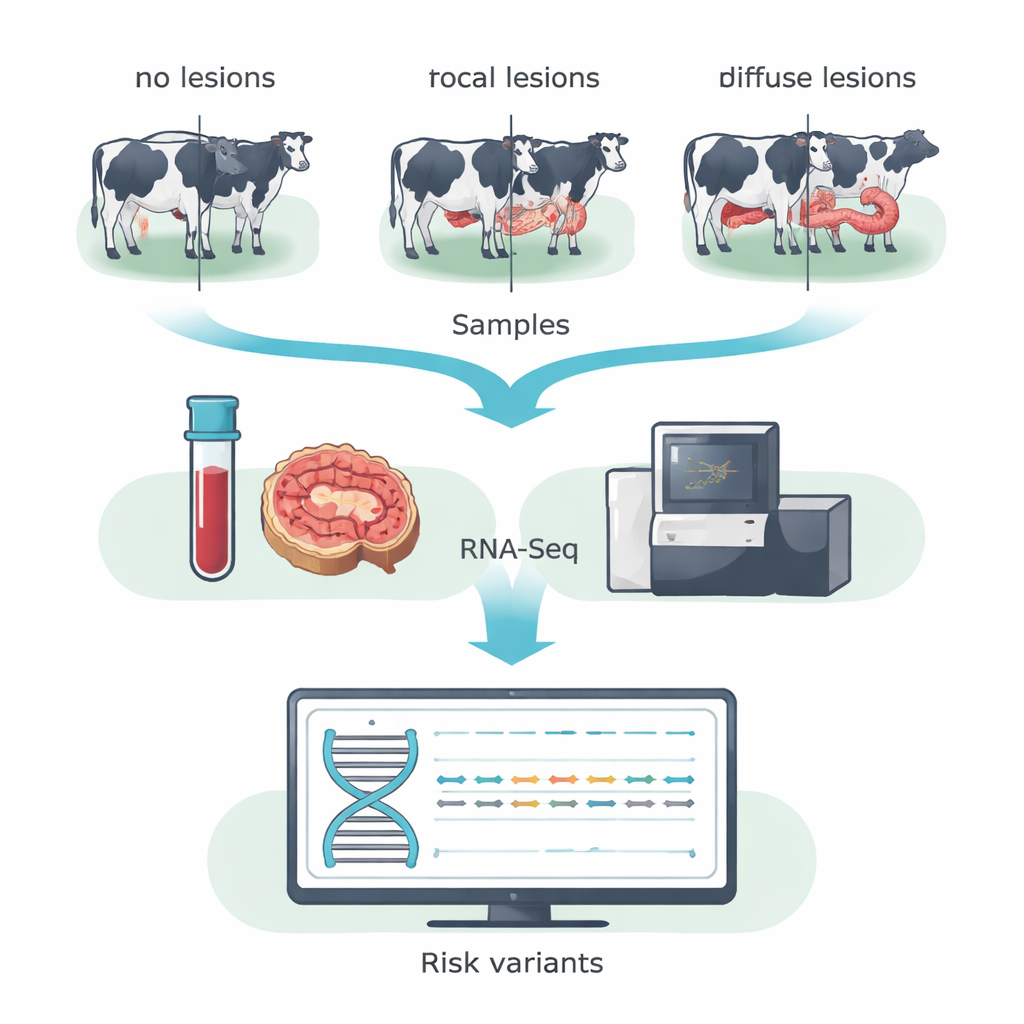
Plutôt que de balayer la séquence d’ADN entière, l’équipe a utilisé le séquençage de l’ARN (RNA‑Seq) pour se concentrer sur les gènes réellement actifs chez l’animal. Ils ont prélevé du sang et des échantillons de la valve iléo‑caecale — une région intestinale fortement affectée par MAP — chez 14 vaches Holstein d’une ferme laitière espagnole. D’après l’examen microscopique des tissus intestinaux, les vaches ont été classées en trois catégories : animaux sans lésions détectables, animaux avec de petites lésions localisées (focales) typiques d’une infection subclinique longue, et animaux avec des lésions étendues et sévères (diffuses) associées à la maladie clinique. En fusionnant les données du sang et de l’intestin au sein de chaque groupe, les chercheurs ont renforcé leur capacité à détecter des changements d’une lettre d’ADN dans des gènes exprimés, appelés SNP codants.
Trouver des changements nuisibles dans des gènes immunitaires clés
Parmi des centaines de milliers de variants, l’équipe s’est concentrée sur ceux qui modifient la séquence protéique et sont prédits comme altérant la fonction des protéines — les variants dits délétères. Ils ont appliqué des filtres stricts pour garantir une grande confiance, puis utilisé des outils de prédiction établis pour signaler les changements à risque. Ce processus d’affinage a révélé 31 variants de ce type uniques aux vaches sans lésions, 15 uniques aux vaches avec lésions focales, et 31 uniques aux vaches avec lésions diffuses. Beaucoup se trouvaient dans des gènes qui régissent la façon dont les cellules immunitaires reconnaissent et éliminent les infections, contrôlent la mort cellulaire et gèrent le métabolisme. Une famille de gènes remarquable était BOLA, la version bovine du complexe majeur d’histocompatibilité de classe II, qui aide les cellules immunitaires à présenter des fragments bactériens aux lymphocytes T. Différents variants potentiellement nuisibles de BOLA ont été trouvés dans les trois groupes de vaches, suggérant que des versions spécifiques de BOLA peuvent orienter les animaux vers la résistance, une infection contrôlée ou une inflammation dommageable.
Des variants d’ADN aux voies de la maladie
Pour comprendre ce que ces changements génétiques pourraient signifier en pratique, les chercheurs ont examiné quelles voies biologiques étaient enrichies dans chaque groupe. Les vaches sans lésions présentaient des variants altérés dans des gènes liés au traitement des antigènes, au trafic vésiculaire et à l’équilibre immunitaire intestinal, notamment BOLA, AP3B1 et CHGA. Ces changements pourraient favoriser une digestion efficace des bactéries au sein des cellules immunitaires et un environnement intestinal stable qui limite les dommages. Chez les vaches avec lésions focales, les variants délétères se regroupaient dans des gènes (ORMDL3 et KANK2) qui diminuent la mort cellulaire programmée et ajustent le métabolisme cellulaire, aidant potentiellement l’hôte à maintenir de faibles nombres bactériens pendant une longue phase subclinique. Chez les vaches avec lésions diffuses, les gènes affectés pointaient vers des voies immunitaires hyperactives telles que la différenciation Th1/Th2 et la présentation d’antigènes, ainsi que le transport de la bile et les voies de réponse aux médicaments. Ici, des gènes altérés de la famille BOLA pourraient conduire à une réaction inflammatoire forte, parfois auto‑dommageable, rappelant des schémas observés dans de nombreuses maladies auto‑immunes et inflammatoires humaines.
Indices pour sélectionner des troupeaux plus résistants
Au‑delà d’éclairer comment différents variants génétiques façonnent la réponse immunitaire à MAP, l’étude a également relié ces changements à risque à des régions connues du génome bovin associées à des traits de santé, y compris la sensibilité à la paratuberculose et à d’autres infections. Bien que ces résultats nécessitent encore une validation sur des troupeaux plus nombreux et ne puissent pas encore être utilisés comme marqueurs diagnostiques autonomes, ils offrent un catalogue prometteur de variants et de gènes candidats. Pour faire simple, le travail suggère que certaines vaches portent des versions de gènes qui les aident à contrôler silencieusement l’infection, tandis que d’autres portent des versions favorisant une inflammation incontrôlée et une maladie sévère. À l’avenir, ces informations pourraient appuyer la sélection et des tests génétiques visant à orienter les troupeaux vers une résistance naturelle accrue, réduisant à la fois les pertes économiques et le besoin de mesures de contrôle intensives.
Citation: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Mots-clés: paratuberculose bovine, génétique de la maladie de Johne, immunité des bovins laitiers, séquençage ARN, sélection pour résistance aux maladies