Clear Sky Science · fr
La signalisation de l’interféron de type I définit une nouvelle signature de la maladie dans les kératinocytes humains atteints de xeroderma pigmentosum C
Pourquoi le soleil peut être si dangereux pour certaines personnes
Pour la plupart d’entre nous, la lumière du soleil évoque la chaleur et la vitamine D. Mais pour les personnes porteuses d’une maladie génétique rare appelée xeroderma pigmentosum C (XP‑C), même une exposition modérée à la lumière du jour peut provoquer des lésions cutanées sévères et un risque extrême de cancer de la peau. Cette étude va au‑delà du problème bien connu de la réparation de l’ADN dans l’XP‑C et met au jour un niveau caché de signalisation de type immunitaire hyperactive au sein de leurs cellules cutanées, apportant de nouveaux indices sur la vulnérabilité et l’inflammation accrues de leur peau après exposition au soleil.
Quand la réparation de l’ADN échoue dans la peau
Nos cellules cutanées réparent en permanence les dommages de l’ADN causés par les rayons UVB du soleil. Une protéine nommée XPC est l’un des premiers « détecteurs » qui repèrent les lésions induites par les UV et déclenchent une importante machinerie de réparation. Dans l’XP‑C, des mutations du gène XPC empêchent cette étape d’alerte précoce, si bien que les dommages dus aux UV s’accumulent au lieu d’être réparés. Les patients atteints d’XP‑C développent des cancers de la peau des milliers de fois plus fréquemment que la population générale et doivent éviter le soleil de façon rigoureuse. Si ce défaut de réparation de l’ADN est bien établi, la manière dont il reprogramme les systèmes de communication internes des cellules — en particulier ceux qui contrôlent l’inflammation — reste beaucoup moins claire.
Explorer les signaux cellulaires au fil du temps
Pour aborder ce problème, les chercheurs ont conçu des kératinocytes humains — les principales cellules de la couche externe de la peau — totalement dépourvus de XPC, et les ont comparés à des cellules normales par ailleurs identiques. Ils ont exposé les deux types cellulaires à un niveau d’UVB soigneusement choisi, correspondant à une dose de coup de soleil modéré dans des conditions réelles. Puis ils ont examiné les cellules à deux moments. Une heure après l’irradiation, ils ont mesuré l’activité de nombreuses enzymes appelées protéines tyrosine kinases, qui activent ou désactivent des signaux en ajoutant de petites étiquettes phosphate. Vingt‑quatre heures plus tard, ils ont utilisé une spectrométrie de masse avancée pour obtenir un large instantané de milliers de protéines et constater lesquelles augmentaient ou diminuaient en abondance. Cette approche en deux étapes leur a permis de suivre à la fois les « signaux d’alarme » précoces et les « réponses en aval » ultérieures au sein des cellules.
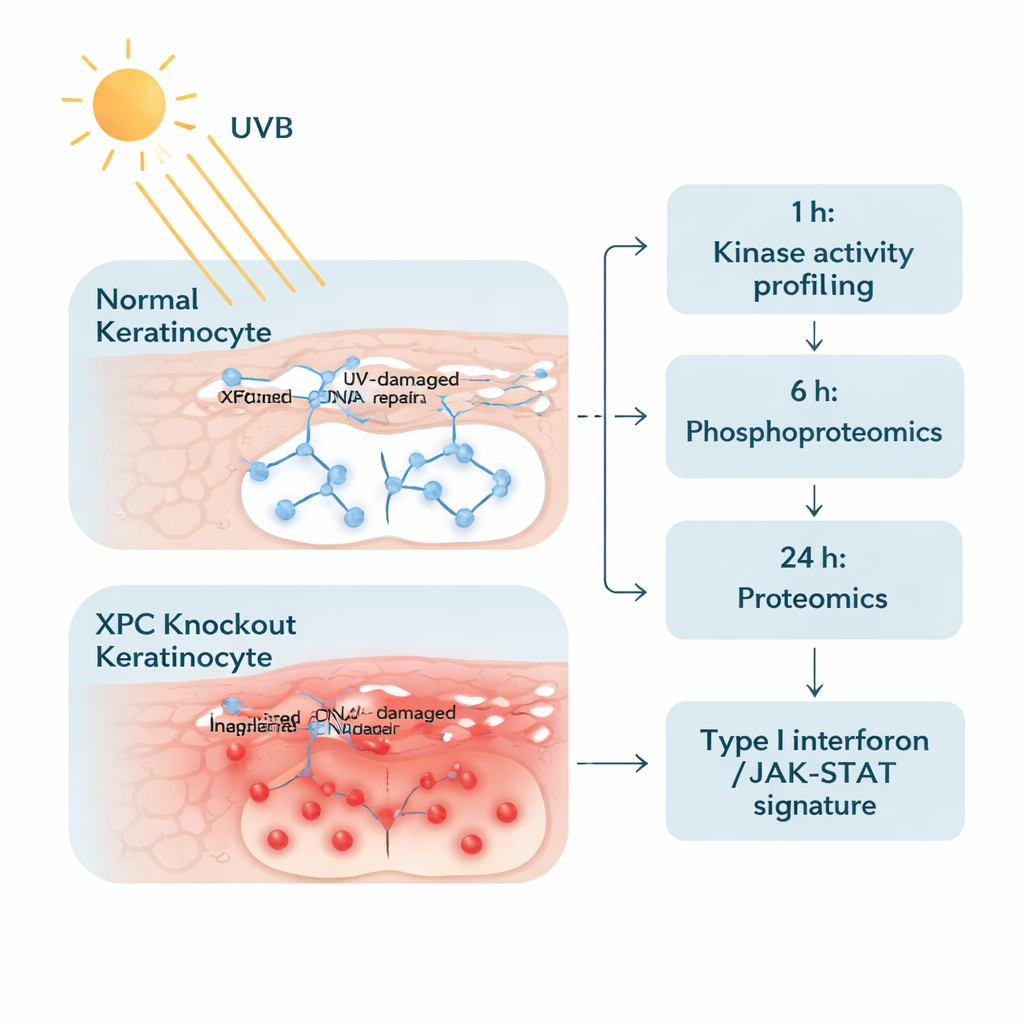
Une voie inflammatoire s’illumine
Le criblage kinomique précoce a révélé que les kératinocytes déficients en XPC répondent aux UVB par une poussée de phosphorylation sur plus d’une centaine de sites par rapport aux cellules normales. Notamment, bon nombre de ces changements se sont regroupés dans la voie de signalisation JAK/STAT — une voie de communication centrale généralement utilisée par des messagers immunitaires tels que les interférons. Des marqueurs liés à JAK1, JAK2, JAK3, TYK2 et aux protéines STAT étaient plus actifs dans les cellules XP‑C, même avant l’exposition aux UVB, et ont été encore renforcés après irradiation. Cela suggère que les cellules sont en état de « vigilance élevée », prêtes à amplifier des messages inflammatoires dès qu’elles rencontrent un stress induit par les UV.
Gènes d’alarme de type interféron dans les cellules cutanées
L’analyse protéomique plus large et réalisée ultérieurement a confirmé et étendu ce constat. Dans les cellules Knockout pour XPC, en particulier après UVB, des centaines de protéines ont été modifiées, et un grand groupe correspondait à des gènes normalement activés par les interférons de type I — les mêmes signaux antiviraux que notre organisme utilise pour combattre les infections. Des protéines telles que MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 et IRF9, classiques « gènes stimulés par l’interféron », étaient fortement élevées. Des analyses de réseaux et de voies ont relié ces protéines à la signalisation JAK/STAT et aux interférons de type I comme thème dominant. Des expériences complémentaires de western blot ont confirmé que des protéines STAT clés étaient davantage phosphorylées, et que ces protéines répondant aux interférons étaient produites à des niveaux bien supérieurs dans les cellules XP‑C que dans les kératinocytes normaux, au repos et surtout après UVB.
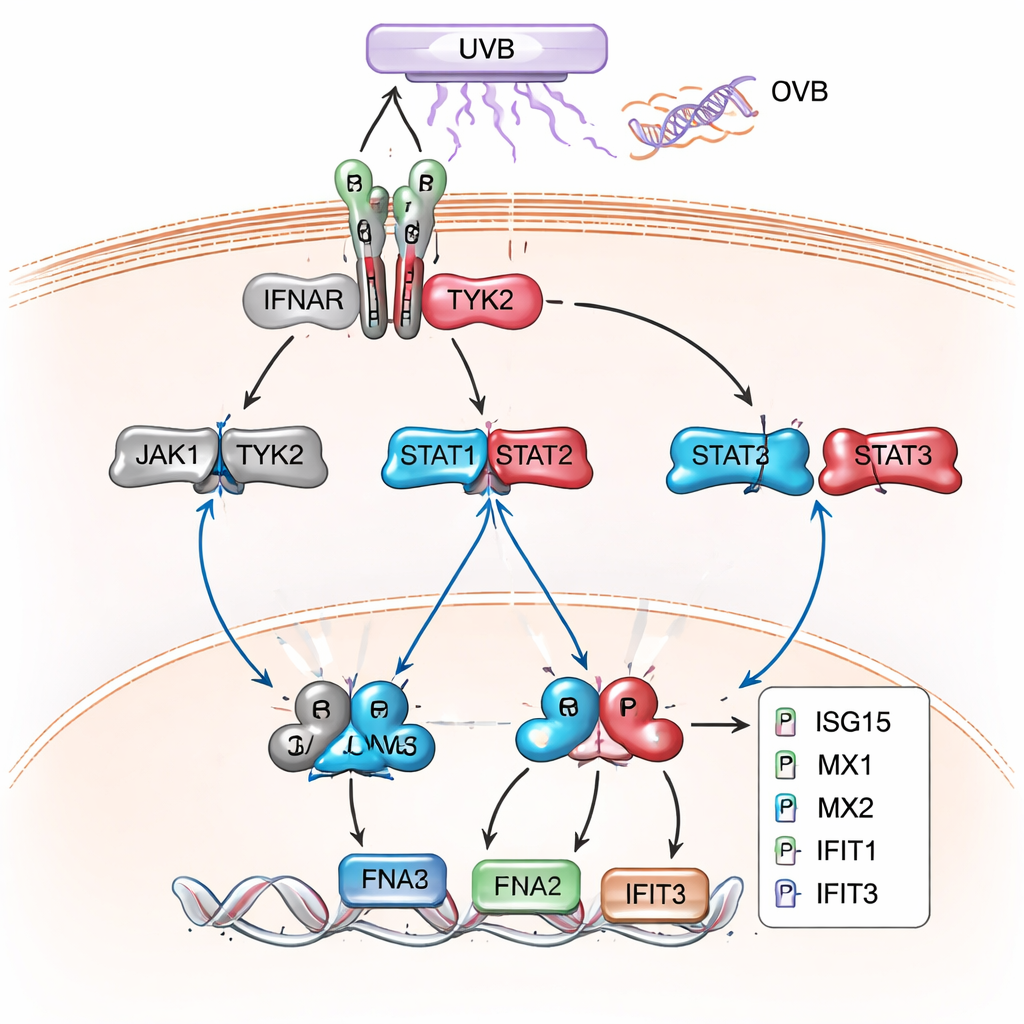
Ce que cela signifie pour les patients et les traitements futurs
Ensemble, ces résultats montrent que l’XP‑C n’est pas seulement une maladie due à une réparation défectueuse de l’ADN ; elle se caractérise également par un état inflammatoire persistant de type interféron au sein des cellules cutanées, activé via la voie JAK/STAT et intensifié par la lumière UV. Pour un lecteur non spécialiste, cela signifie que les kératinocytes XP‑C se comportent comme s’ils combattaient constamment une infection invisible chaque fois qu’ils voient la lumière du soleil, superposant une inflammation chronique aux dommages de l’ADN non réparés. Si l’étude ne teste pas directement de traitements, elle soulève la possibilité que des médicaments finement ciblés sur JAK/STAT ou des circuits inflammatoires connexes pourraient un jour aider à réduire les dommages déclenchés par les UV chez les patients XP‑C et peut‑être dans d’autres affections cutanées inflammatoires présentant cette signature moléculaire.
Citation: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Mots-clés: xeroderma pigmentosum, cancer de la peau, réparation de l’ADN, signalisation des interférons, voie JAK STAT