Clear Sky Science · fr
Modélisation stochastique fractionnaire non linéaire à retard et analyse numérique de la dynamique du virus herpès simplex de type II
Pourquoi ce virus compte toujours
L’herpès génital, le plus souvent causé par le virus herpès simplex de type II (HSV‑II), touche des centaines de millions de personnes dans le monde. Une fois acquis, le virus reste généralement à vie dans l’organisme, réapparaissant de façon imprévisible et se transmettant discrètement même en l’absence de lésions visibles. Cet article ne décrit pas un nouveau médicament ou un vaccin ; il recourt plutôt à des outils mathématiques avancés et à des simulations informatiques pour mieux comprendre comment le HSV‑II se propage dans une population et comment différentes stratégies de contrôle pourraient le contenir.
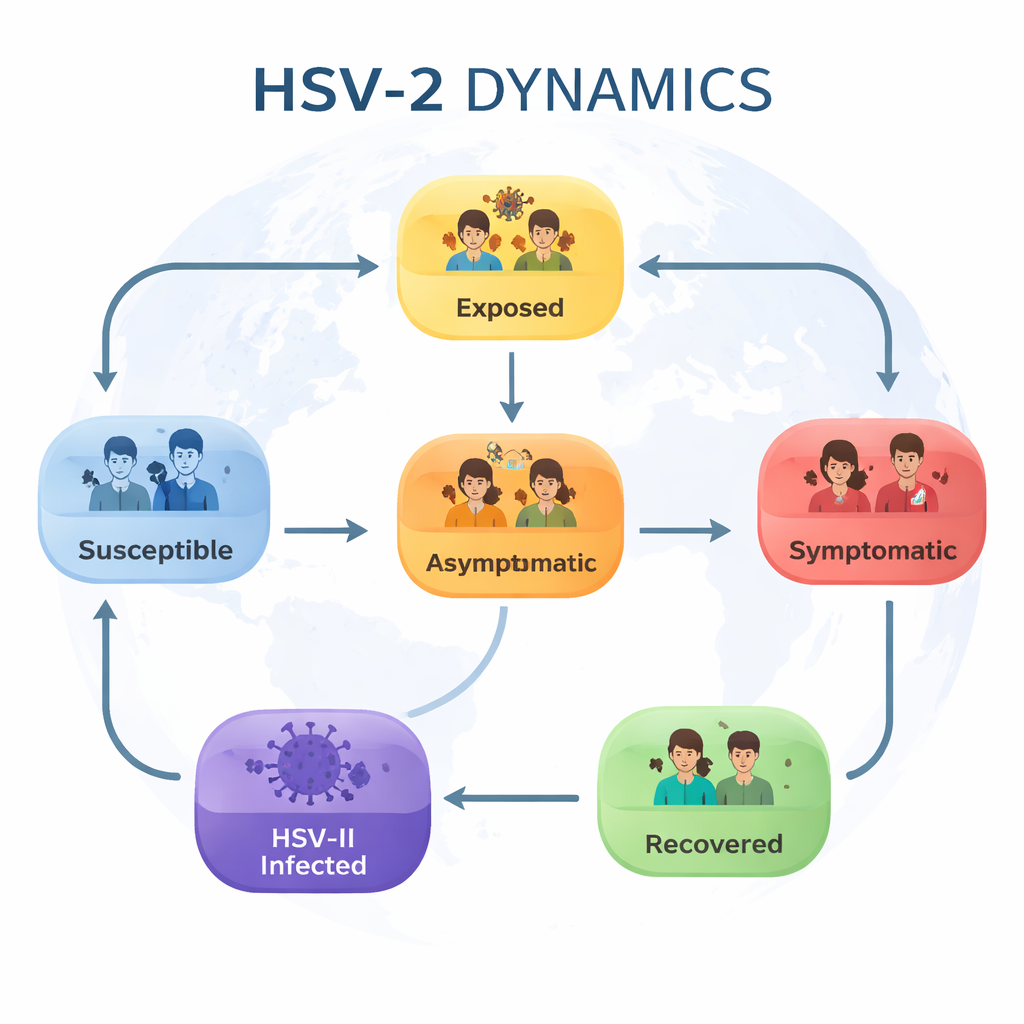
Diviser l’épidémie en groupes simples
Les auteurs commencent par diviser la population en six groupes qui reflètent les principaux stades de l’infection par le HSV‑II : les personnes encore vulnérables (susceptibles), celles récemment infectées mais pas encore contagieuses (exposées), les porteurs sans symptômes (asymptomatiques), ceux présentant des symptômes visibles comme des lésions génitales (symptomatiques), les individus avec une infection établie, et les personnes rétablies pendant un certain temps. Ils décrivent ensuite comment les individus passent d’un groupe à l’autre : infection par contact, progression d’une infection silencieuse à une infection symptomatique, mise sous traitement, guérison, ou perte d’une protection temporaire et retour à la susceptibilité.
Ajouter mémoire, retard et aléa
Les infections réelles n’obéissent pas à des règles mécaniques parfaites, et le modèle en tient compte. D’une part, il inclut un effet de « mémoire » : l’historique des infections influence le comportement et l’immunité actuels, de sorte que le système ne « oublie » pas immédiatement ce qui s’est passé. D’autre part, il y a un décalage temporel explicite entre l’infection et la contagiosité, reflétant les périodes d’incubation et les réponses immunitaires retardées. Enfin, le modèle autorise des fluctuations aléatoires, comme des rencontres fortuites ou des variations de la résistance immunitaire, en ajoutant des termes de bruit conçus ad hoc. Ensemble, ces caractéristiques offrent une image plus riche et plus réaliste du comportement du HSV‑II sur des mois et des années, au lieu de supposer une courbe épidémique parfaitement lisse.
Un nombre unique qui signale le danger
Un résultat central de l’analyse est le nombre de reproduction de base, souvent noté R0. Ce nombre unique résume, en moyenne, combien de nouvelles infections un individu contagieux provoque dans une population majoritairement non infectée. Si R0 est inférieur à 1, les poussées tendent à s’éteindre ; s’il est supérieur à 1, l’infection peut s’installer et persister. Les auteurs montrent que leur système pour le HSV‑II possède deux états d’équilibre principaux : l’un où le virus disparaît et l’autre où il reste présent à long terme. En examinant comment R0 dépend des taux de contact, de la fraction des cas silencieux, de la vitesse de guérison et des taux de mortalité ou d’élimination, ils identifient les leviers les plus influents pour faire basculer le système de la persistance vers l’élimination.
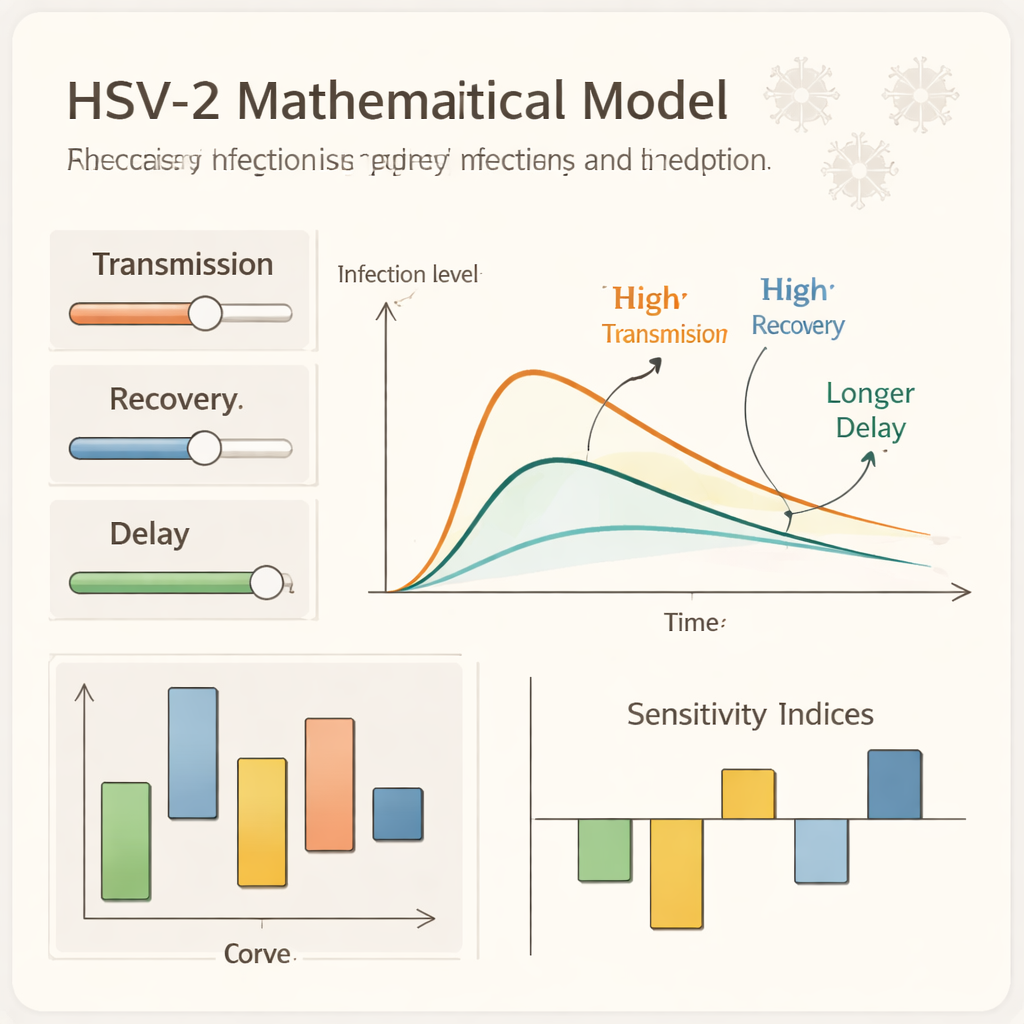
Tester le modèle sur ordinateur
Pour explorer ces idées numériquement, l’équipe met en place un schéma informatique particulier qui reproduit la biologie sous-jacente même en utilisant des pas de temps relativement grands. Cette approche non standard garantit que les tailles de population simulées ne deviennent jamais négatives et restent dans des limites réalistes. En faisant fonctionner le modèle sous de nombreux scénarios, ils suivent l’évolution dans le temps des effectifs de susceptibles, exposés, asymptomatiques, symptomatiques, infectés et rétablis. Ils constatent, par exemple, que des effets de mémoire plus marqués peuvent prolonger une infection faible et persistante, tandis que des délais plus longs déplacent et étirent les pics épidémiques. Leurs calculs de sensibilité montrent que l’augmentation des paramètres liés à la transmission élève R0, alors que l’accélération de la guérison ou de l’élimination le fait baisser, ce qui met en évidence où les efforts de prévention et de traitement sont les plus efficaces.
Ce que cela signifie pour la santé quotidienne
Pour les non spécialistes, le message de ce travail est que l’avenir du HSV‑II au sein d’une communauté n’est pas une fatalité aléatoire. En modélisant soigneusement comment les individus traversent les différents stades de l’infection, et en tenant compte des délais, des effets immunitaires persistants et des événements aléatoires, les auteurs construisent un outil capable de tester des scénarios « et si » avant de les mettre en œuvre dans le monde réel. Leurs résultats suggèrent que réduire les occasions de transmission et améliorer le traitement et la récupération peuvent conjointement pousser le virus vers l’extinction dans une population. Bien que cette étude n’offre pas de remède immédiat, elle fournit un cadre solide pour concevoir des stratégies de santé publique plus intelligentes, évaluer des vaccins potentiels et, finalement, réduire le fardeau à long terme de l’herpès génital.
Citation: Raza, A., Alsulami, M., Lampart, M. et al. Nonlinear fractional stochastic delay modeling and computational analysis of herpes simplex virus type II dynamics. Sci Rep 16, 7009 (2026). https://doi.org/10.1038/s41598-026-37658-w
Mots-clés: herpès génital, transmission du HSV-2, modélisation mathématique, dynamique stochastique, ordre fractionnaire à retard