Clear Sky Science · fr
Wnt-3a exacerbe la production de TNF-α dans les microglies stimulées par le LPS indépendamment de la voie canonique β-caténine
Pourquoi l’inflammation cérébrale compte
De nombreux troubles cérébraux, y compris la maladie de Parkinson, impliquent aujourd’hui une inflammation chronique. Dans ce processus, les cellules immunitaires résidentes du cerveau, appelées microglies, peuvent passer d’un rôle protecteur à un état hyperactif qui endommage les neurones voisins. Cette étude pose une question d’actualité : une molécule de signalisation nommée Wnt‑3a, longtemps considérée comme apaisante et protectrice, peut‑elle en réalité aggraver l’inflammation dans certaines conditions ? La réponse se révèle plus complexe que prévu et illustre pourquoi la même molécule peut être bénéfique dans un contexte et nuisible dans un autre.
Un messager à deux visages
Les protéines Wnt forment une famille de messagers chimiques qui organisent le développement du cerveau, maintiennent les cellules cérébrales à l’âge adulte et modulent la réponse des cellules aux lésions. L’un des membres les mieux étudiés, Wnt‑3a, est généralement associé à une voie de signalisation « canonique » qui stabilise une protéine appelée β‑caténine à l’intérieur des cellules. Dans de nombreux systèmes, l’activation de cette voie semble atténuer l’inflammation et favoriser la survie neuronale, si bien que certains chercheurs ont envisagé d’augmenter Wnt‑3a pour protéger les neurones producteurs de dopamine vulnérables dans la maladie de Parkinson. Toutefois, les Wnt peuvent aussi signaler via des voies alternatives « non canoniques » susceptibles de promouvoir l’inflammation, et la voie dominante dépend du type cellulaire et de son état.
Quand les cellules calmes restent calmes
Pour explorer ces possibilités, les auteurs ont étudié des microglies primaires cultivées à partir de cerveaux de souris. Ils ont d’abord observé des microglies au repos, en état homéostatique, et les ont exposées uniquement à Wnt‑3a. Dans ces conditions calmes, Wnt‑3a n’augmente pas la libération de molécules inflammatoires clés telles que le TNF‑α ou l’IL‑1β. Bien que certaines voies de signalisation intracellulaire soient activées, les microglies ne basculent pas vers un profil fortement inflammatoire. Cela suggère que, dans un cerveau sain et non enflammé, l’ajout isolé de Wnt‑3a a peu d’effet direct sur la production inflammatoire microgliale.
Quand des cellules inflammées sont poussées plus loin
Le tableau a changé radicalement une fois les microglies préalablement stimulées dans un état inflammatoire par du lipopolysaccharide bactérien (LPS), un outil standard de laboratoire pour imiter une infection. Comme prévu, le LPS seul induisait une forte augmentation de la production de TNF‑α. Mais lorsque Wnt‑3a était ajouté en même temps que le LPS, les microglies libéraient significativement plus de TNF‑α qu’avec le LPS seul, tandis que l’IL‑1β n’augmentait pas davantage. Des mesures détaillées ont montré que cette hausse de TNF‑α ne résultait ni d’une activation accrue de la voie inflammatoire NFκB habituelle, ni d’une activation supplémentaire de la voie canonique β‑caténine. Le blocage de la voie β‑caténine par une protéine appelée DKK1 n’a pas empêché la montée de TNF‑α induite par Wnt‑3a, indiquant que la voie « anti‑inflammatoire » attendue n’en était pas la cause.
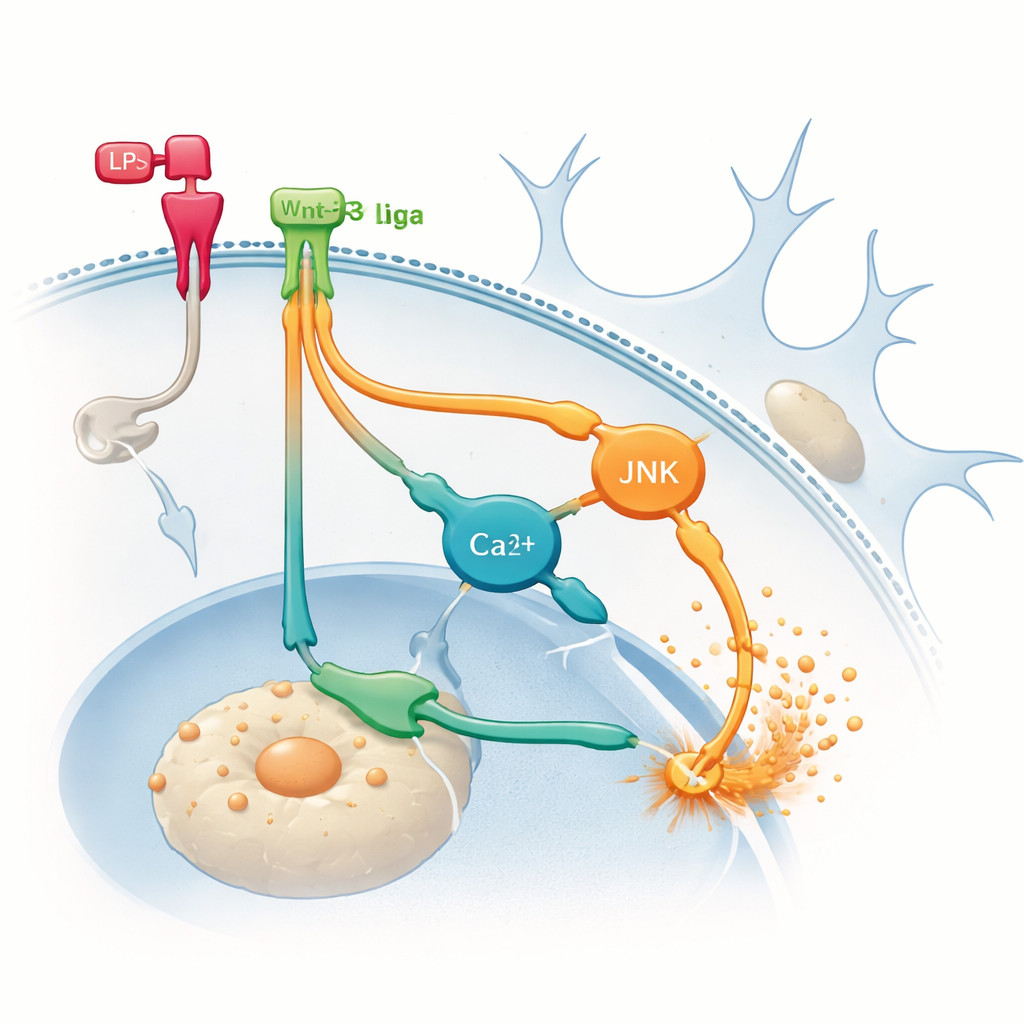
Des voies cachées qui attisent les flammes
Pour localiser l’origine de l’inflammation supplémentaire, l’équipe s’est intéressée aux voies non canoniques alternatives que peuvent emprunter les Wnt. Ils ont bloqué pharmacologiquement deux branches de signalisation à l’intérieur des microglies : l’une impliquant une protéine appelée JNK, et l’autre liée aux variations de calcium intracellulaire. L’inhibition de l’une ou l’autre de ces branches a réduit la production de TNF‑α induite par le LPS et, de manière importante, a empêché Wnt‑3a d’amplifier encore le TNF‑α. Ces résultats suggèrent que, une fois les microglies déjà enflammées, Wnt‑3a peut privilégier les voies non canoniques qui amplifient les signaux inflammatoires plutôt que de les calmer. Autrement dit, le même messager peut emprunter un itinéraire interne différent selon l’état initial de la cellule, avec des conséquences très distinctes.
Test dans un modèle de Parkinson
Les chercheurs ont ensuite demandé si ce comportement de Wnt‑3a chez les microglies se traduirait par des effets plus importants sur les neurones dans un cerveau vivant. Ils ont administré Wnt‑3a directement dans les ventricules cérébraux de souris traitées par la toxine MPTP, un modèle largement utilisé reproduisant les atteintes des neurones dopaminergiques et l’activation microgliale de type Parkinson. Comme prévu, le MPTP réduisait le nombre de neurones dopaminergiques et augmentait le nombre de microglies dans une région mésencéphalique cruciale pour le mouvement. Cependant, un excès de Wnt‑3a n’a pas aggravé davantage la perte neuronale ni modifié de façon significative le nombre de microglies par rapport aux animaux traités par le véhicule. Dans ce contexte in vivo complexe, Wnt‑3a n’a ni sauvé ni clairement aggravé les effets délétères de la toxine sur la période étudiée.
Que signifie cela pour les thérapies futures
Globalement, l’étude montre que Wnt‑3a n’est pas un simple interrupteur marche/arrêt de l’inflammation cérébrale. Chez des microglies au repos, il a peu d’effet, mais chez des cellules déjà enflammées il peut augmenter sélectivement la libération de TNF‑α via des voies non canoniques, indépendamment de la voie classique β‑caténine. Parallèlement, l’ajout de Wnt‑3a dans un modèle murin proche de la maladie de Parkinson n’a pas manifestement protégé ni aggravé à court terme la survie des neurones dopaminergiques. Pour ceux qui s’intéressent aux traitements futurs, le message clé est que cibler la signalisation Wnt exigera une appréciation attentive du contexte cellulaire. Des thérapies fondées sur Wnt‑3a ou des molécules apparentées pourraient être utiles dans certaines situations, mais risquent d’être contre‑productives dans d’autres si elles intensifient involontairement une inflammation nocive.
Citation: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Mots-clés: inflammation cérébrale, microglie, signalisation Wnt, maladie de Parkinson, TNF-alpha