Clear Sky Science · fr
Activation améliorée du méropénem par un peptide dérivé du microbiome ciblant la carbapénémase oxacillinase 48 chez des isolats de Klebsiella pneumoniae résistants aux carbapénèmes
Pourquoi cela compte pour la santé quotidienne
La résistance aux antibiotiques rend des infections autrefois traitables plus difficiles, voire impossibles à guérir, en particulier à l’hôpital. Cette étude explore une nouvelle façon de « réarmer » un antibiotique de dernier recours existant, le méropénem, contre une bactérie dangereuse appelée Klebsiella pneumoniae, qui infecte souvent les patients en réanimation. Plutôt que d’inventer un nouveau médicament, les chercheurs testent une petite molécule d’aide, un peptide issu du microbiome humain, qui désactive l’un des outils clés de résistance de la bactérie afin que le méropénem retrouve son efficacité.
Un germe hospitalier tenace et son bouclier chimique
Klebsiella pneumoniae est une cause courante de pneumonies, d’infections sanguines et d’infections urinaires chez les patients hospitalisés. Certaines souches sont devenues résistantes aux carbapénèmes, une classe puissante d’antibiotiques que les médecins réservent en général aux cas graves et difficiles à traiter. Nombre de ces bactéries produisent une enzyme particulière appelée OXA-48, qui agit comme un bouclier chimique en dégradant les carbapénèmes avant qu’ils ne puissent tuer le microbe. Au Moyen-Orient, y compris en Iran, les souches productrices d’OXA-48 sont particulièrement répandues, et les options thérapeutiques diminuent à mesure que la résistance apparaît même contre des combinaisons médicamenteuses plus récentes. Cela a fait de l’OXA-48 une cible prioritaire pour de nouvelles thérapies.
Conception d’un peptide d’aide issu du microbiome humain
Les chercheurs avaient auparavant utilisé des modèles informatiques pour parcourir des bases de données de peptides antimicrobiens naturels humains — de courts fragments protéiques produits par notre organisme et par les microbes résidents — afin d’identifier des candidats susceptibles de se lier fortement à l’enzyme OXA-48. Par des simulations d’accostage virtuel et de dynamiques moléculaires longues, ils ont affiné ces candidats et sélectionné l’un d’eux, nommé M104, dont les calculs prédisaient qu’il se lierait de façon stable au site actif de l’enzyme et bloquerait sa fonction tout en restant hydrosoluble et chimiquement stable. Dans cette étude, ils ont mis M104 à l’épreuve en laboratoire, en le combinant avec le méropénem contre 20 isolats de Klebsiella issus de patients : 10 producteurs d’OXA-48 résistants au méropénem, et 10 dépourvus de carbapénémases et sensibles aux antibiotiques.
Rendre un ancien antibiotique à nouveau efficace
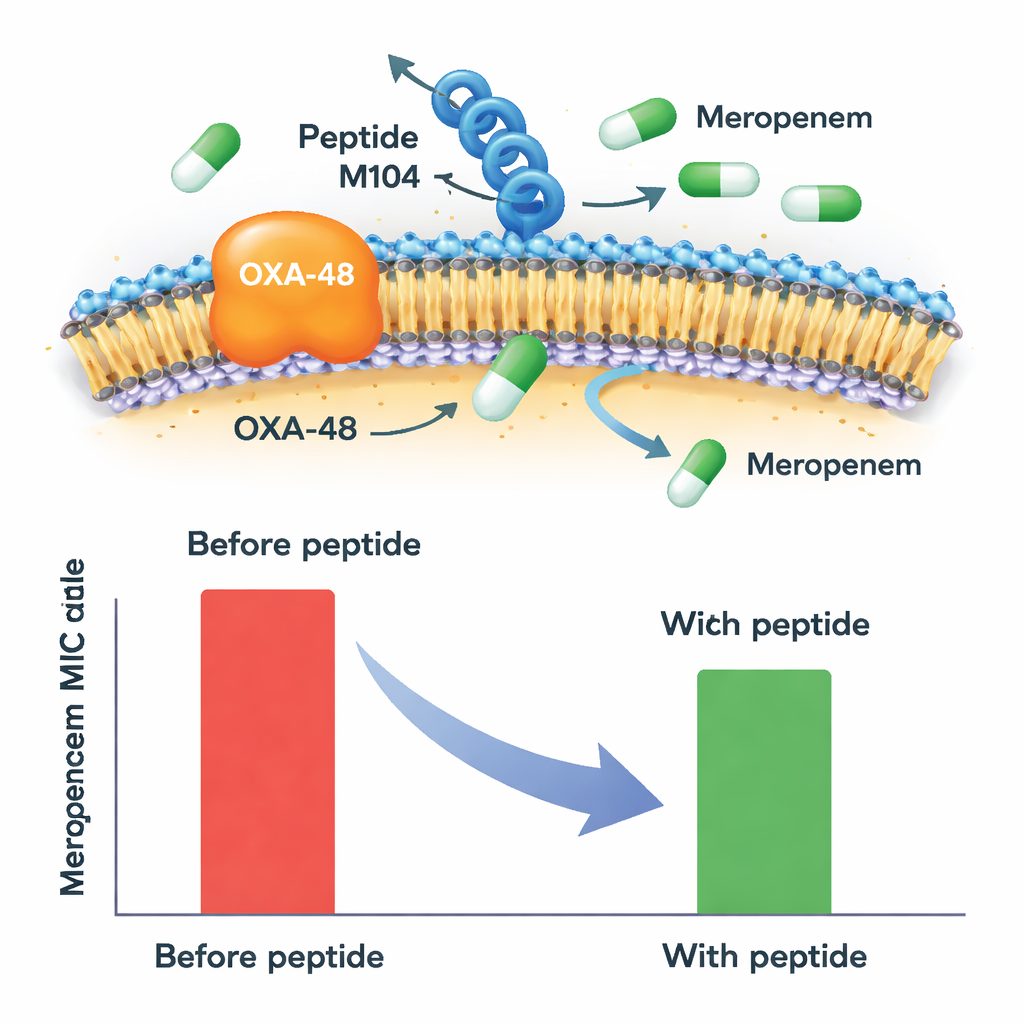
Lorsque le méropénem était utilisé seul, tous les isolats de Klebsiella positifs pour OXA-48 étaient clairement résistants. L’ajout du peptide M104 a changé la donne. À sa concentration la plus élevée testée, M104 a réduit la quantité de méropénem nécessaire pour stopper la croissance bactérienne d’au moins moitié — et dans certains cas jusqu’à six fois — pour chaque producteur d’OXA-48 résistant testé. Cela a fait basculer de nombreuses souches d’un statut clairement résistant vers une zone intermédiaire, voire sensible, selon les seuils cliniques acceptés. Fait important, M104 n’a pas eu d’effet bactéricide seul et n’a pas potentialisé le méropénem lorsque les bactéries ne possédaient pas l’enzyme OXA-48, ce qui suggère une action très spécifique sur ce mécanisme de résistance plutôt qu’une toxicité large et non sélective.
Défis posés par les biofilms visqueux et contrôles de sécurité
De nombreuses infections hospitalières impliquent des biofilms — des communautés bactériennes visqueuses et stratifiées qui adhèrent aux dispositifs et aux tissus et sont beaucoup plus difficiles à éradiquer que des cellules libres. L’équipe a donc testé si M104 pouvait aider le méropénem à prévenir la formation de biofilms ou à éliminer des biofilms déjà établis pour des souches de Klebsiella formant fortement des biofilms. Bien que la combinaison peptide–méropénem ait généralement divisé par deux la quantité de médicament nécessaire pour bloquer la croissance des biofilms ou commencer à déloger des biofilms matures, ces effets sont restés modestes et n’ont pas atteint une signification statistique nette dans cet échantillon réduit. Du côté de la sécurité, M104 n’a montré aucun dommage détectable aux globules rouges humains et n’a pas réduit la viabilité des fibroblastes cutanés humains après 24 heures à une concentration plus élevée que celle utilisée pour les tests bactériens ; ce n’est qu’après 48 heures que la survie cellulaire a diminué d’environ 10 %. Les comparaisons de séquences ont également suggéré un faible risque que le peptide cible par inadvertance d’autres protéines bactériennes ou humaines.
Ce que cela pourrait signifier pour les traitements futurs
Globalement, les résultats suggèrent que le peptide M104 peut désarmer spécifiquement l’enzyme de résistance OXA-48 et restaurer une grande partie de l’efficacité du méropénem contre des Klebsiella pneumoniae autrement intraitables, du moins pour des bactéries en état planctonique. Bien que son impact sur des biofilms établis et résistants ait été limité dans les conditions testées, l’étude présente le premier bloqueur peptidique rapporté de l’OXA-48 et démontre que de tels adjuvants ciblés peuvent être à la fois efficaces et relativement peu nocifs pour les cellules humaines à court terme. Avec des tests supplémentaires sur un plus grand nombre de souches bactériennes, d’autres carbapénèmes, des formulations optimisées et des modèles animaux, ce type de thérapie d’appoint de précision pourrait contribuer à prolonger la durée d’utilité de nos antibiotiques les plus puissants, plutôt que de laisser les cliniciens faire face à des infections résistantes sans options.
Citation: Sadeghi, S., Faramarzi, M.A. & Siroosi, M. Enhanced meropenem activity by a microbiome derived peptide targeting oxacillinase 48 carbapenemase in carbapenem resistant Klebsiella pneumoniae isolates. Sci Rep 16, 7589 (2026). https://doi.org/10.1038/s41598-026-37644-2
Mots-clés: résistance aux antibiotiques, Klebsiella résistante aux carbapénèmes, enzyme OXA-48, méropénem, inhibiteurs peptidiques