Clear Sky Science · fr
Modèle pour la description des interactions entre les ellagitannins et les ions Fe(II)
Pourquoi les composés végétaux dans les aliments pour animaux comptent
Les bactéries résistantes aux antibiotiques représentent une préoccupation croissante pour les agriculteurs et les responsables de la santé publique. Beaucoup de ces microbes difficiles à traiter apparaissent chez le bétail, où les antibiotiques sont encore largement utilisés dans les aliments. Cette étude porte sur les tanins — des composés naturels d’origine végétale — comme alternative prometteuse. Elle explique en particulier comment un groupe particulier de tanins issus du bois de châtaignier peut se lier au fer de façons susceptibles d’affamer les bactéries d’un nutriment dont elles ont impérativement besoin pour se développer.
Défenseurs naturels cachés dans les arbres
Les tanins sont des molécules végétales amères qui donnent à un vin rouge son astringence et qui sont utilisées depuis des siècles pour le tannage du cuir et la fabrication d’encres. Ils sont abondants dans de nombreux aliments et aliments pour animaux et sont généralement sans danger pour les animaux et les humains. Certains types, appelés ellagitannins, sont particulièrement intéressants car ils possèdent de nombreux « petits mains » chimiques capables de s’accrocher aux ions métalliques tels que le fer. L’extrait de bois de châtaignier, déjà utilisé dans l’alimentation animale, contient plusieurs ellagitannins, dont deux gros appelés roburin A et roburin D. Des travaux antérieurs ont montré que des apparentés plus simples de ces composés peuvent lier le fer et potentiellement empêcher les bactéries d’accéder à cet élément essentiel.
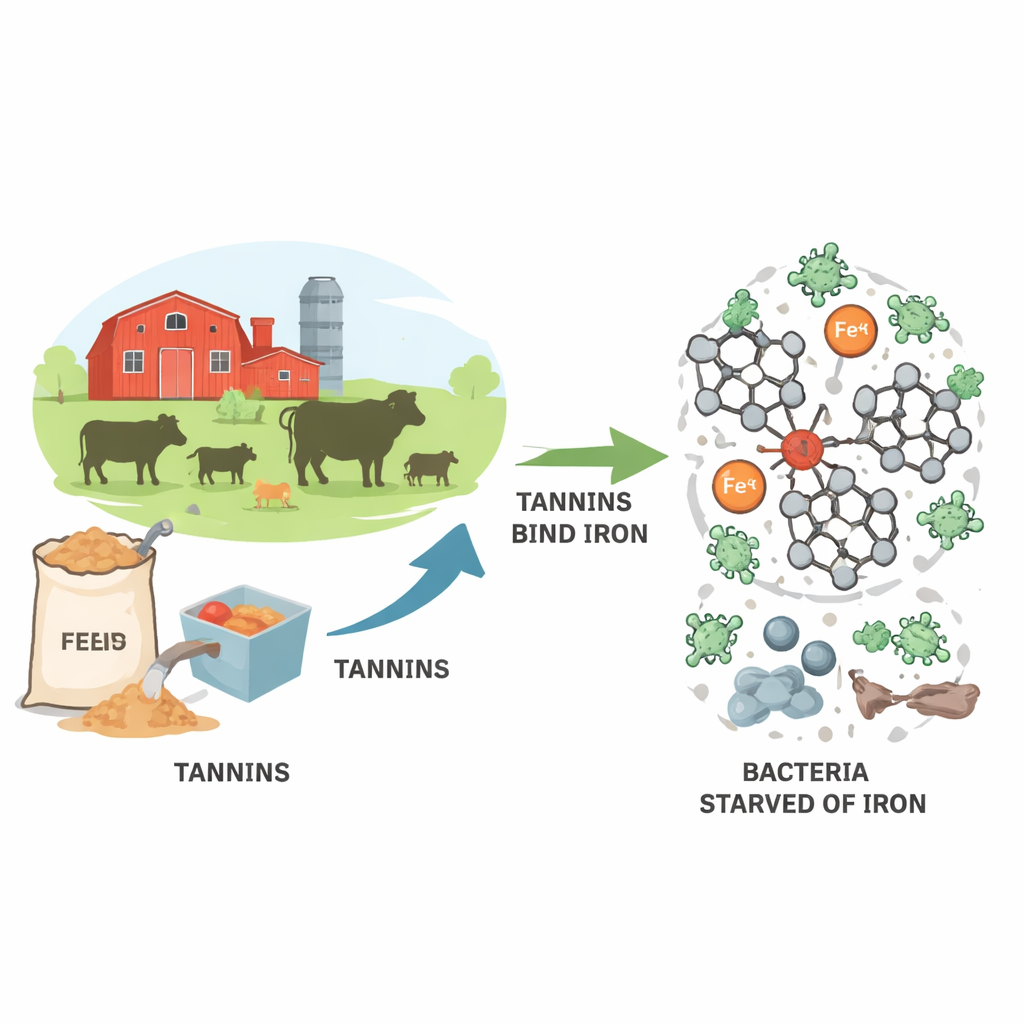
Priver les bactéries de leur métal favori
Les bactéries ne peuvent pas prospérer sans fer. Elles l’utilisent pour alimenter la respiration, construire l’ADN et faire fonctionner de nombreuses réactions enzymatiques. Dans l’intestin des animaux ou dans des milieux de culture, elles s’approvisionnent normalement en fer au moyen de leurs propres petites molécules capteuses de fer. Les ellagitannins gênent ce processus en formant des complexes serrés avec les ions fer, « verrouillant » effectivement le métal et le rendant inaccessible aux bactéries. Les auteurs se sont concentrés sur le fer sous sa forme Fe(II), état rapidement capturé par les tanins en solution aqueuse avant une oxydation lente vers Fe(III). En isolant roburin A et D à partir de l’extrait de châtaignier et en les étudiant dans des solutions soigneusement contrôlées, l’équipe a pu suivre l’efficacité de ces grands tanins à retirer le fer de la phase liquide.
Explorer comment les tanins saisissent le fer
Pour comprendre les détails, les chercheurs ont d’abord examiné comment les roburins gagnent et perdent des protons (un processus appelé équilibre acide–base) lorsque le pH change. À l’aide de la spectroscopie ultraviolet–visible, ils ont suivi les déplacements des absorptions lumineuses des roburins selon différents niveaux de pH. Ces déplacements ont révélé que roburin A et D se comportent de façon similaire à leurs cousins plus petits, la vescalagine et la castalagine, mais avec environ deux fois plus de sites capables de perdre un proton puis de participer à la liaison du fer. Ensuite, ils ont mélangé tanins et fer à des rapports variables et ont de nouveau utilisé l’absorption de la lumière pour établir des diagrammes de Job, qui montrent quel rapport de mélange produit le complexe fer–tanin maximal. À partir de ces données, ils ont conclu que chaque molécule de roburin peut lier six ions Fe(II) — soit le double de la capacité des ellagitannins plus petits.
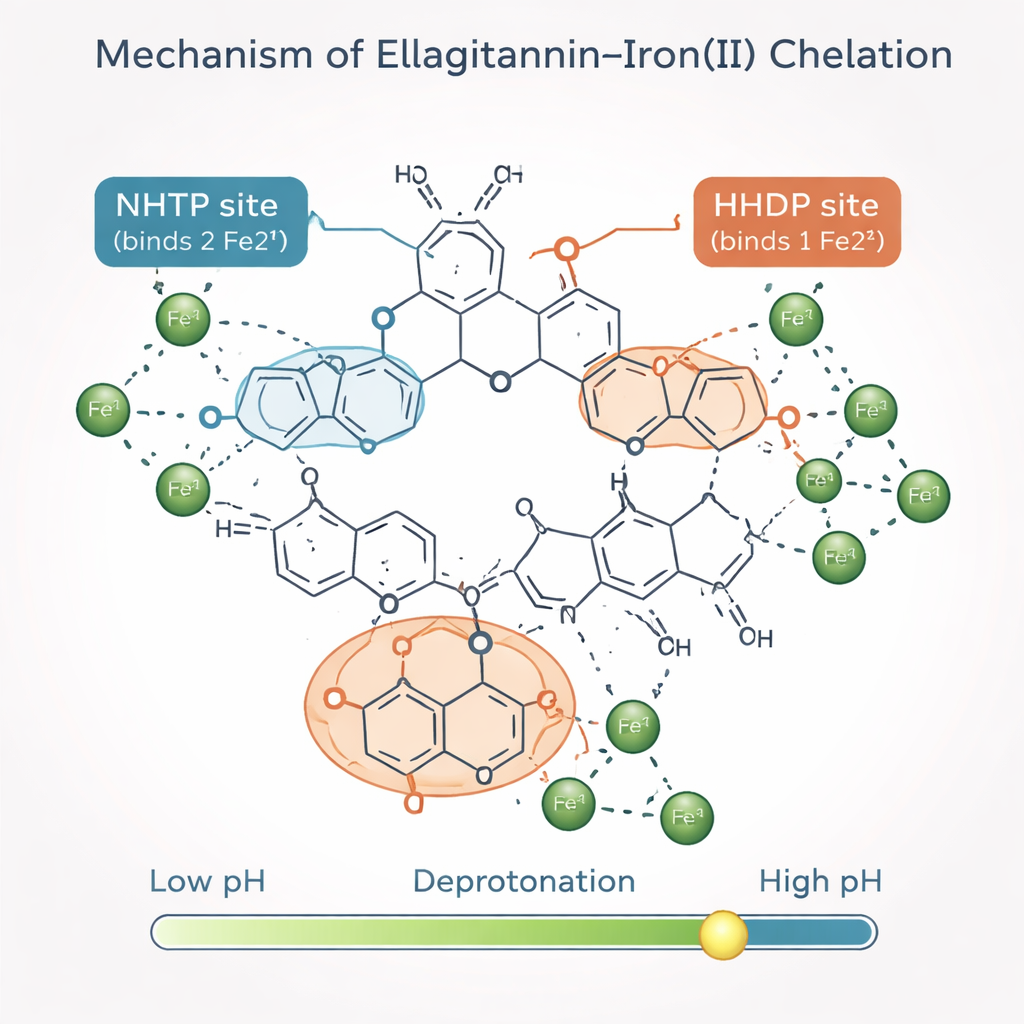
Une carte prédictive des points chauds de liaison au fer
Au-delà du simple comptage du nombre d’ions fer capturés, les auteurs voulaient savoir quels « modules » structurels des ellagitannins effectuent le travail. Ils ont construit un modèle mathématique qui considère chaque molécule d’ellagitannin comme une collection de blocs constitutifs répétitifs. Deux modules clés, appelés groupes NHTP et HHDP, offrent chacun des sites de liaison spécifiques pour le fer une fois qu’ils ont perdu leurs protons les plus acides. En combinant leurs nouvelles mesures avec des données antérieures de résonance magnétique nucléaire et de spectroscopie, l’équipe a montré que chaque groupe NHTP lie typiquement deux ions fer, tandis que chaque groupe HHDP en lie un. Avec seulement quelques paramètres ajustables, leur modèle a reproduit avec précision les diagrammes de Job expérimentaux non seulement pour les ellagitannins plus simples mais aussi pour les plus grands roburins qui n’avaient pas servi à l’entraînement du modèle.
Conséquences pour une agriculture plus verte
En termes simples, ce travail transforme la chimie complexe des tanins et du fer en un mode d’emploi utilisable. Il montre qu’en comptant les unités NHTP et HHDP dans un ellagitannin, les scientifiques peuvent prédire combien d’ions fer une molécule donnée capturera dans une plage de conditions légèrement acides. Parce que les extraits de châtaignier riches en roburins saisissent plus de fer que les tanins plus petits ou que de simples acides végétaux, ils constituent des candidats solides pour limiter l’apport en fer disponible aux bactéries intestinales nuisibles des animaux d’élevage. Bien que des recherches supplémentaires soient nécessaires — notamment pour d’autres structures de tanins et pour le fer sous d’autres formes — ce modèle aide à orienter la conception et la sélection d’additifs végétaux pour aliments, susceptibles de réduire la dépendance aux antibiotiques conventionnels et de soutenir une production animale plus durable et « plus verte ».
Citation: Frešer, F., Hostnik, G. & Bren, U. Model for the description of interactions between ellagitannins and Fe(II) ions. Sci Rep 16, 6631 (2026). https://doi.org/10.1038/s41598-026-37616-6
Mots-clés: ellagitannins, chélatation du fer, tanins dans les aliments pour animaux, alternatives aux antibiotiques, extrait de bois de châtaignier