Clear Sky Science · fr
Inactivation de LIMK2 supprime la différenciation des fibroblastes dermiques induite par stimulation mécanique et la résistance à l’apoptose
Pourquoi certaines cicatrices prolifèrent de manière incontrôlée
La plupart des coupures et des plaies chirurgicales laissent une ligne fine et plate. Mais chez certaines personnes, le processus de réparation s’emballe et forme des cicatrices épaisses et surélevées appelées cicatrices hypertrophiques ou chéloïdes, qui peuvent démanger, faire mal et limiter les mouvements. Cette étude explore pourquoi des cellules cutanées ordinaires deviennent parfois des productrices excessives de cicatrices, et désigne un interrupteur moléculaire unique, nommé LIMK2, qui pourrait être atténué pour empêcher les cicatrices de s’étendre de façon incontrôlée.
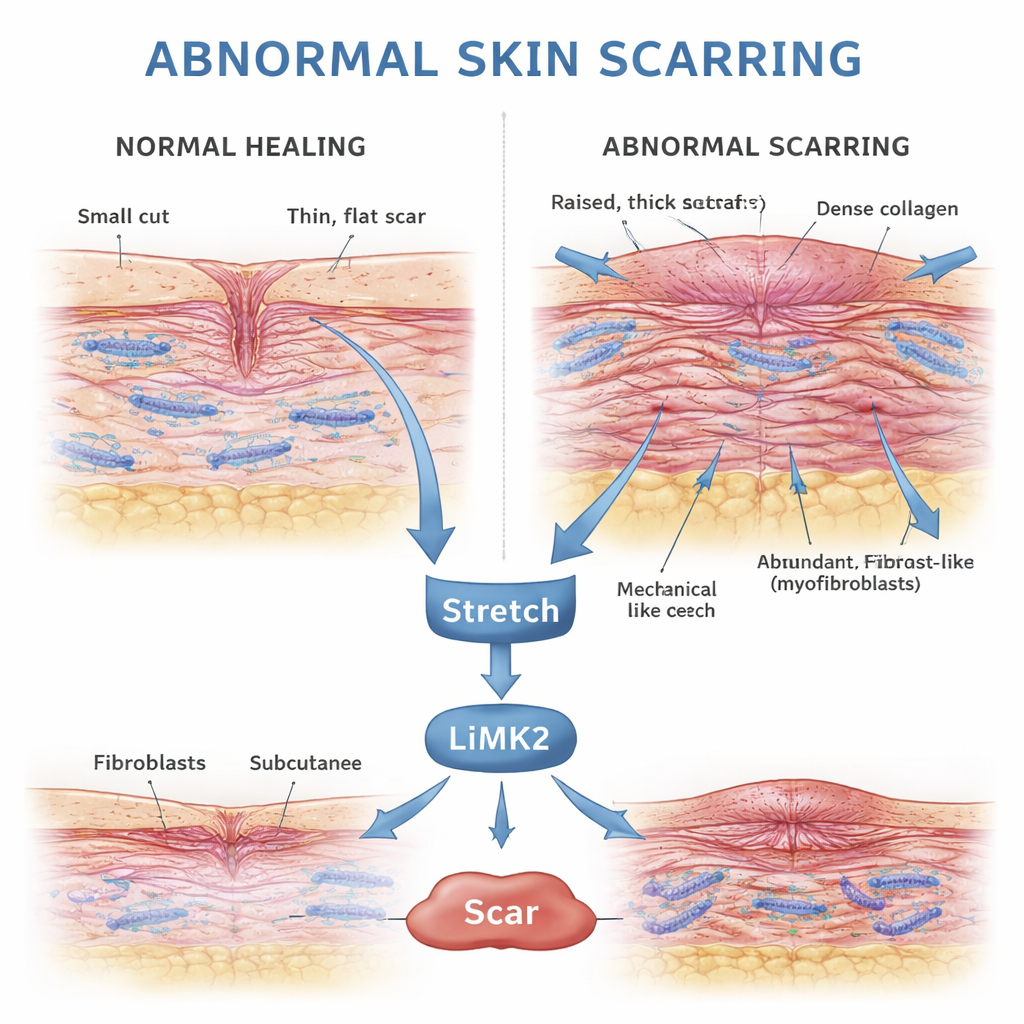
Comment la peau guérit normalement après une blessure
Quand la peau est blessée, l’organisme déclenche un programme de réparation finement chronométré. Les fibroblastes — cellules « ouvrières » du derme — migrent vers la plaie, se multiplient et déposent du collagène, l’armature protéique du nouveau tissu. Beaucoup de ces fibroblastes se transforment temporairement en une forme plus contractile, les myofibroblastes, qui aident à rapprocher les bords de la plaie. Une fois la surface refermée et le tissu stabilisé, ces myofibroblastes doivent normalement disparaître via un processus contrôlé appelé apoptose, laissant une cicatrice modeste et souple.
Quand les forces quotidiennes aggravent les cicatrices
Les cicatrices anormales apparaissent souvent là où la peau est constamment étirée — sur la poitrine, les épaules ou le bas-ventre. Cette observation a conduit les chercheurs à suspecter que les forces mécaniques, comme la traction et la tension le long d’une plaie en cours de guérison, peuvent pousser les fibroblastes à rester actifs trop longtemps. Des travaux antérieurs ont montré qu’étirer ces cellules en laboratoire augmente une protéine appelée α-SMA, un marqueur des myofibroblastes, et active des gènes qui aident les cellules à résister à l’apoptose. La nouvelle étude se concentre sur LIMK2, un élément clef d’une chaîne de signalisation mécanique à l’intérieur des cellules qui relie l’étirement physique aux modifications du squelette interne constitué de filaments d’actine.
Un interrupteur clé pour les cellules formatrices de cicatrices
Pour tester le rôle de LIMK2, les chercheurs ont utilisé des fibroblastes dermiques humains issus de peau normale et de tissus chéloïdes. Ils ont introduit une version inactive de LIMK2 dans certaines cellules, laissant d’autres inchangées ou leur fournissant une version constamment active comme témoins. Lorsqu’on étirait mécaniquement les cellules, les fibroblastes normaux réagissaient comme attendu : hausse rapide de la cofiline phosphorylée et fibres d’actine renforcées, augmentation de l’α-SMA, plus de production de collagène et niveaux plus élevés de Bcl-2, une protéine protectrice contre la mort cellulaire, accompagnés de niveaux réduits de la protéine pro-apoptotique BAX. En contraste frappant, les fibroblastes avec LIMK2 inactif changeaient à peine sous l’étirement. Ils n’augmentaient pas l’α-SMA, n’élevaient pas Bcl-2 ni ne réduisaient BAX, et produisaient moins de collagène. Ces cellules contractaient aussi moins fortement des gels de collagène et ramperaient plus lentement dans un test simulant une plaie, suggérant une force de traction amoindrie et une capacité réduite d’envahir les tissus environnants.
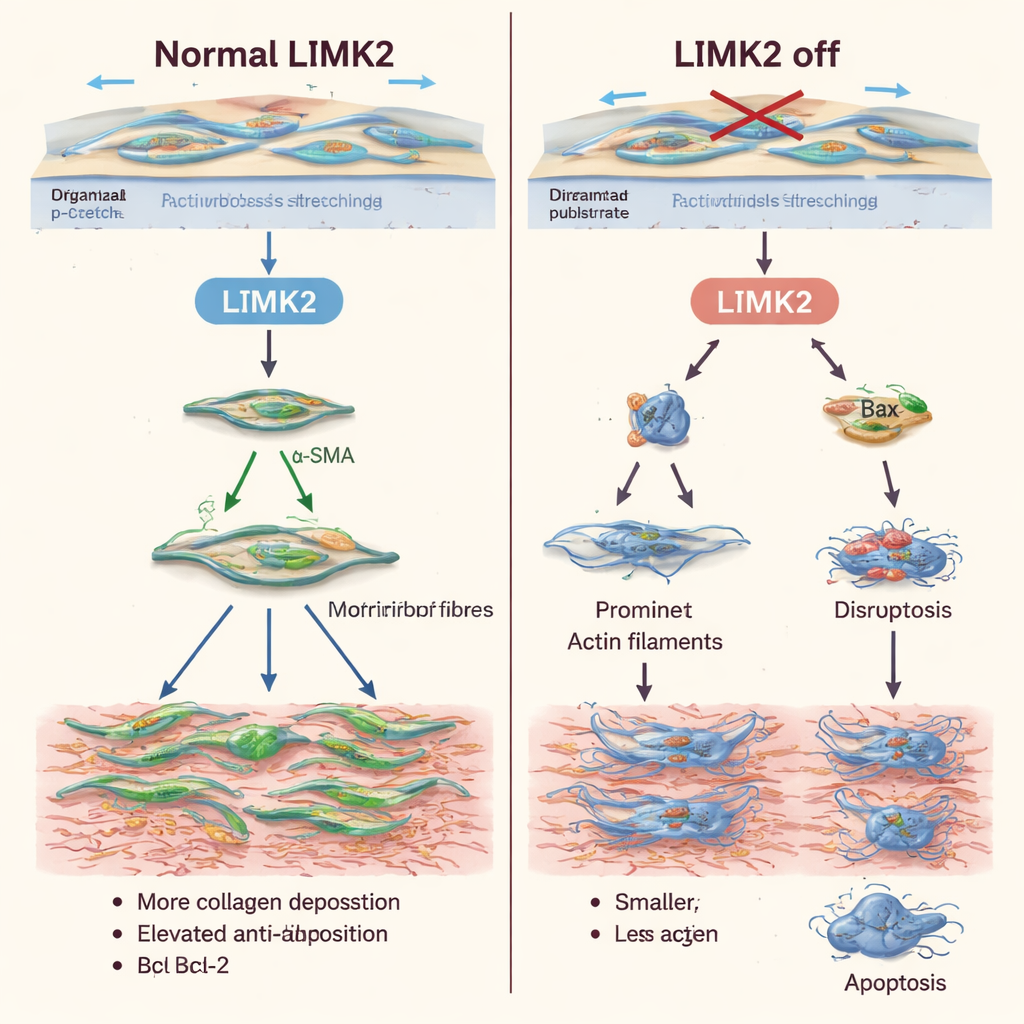
Rendre les cellules cicatricielles récalcitrantes plus faciles à éliminer
Au-delà de l’effet sur le comportement des fibroblastes sous tension, l’inactivation de LIMK2 les rendait plus susceptibles de mourir et moins susceptibles de se multiplier. Les cellules avec LIMK2 inactif présentaient des niveaux plus élevés d’apoptose au repos, et l’étirement mécanique — normalement un signal de survie — ne les protégeait plus. La cytométrie en flux et le marquage fluorescent ont confirmé qu’un plus grand nombre de cellules se trouvaient en phases précoces ou tardives de mort cellulaire programmée. En parallèle, les comptages cellulaires et les tests de marquage de l’ADN ont montré que ces cellules se divisaient beaucoup moins que la normale. Des schémas similaires sont apparus lorsque l’équipe a utilisé la latrunculine A, un médicament qui perturbe les filaments d’actine, étayant l’idée que LIMK2 agit principalement en contrôlant le cadre interne de la cellule.
Ce que cela pourrait signifier pour les traitements futurs des cicatrices
Les résultats suggèrent que LIMK2 se situe à un carrefour où se rencontrent forces mécaniques, survie cellulaire et activité de formation de cicatrices. Quand LIMK2 est actif, l’étirement pousse les fibroblastes vers un état myofibroblastique robuste et persistant : ils contractent fortement, résistent à la mort et produisent du collagène en excès, favorisant des cicatrices épaisses et surélevées. Éteindre LIMK2 inverse une grande partie de ces effets — les fibroblastes deviennent moins contractiles, moins mobiles, moins prolifératifs et plus enclins à l’apoptose. Pour les patients, cela ouvre la perspective de crèmes, injections ou pansements qui bloqueraient doucement LIMK2 ou ses effets sur l’actine en aval, aidant les plaies à haut risque à guérir avec des cicatrices plus plates et plus confortables.
Citation: Ishii, M., Kuroda, K., Otani, N. et al. LIMK2 inactivation suppresses mechanical stimulation-induced dermal fibroblast differentiation and resistance to apoptosis. Sci Rep 16, 7453 (2026). https://doi.org/10.1038/s41598-026-37610-y
Mots-clés: cicatrices chéloïdes, guérison des plaies, fibroblastes, tension mécanique, apoptose