Clear Sky Science · fr
Ubiquitination de SMAD2 via le motif PY régule la masse musculaire squelettique et la dégénérescence fibreuse
Pourquoi cette étude sur le muscle est importante
En vieillissant, beaucoup d’entre nous constatent que leurs muscles s’affaiblissent et diminuent de volume, et en cas de maladie chronique ou de blessure le muscle peut être progressivement remplacé par du tissu cicatriciel rigide. Cette étude aborde une question fondamentale derrière ces changements : comment les cellules musculaires empêchent‑elles un signal puissant de contrôle de la croissance, appelé TGF‑bêta, d’aller trop loin et de provoquer perte musculaire et fibrose (cicatrisation) ? En dévoilant un minuscule « interrupteur » intégré dans une protéine clé de la voie TGF‑bêta, les auteurs révèlent un nouveau mécanisme qui contribue à préserver la masse musculaire et la structure tissulaire saine.
Un frein intégré sur un signal puissant
TGF‑bêta est une molécule de signalisation qui indique aux cellules quand ralentir la croissance, changer d’identité ou produire du tissu conjonctif. Dans le muscle squelettique, un excès de TGF‑bêta réduit le diamètre des fibres et favorise la fibrose ; à l’inverse, trop peu perturbe le contrôle normal de la croissance. À l’intérieur des cellules, TGF‑bêta agit principalement via une protéine relais appelée SMAD2. Après que TGF‑bêta se lie à ses récepteurs à la surface cellulaire, SMAD2 est activé et migre vers le noyau pour modifier l’activité des gènes. Pour éviter que cette activation ne devienne permanente, les cellules marquent chimiquement SMAD2 par de petites molécules d’ubiquitine, l’orientant vers l’élimination. Une courte séquence de SMAD2, connue sous le nom de motif PY, est le site d’ancrage des enzymes qui attachent ces étiquettes ubiquitine. Les chercheurs se sont demandé : si ce site d’ancrage est supprimé chez un animal vivant, le frein SMAD2 échoue‑t‑il, et que deviennent les muscles avec le temps ?
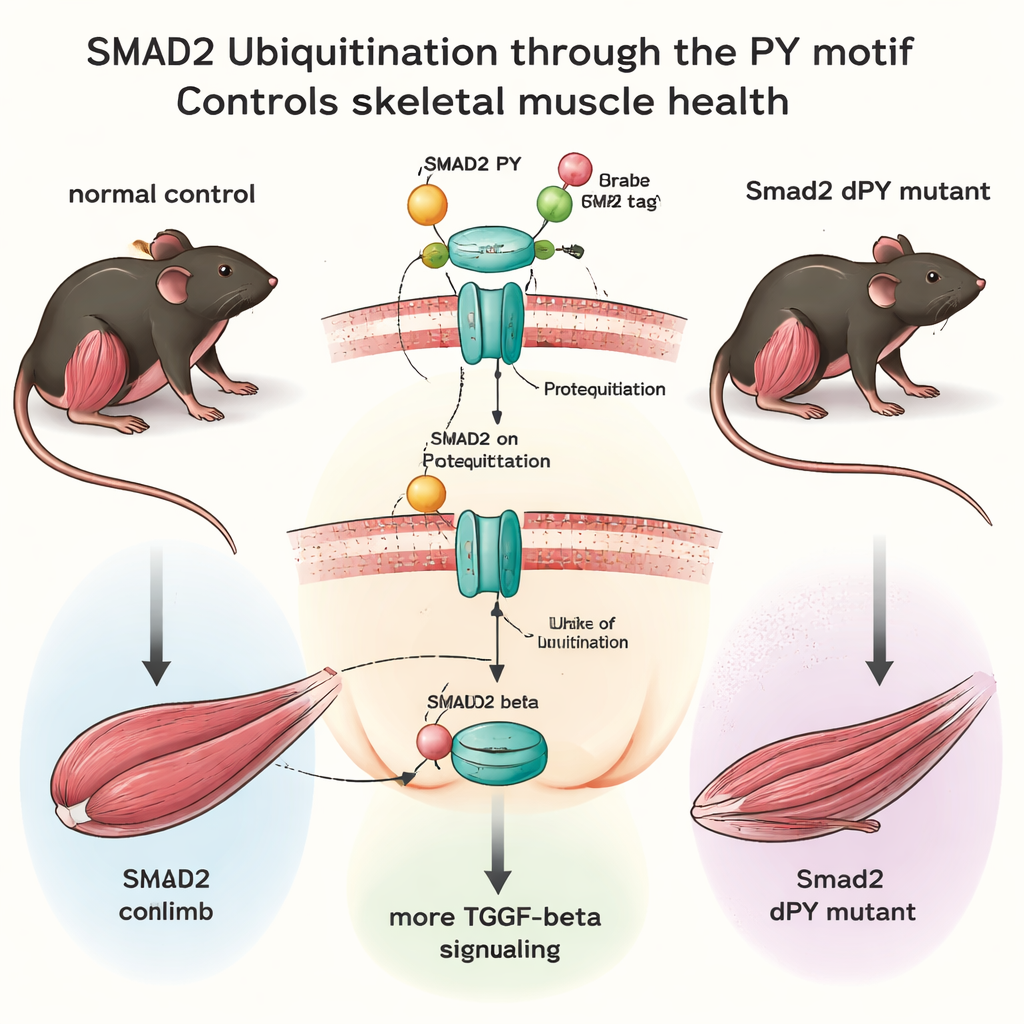
Des souris génétiquement modifiées sans étiquette de sécurité
À l’aide d’outils modernes d’édition du génome, l’équipe a créé des souris chez lesquelles seulement 15 « lettres » d’ADN ont été supprimées dans le gène Smad2, supprimant précisément le motif PY sans perturber le reste de la protéine. Ces souris Smad2dPY sont nées normalement, ont atteint l’âge adulte et étaient fertiles, montrant que ce réglage fin n’est pas essentiel au développement de base dans des conditions de laboratoire standard. Cependant, une analyse plus approfondie des muscles a révélé un autre tableau. Les jeunes adultes présentaient seulement des changements subtils, mais à 12 mois — soit l’équivalent d’un âge moyen chez la souris — les principaux muscles postérieurs pesaient moins et les fibres individuelles étaient plus petites comparées à leurs congénères normaux. Dans ces muscles, les niveaux de protéine SMAD2 étaient plus élevés, tandis que son ubiquitination était réduite, confirmant que l’absence du motif PY rendait SMAD2 plus stable et moins susceptible d’être dégradé.
Des cellules musculaires hyper‑sensibles et une réparation bloquée
Pour comprendre ce que cela signifiait au niveau cellulaire, les chercheurs ont isolé des précurseurs musculaires (myoblastes) des souris mutantes. Exposés à TGF‑bêta en culture, ces myoblastes montraient une activation plus forte de SMAD2 et une induction plus grande des gènes répondant à TGF‑bêta que les cellules provenant de souris normales. Parallèlement, leur capacité à fusionner en longues fibres musculaires multi‑nuclées — étape clé de la croissance et de la régénération musculaire — était altérée. Des changements similaires ont été observés dans les fibroblastes, les cellules du tissu conjonctif situées entre les fibres musculaires : les fibroblastes mutants répondaient plus fortement à TGF‑bêta et exprimaient plus facilement des gènes associés aux myofibroblastes producteurs de cicatrices. Ensemble, ces résultats suggèrent que sans le motif PY, à la fois les cellules formant le muscle et les cellules de soutien deviennent hypersensibles au TGF‑bêta, faisant pencher la balance vers des fibres plus petites et davantage de tissu fibreux.
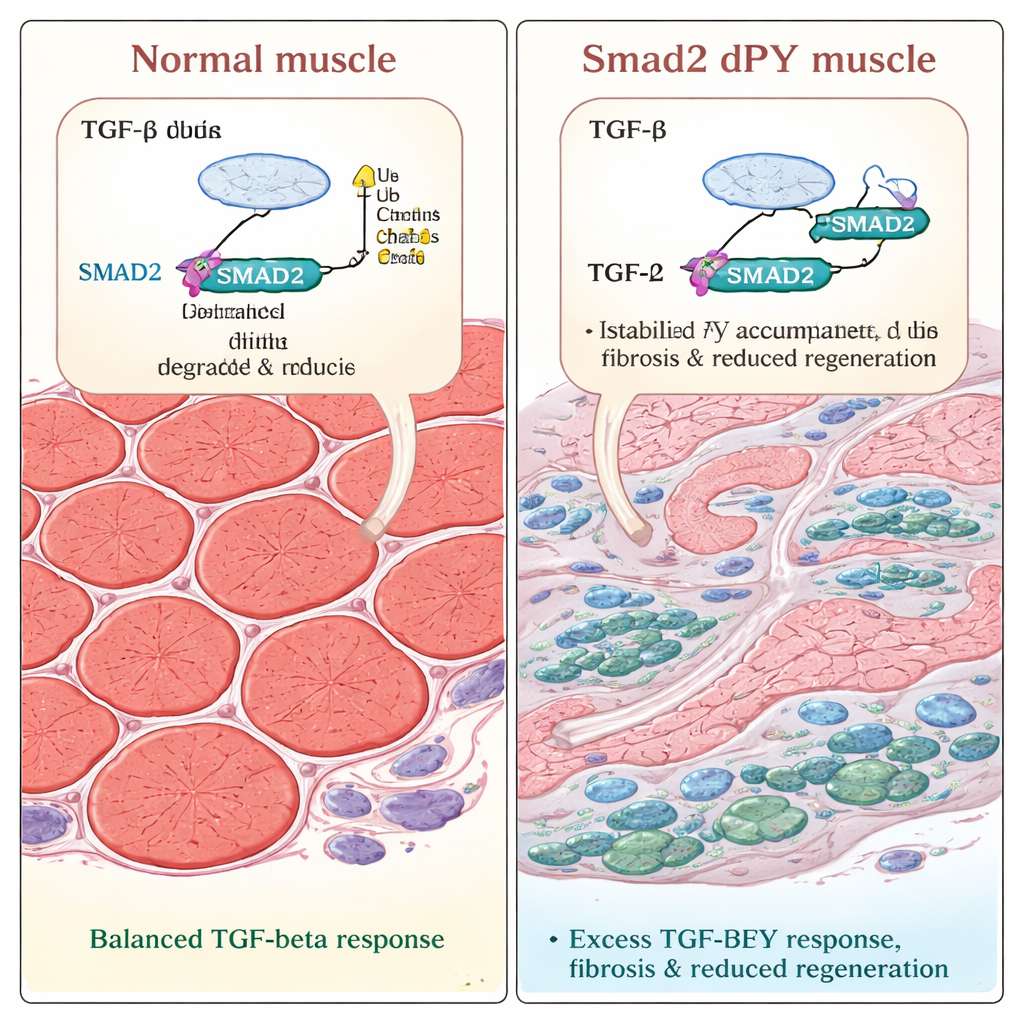
Quand la blessure survient, la cicatrisation l’emporte
L’équipe a ensuite testé comment ces muscles altérés faisaient face à une lésion. Ils ont injecté une toxine dans les muscles des pattes pour déclencher une blessure et une réparation, modèle bien établi de régénération. Chez les souris normales comme chez les mutants, les fibres endommagées se décomposaient d’abord puis commençaient à repousser. Mais trois semaines après la lésion, les fibres régénérées chez les Smad2dPY étaient visiblement plus fines. La microscopie montrait des zones plus étendues remplies de collagène, le principal constituant du tissu cicatriciel, et un nombre accru de myofibroblastes positifs pour l’alpha‑actine de muscle lisse, des cellules connues pour conduire la fibrose. Ces résultats montrent que lorsque SMAD2 ne peut pas être correctement étiqueté et renouvelé, le processus de réparation est déséquilibré : au lieu de reconstruire pleinement un muscle solide, le tissu guérit avec un excès de cicatrisation et une masse contractile réduite.
Ce que cela signifie pour la santé musculaire
Pour les non‑spécialistes, le message principal est qu’une toute petite caractéristique moléculaire — le motif PY sur SMAD2 — agit comme une garde silencieuse mais importante dans le muscle squelettique. Elle permet aux cellules d’atténuer la signalisation TGF‑bêta en favorisant l’élimination de SMAD2, contribuant ainsi au maintien d’une taille musculaire normale et à la limitation de la fibrose, en particulier lorsque les niveaux de TGF‑bêta augmentent naturellement avec l’âge ou en cas de blessure chronique. Lorsque ce système de sécurité est désactivé chez la souris, les muscles deviennent progressivement plus petits et plus susceptibles de cicatriser, et ils ne récupèrent pas complètement après une lésion. Bien que ces travaux aient été réalisés chez l’animal, ils mettent en lumière l’ubiquitination de SMAD2 comme une voie cible potentielle pour de futures stratégies visant à préserver la masse musculaire et à prévenir la dégénérescence fibreuse liée à l’âge ou à la maladie.
Citation: Yamasaki, Y., Sakamoto, K., Yashiro, S. et al. SMAD2 ubiquitination through PY motif regulates skeletal muscle mass and fibrotic degeneration. Sci Rep 16, 6666 (2026). https://doi.org/10.1038/s41598-026-37582-z
Mots-clés: muscle squelettique, signalisation TGF‑bêta, SMAD2, ubiquitination, fibrose