Clear Sky Science · fr
Modifications de l’activité d’EGFR après édition CRISPR/Cas9 du domaine de liaison à l’EGF
Pourquoi reconfigurer un signal cancéreux importe
Le cancer du col de l’utérus dépend souvent d’un puissant interrupteur de croissance appelé récepteur du facteur de croissance épidermique (EGFR). De nombreuses tumeurs présentent d’énormes quantités de ces récepteurs, pourtant les médicaments visant à les bloquer n’ont aidé qu’une fraction des patients. Cette étude pose une question fondamentale aux implications thérapeutiques majeures : que se passe‑t‑il si vous supprimez la capacité d’EGFR à capter son signal de croissance préféré, le facteur de croissance épidermique (EGF), sans retirer le récepteur lui‑même ?
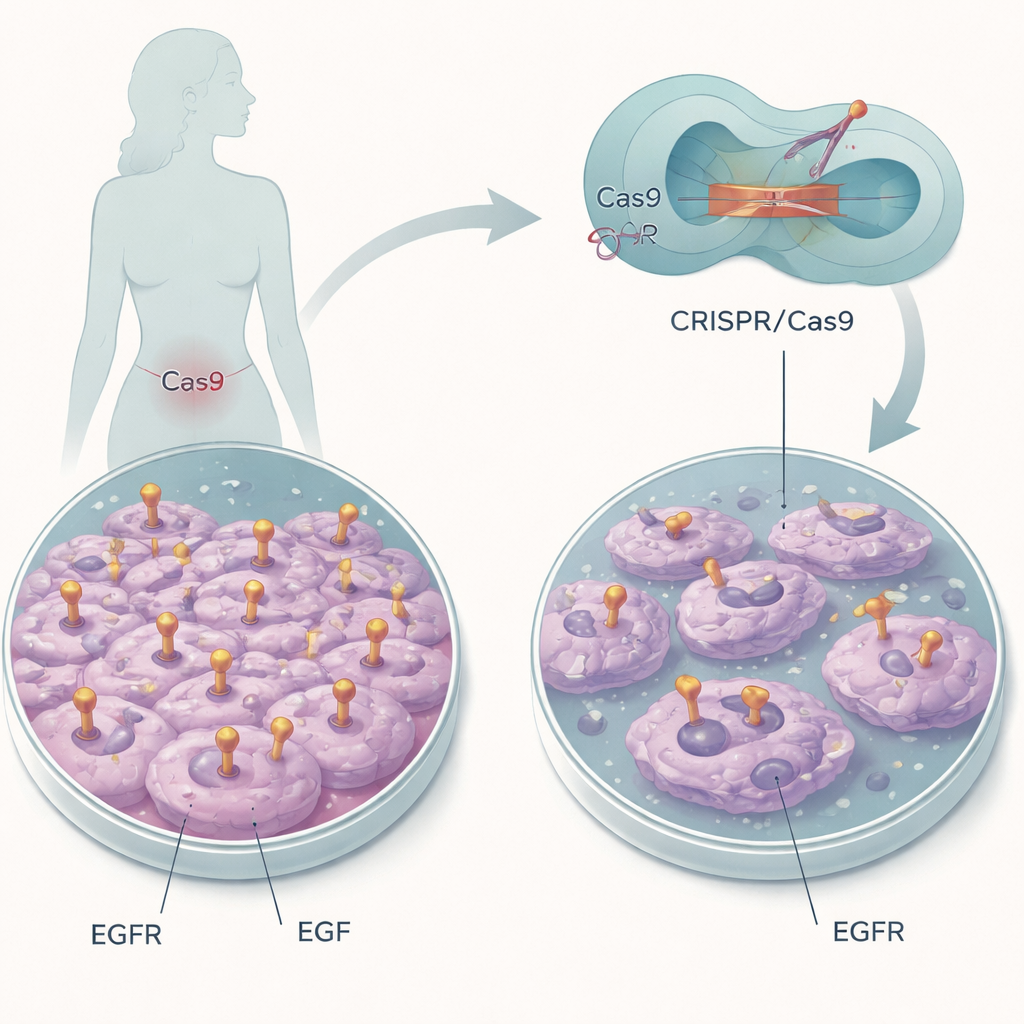
Éteindre un « interrupteur » moléculaire
Les chercheurs se sont concentrés sur une lignée cellulaire de cancer du col qui porte de grandes quantités d’EGFR par ailleurs normal. Plutôt que de détruire le gène, ils ont utilisé l’édition génomique CRISPR/Cas9 comme un scalpel moléculaire pour modifier seulement quelques acides aminés dans la poche de liaison à l’EGF d’EGFR. Deux positions particulières, appelées L14 et Y45, aident l’EGF à s’ancrer sur le récepteur. En substituant ces éléments constitutifs par d’autres, l’équipe a cherché à conserver la présence d’EGFR tout en le rendant aveugle à l’EGF, ce qui leur permettait d’isoler le rôle de cette interaction unique dans le comportement des cellules cancéreuses.
Construire des lignées cellulaires cancéreuses sur mesure
Dans un premier temps, l’équipe a testé ces mutations dans des cellules en utilisant des plasmides qui produisent de façon transitoire soit l’EGFR normal soit l’EGFR altéré. L’EGF marqué par fluorescence a révélé que toutes les formes mutants lient beaucoup moins de ligand que le récepteur normal, en particulier lorsque L14 et Y45 sont modifiés ensemble. Les chercheurs ont ensuite introduit ces changements directement dans le génome des cellules cancéreuses avec CRISPR/Cas9, générant plusieurs nouveaux clones cellulaires. Certains portaient une mutation unique, d’autres la double mutation sur une copie d’EGFR et des modifications inactivantes sur l’autre. La modélisation informatique des formes protéiques résultantes a montré que ces altérations déformaient le site de liaison suffisamment pour affaiblir ou abolir l’ancrage de l’EGF, en accord avec les tests de liaison.
Quand le récepteur se déplace mais que les cellules survivent
Des images détaillées ont révélé que les récepteurs modifiés se comportaient très différemment à l’intérieur de la cellule. Dans les cellules cancéreuses non modifiées, l’EGFR siège à la surface cellulaire, capture l’EGF, puis migre vers l’intérieur en devenant chimiquement activé par phosphorylation. Dans les clones portant la double mutation, la liaison de l’EGF a essentiellement disparu et l’EGFR n’était plus observé sur la membrane ; à la place, la faible quantité de récepteur restante s’accumulait à l’intérieur de la cellule. Même une seule modification Y45 réduisait considérablement la liaison et abaissait les niveaux globaux d’EGFR. Pourtant, malgré cette perturbation de la voie classique EGF–EGFR, les cellules cancéreuses restaient viables et continuaient de se développer en culture avec seulement des modifications modestes de leurs profils du cycle cellulaire.
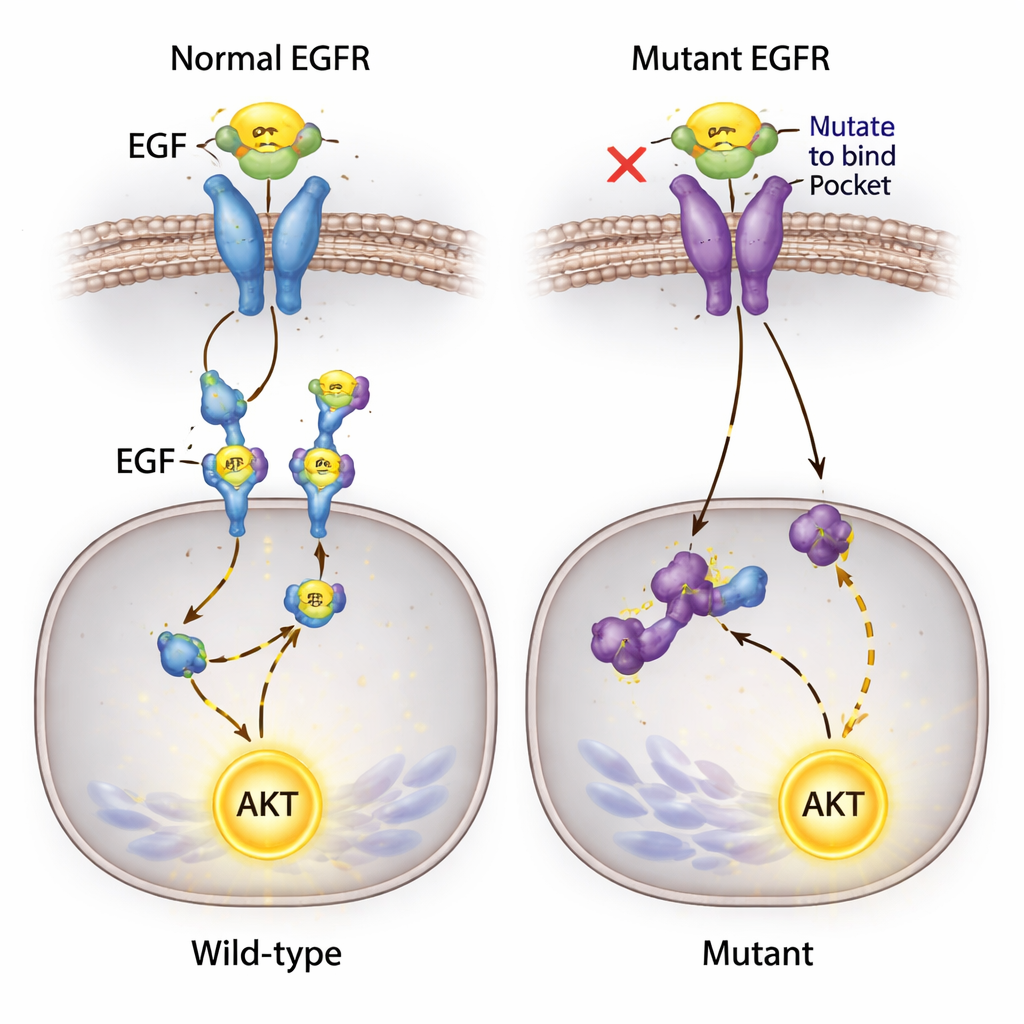
Un signal inattendu qui ne s’éteint pas
Une des découvertes les plus surprenantes concernait AKT, une protéine clé qui favorise la survie cellulaire et est habituellement activée en aval d’EGFR. Les chercheurs s’attendaient à ce que bloquer la liaison EGF–EGFR fasse taire cette voie. Au contraire, lorsque they ont ajouté de l’EGF au milieu, AKT s’est fortement activé dans toutes les lignées cellulaires — y compris celles où l’EGF ne pouvait plus se lier à EGFR et où la phosphorylation du récepteur était indétectable. Parce que ces cellules portent une mutation connue dans un autre gène de signalisation, PIK3CA, l’équipe suspecte que des routes alternatives peuvent permettre à l’EGF d’alimenter l’activation d’AKT, possiblement via d’autres protéines de surface ou des mutations de fond, contournant l’EGFR édité.
Modifications génétiques cachées et thérapies futures
Pour s’assurer que CRISPR ne provoquait pas d’éditions indésirables étendues, les scientifiques ont séquencé l’ensemble des génomes des nouvelles lignées cellulaires. Ils ont confirmé que les mutations souhaitées d’EGFR étaient présentes et n’ont trouvé aucune preuve de coupures aux sites hors cible prédits pour les guides CRISPR. Cependant, ils ont détecté de nombreuses mutations spontanées disséminées dans le génome, dont certaines pourraient influencer le comportement des cellules. Cela souligne que même lorsque CRISPR atteint sa cible prévue, l’instabilité intrinsèque de l’ADN des cellules cancéreuses peut compliquer l’interprétation des résultats expérimentaux et la conception de thérapies géniques précises.
Ce que cela signifie pour les patients
Pour le non‑spécialiste, le message à retenir est que bloquer simplement la poignée de main entre l’EGF et l’EGFR — même de manière très précise au niveau atomique — n’empêche pas automatiquement les cellules cancéreuses de recevoir des ordres de « croître et survivre ». L’étude montre que les cellules cancéreuses peuvent rediriger des signaux clés comme l’activation d’AKT autour d’un récepteur bloqué, et que l’édition CRISPR elle‑même doit être évaluée avec soin dans de tels génomes instables. Ces lignées cellulaires ingénierées fournissent désormais un modèle de laboratoire puissant pour rechercher les voies de secours qui soutiennent les tumeurs dépendantes d’EGFR, informations qui pourraient finalement conduire à des traitements combinés ciblant à la fois EGFR et ses complices cachés.
Citation: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Mots-clés: EGFR, cancer du col de l’utérus, CRISPR, signalisation EGF, voie AKT