Clear Sky Science · fr
L’amplification du nombre de copies entraîne la surexpression d’IFI30 et une activation immunitaire coordonnée, identifiant une nouvelle cible diagnostique et thérapeutique dans l’adénocarcinome gastrique
Pourquoi une protéine de l’estomac compte
Le cancer gastrique fait partie des cancers les plus mortels au monde, en grande partie parce qu’il est souvent détecté tard et difficile à traiter. Cette étude se concentre sur une protéine peu connue, IFI30, présente dans des cellules qui aident le système immunitaire à reconnaître les menaces. En retraçant comment IFI30 est altérée dans les tumeurs de l’estomac et comment elle façonne les défenses de l’organisme, les chercheurs suggèrent qu’elle pourrait devenir un outil puissant pour un diagnostic plus précoce et pour le choix de traitements personnalisés plus efficaces.
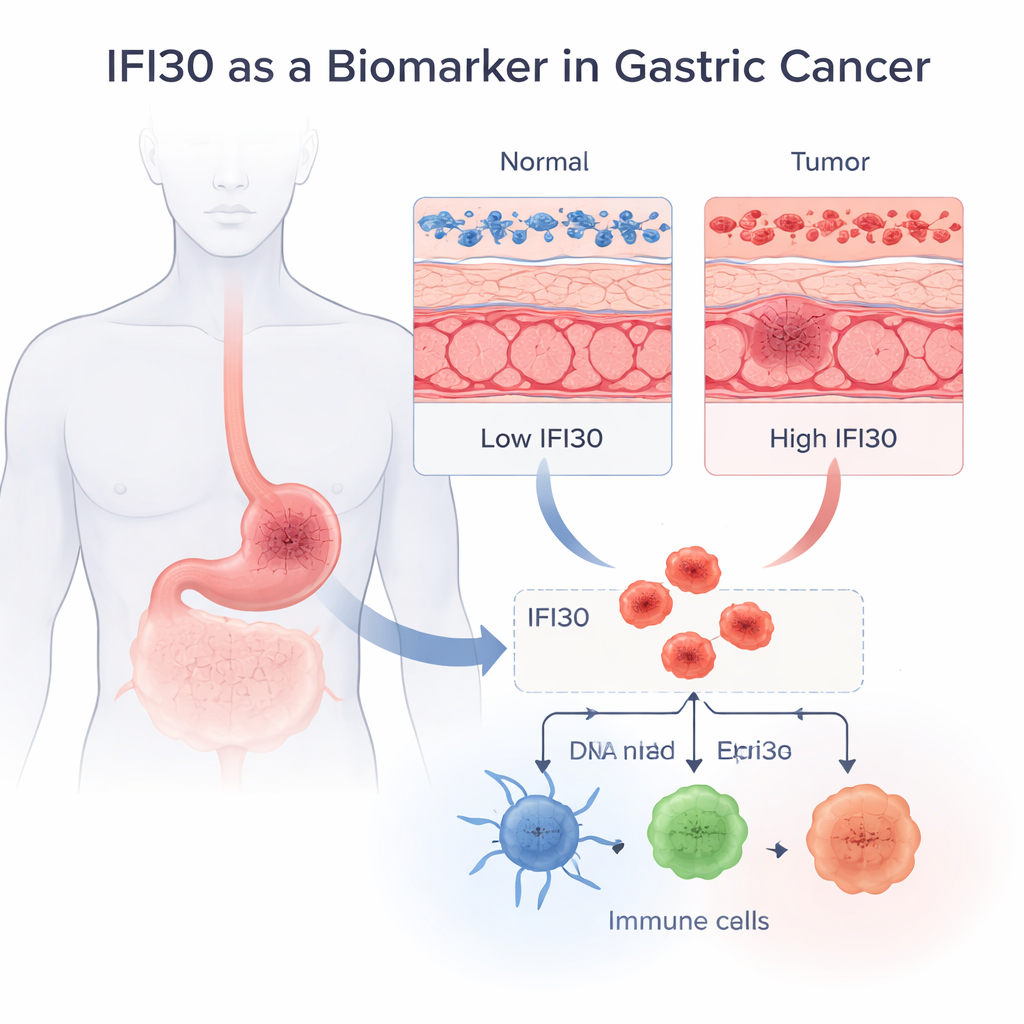
Un signal caché dans les tumeurs gastriques
L’équipe a commencé par poser une question simple : IFI30 est-elle présente à des niveaux différents dans les tissus gastriques sains par rapport aux tissus cancéreux ? En utilisant de larges jeux de données publics regroupant l’activité génique de milliers d’échantillons, ils ont constaté qu’IFI30 est systématiquement beaucoup plus exprimée dans l’adénocarcinome gastrique — le type de cancer de l’estomac le plus courant — que dans la muqueuse gastrique normale. Cela était vrai dans plusieurs cohortes indépendantes et aux niveaux de l’ARN comme de la protéine. Lorsque les auteurs ont testé la capacité d’IFI30 seule à distinguer tissu tumoral et tissu sain, la performance était remarquable : une précision diagnostique (AUC) de 0,92, considérée excellente pour un marqueur unique. Des images microscopiques ont également localisé IFI30 au sein du système de recyclage intracellulaire, où les antigènes sont traités pour la reconnaissance immunitaire.
Des modifications de l’ADN qui suractivent IFI30
Ensuite, les chercheurs ont cherché pourquoi IFI30 est si élevée dans ces tumeurs. En analysant les génomes tumoraux du Cancer Genome Atlas, ils ont découvert que des copies supplémentaires du gène IFI30 — connues sous le nom d’amplifications du nombre de copies — étaient le principal moteur de sa surexpression. Les tumeurs avec amplification d’IFI30 montraient généralement une plus grande instabilité du génome global et portaient souvent des mutations cancéreuses bien connues, telles que TP53 et PIK3CA. À mesure que le nombre de copies d’IFI30 augmentait, ses niveaux d’ARN augmentaient aussi, laissant penser à un lien direct entre ces altérations structurelles de l’ADN et la production accrue de cette protéine. Cela présente IFI30 non pas comme un simple spectateur, mais comme partie intégrante d’un profil biologique tumoral agressif.
Interrelations immunitaires autour de la tumeur
Parce qu’IFI30 participe au traitement du matériel que les cellules immunitaires présentent comme des « affiches » aux lymphocytes T, l’équipe a exploré sa localisation précise dans le microenvironnement tumoral. Le séquençage unicellulaire, qui lit l’expression génique cellule par cellule, a montré qu’IFI30 est particulièrement enrichie dans les cellules dendritiques, les macrophages et les lymphocytes T CD8 — acteurs clés du déclenchement et du maintien de l’immunité anti-tumorale. Des analyses de réseaux ont révélé une communication dense entre les cellules immunitaires riches en IFI30 et les cellules tumorales et stromales environnantes. Les tumeurs à haute expression d’IFI30 présentaient une forte activation des voies liées à la présentation d’antigènes, aux signaux inflammatoires et aux molécules de communication qui attirent et organisent les cellules immunitaires. Parallèlement, ces tumeurs affichaient des traits d’invasion et de stress, tels que l’accélération du cycle cellulaire, le remodelage tissulaire et l’adaptation à l’hypoxie, soulignant le rôle d’IFI30 à l’intersection de l’attaque et de la défense au sein du cancer.
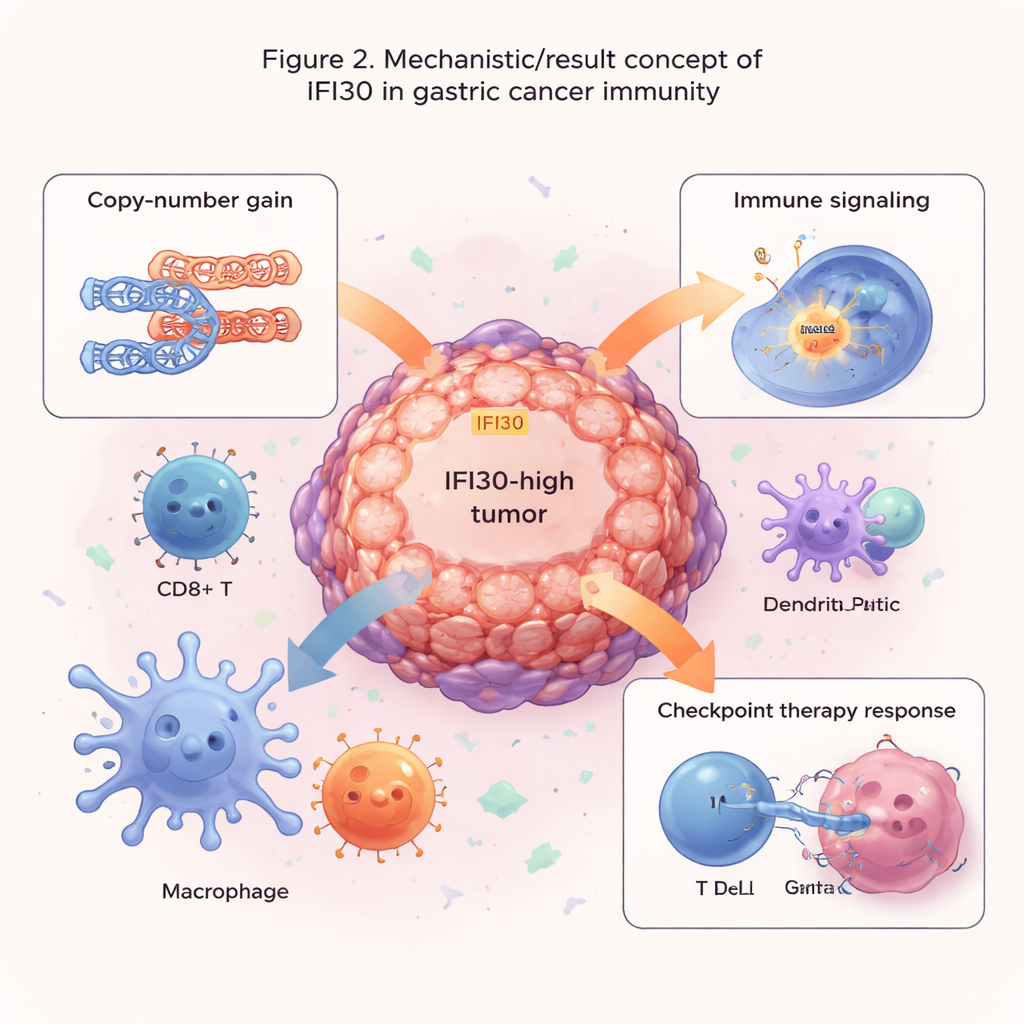
Indices pour le choix des médicaments et l’immunothérapie
Les auteurs ont ensuite demandé si IFI30 pouvait aider à prédire la réponse des tumeurs aux traitements. En mettant en regard les niveaux d’IFI30 avec de larges jeux de données de réponses aux médicaments, ils ont trouvé que les tumeurs riches en IFI30 tendent à résister à certains médicaments ciblant la division cellulaire ou une voie de croissance courante (MAPK), mais semblent plus sensibles aux agents bloquant la signalisation EGFR et PI3K/AKT. Fait notable, les niveaux d’IFI30 suivaient de près ceux de PD-L1, un frein majeur des lymphocytes T ciblé par les inhibiteurs de point de contrôle actuels. Dans plusieurs études d’immunothérapie, les patients dont les tumeurs exprimaient davantage IFI30 étaient plus susceptibles de répondre au blocage des points de contrôle que ceux ayant de faibles niveaux. Un score basé sur IFI30 surpassait des mesures établies telles que la charge mutationnelle tumorale et PD-L1 seul, et était particulièrement enrichi dans les tumeurs à instabilité microsatellite élevée, un sous-groupe déjà connu pour mieux répondre à l’immunothérapie.
Du banc de laboratoire à une cible potentielle
Pour tester si IFI30 n’est qu’un marqueur ou contribue aussi à la croissance tumorale, l’équipe a réduit son expression dans des lignées de cancer gastrique à l’aide d’outils génétiques. Quand IFI30 était inhibée, les cellules cancéreuses proliféraient plus lentement, ce qui indique un rôle direct dans le maintien de la croissance tumorale. Dans l’ensemble, les données suggèrent qu’IFI30 est à la fois un reflet de l’activité immunitaire et un contributeur au comportement malin. Pour les patients, cela signifie qu’une mesure simple d’IFI30 pourrait un jour aider les médecins à détecter le cancer gastrique de manière plus fiable, prédire qui pourrait bénéficier de certains médicaments ciblés ou d’immunothérapies, et éventuellement orienter de nouveaux traitements visant directement ou indirectement à bloquer les actions pro-tumorales d’IFI30.
Citation: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Mots-clés: cancer gastrique, IFI30, biomarqueur, immunité tumorale, immunothérapie