Clear Sky Science · fr
Analyse computationnelle des hydrures X2CaZnH6 (X = K, Rb et Cs) pour le stockage de l’hydrogène
L’hydrogène dans une boîte
L’hydrogène est souvent présenté comme le carburant propre du futur, mais le stocker de manière sûre et compacte reste un obstacle majeur. Cette étude explore une nouvelle famille de matériaux cristallins capables de retenir l’hydrogène au sein de leur réseau atomique, un peu comme l’eau dans une éponge. En concevant ces composés par calcul avant qu’ils ne soient synthétisés en laboratoire, les auteurs montrent comment ils pourraient servir de carburants solides pour des technologies hydrogène du futur.
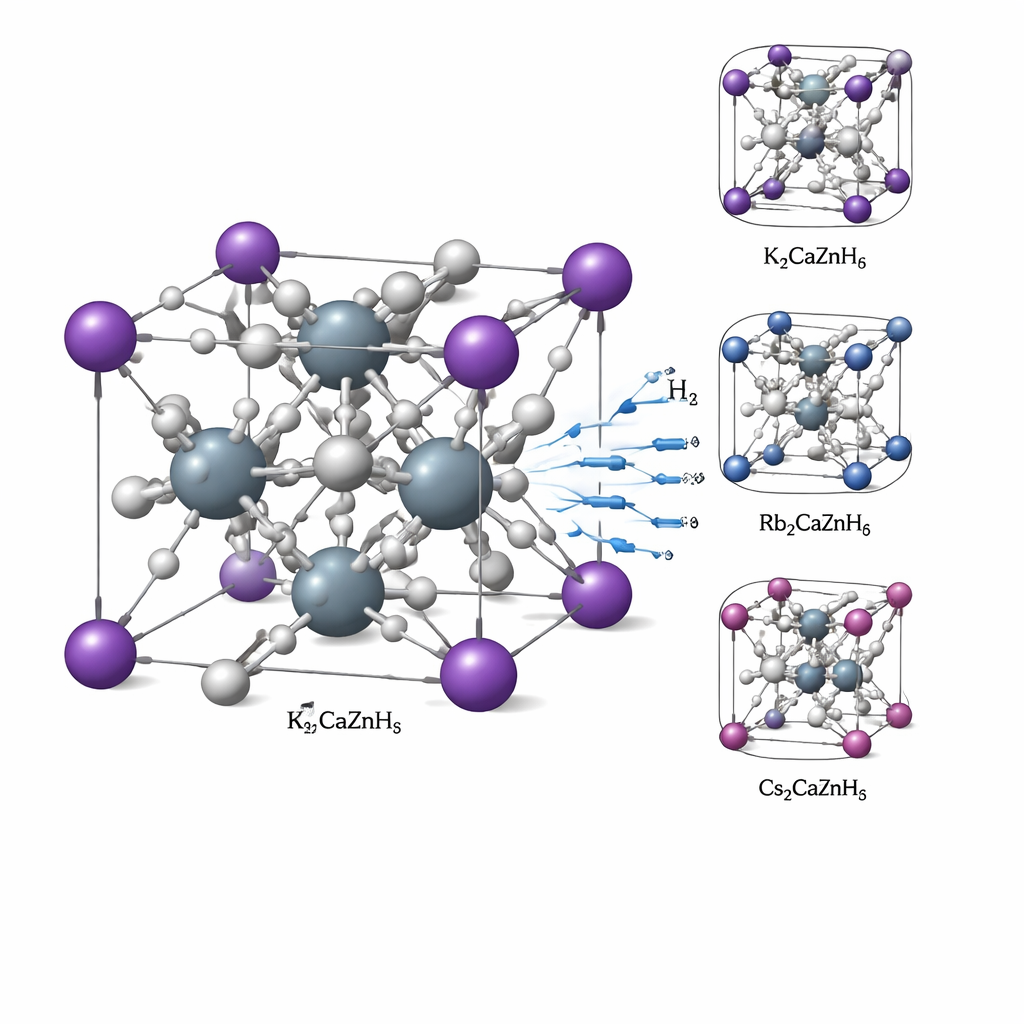
Un cristal construit comme un réseau 3D
Les matériaux étudiés sont des hydrures à double pérovskite, de formule X2CaZnH6, où X peut être le potassium (K), le rubidium (Rb) ou le césium (Cs). Les trois forment une structure simple en forme de cube dans laquelle des atomes lourds occupent des positions bien définies et les atomes d’hydrogène prennent place autour d’eux. À l’aide de calculs quantiques, les auteurs confirment que ces cristaux sont structurellement stables : les atomes s’emboîtent avec des tailles appropriées, l’énergie globale du matériau est suffisamment basse pour qu’il puisse se former naturellement, et les vibrations atomiques ne suggèrent pas d’instabilités cachées. Des essais mécaniques réalisés in silico montrent que les cristaux sont rigides sans être excessivement fragiles, un équilibre qui leur permet de conserver leur forme tout en autorisant de petites réarrangements lors de l’absorption ou de la libération d’hydrogène.
Quelle quantité d’hydrogène peuvent-ils contenir ?
Pour tout matériau de stockage, deux chiffres-clés sont la capacité massique (combien d’hydrogène par poids) et la capacité volumique (par volume), ainsi que la température à laquelle l’hydrogène peut être libéré. Les trois composés étudiés stockent entre environ 1,6 et 3,2 % de leur masse sous forme d’hydrogène, et environ 15 à 18 kilogrammes d’hydrogène par mètre cube de matériau. La version à base de potassium, K2CaZnH6, contient le plus d’hydrogène mais nécessite des températures plus élevées (environ 658 K, soit 385 °C) pour le libérer. La version au césium stocke légèrement moins d’hydrogène et requiert également des températures assez élevées. Le composé au rubidium, Rb2CaZnH6, se distingue : il libère l’hydrogène à environ 385 K (environ 110 °C), une plage bien plus proche de ce qui est pratique pour des dispositifs réels, tout en conservant une densité de stockage respectable.
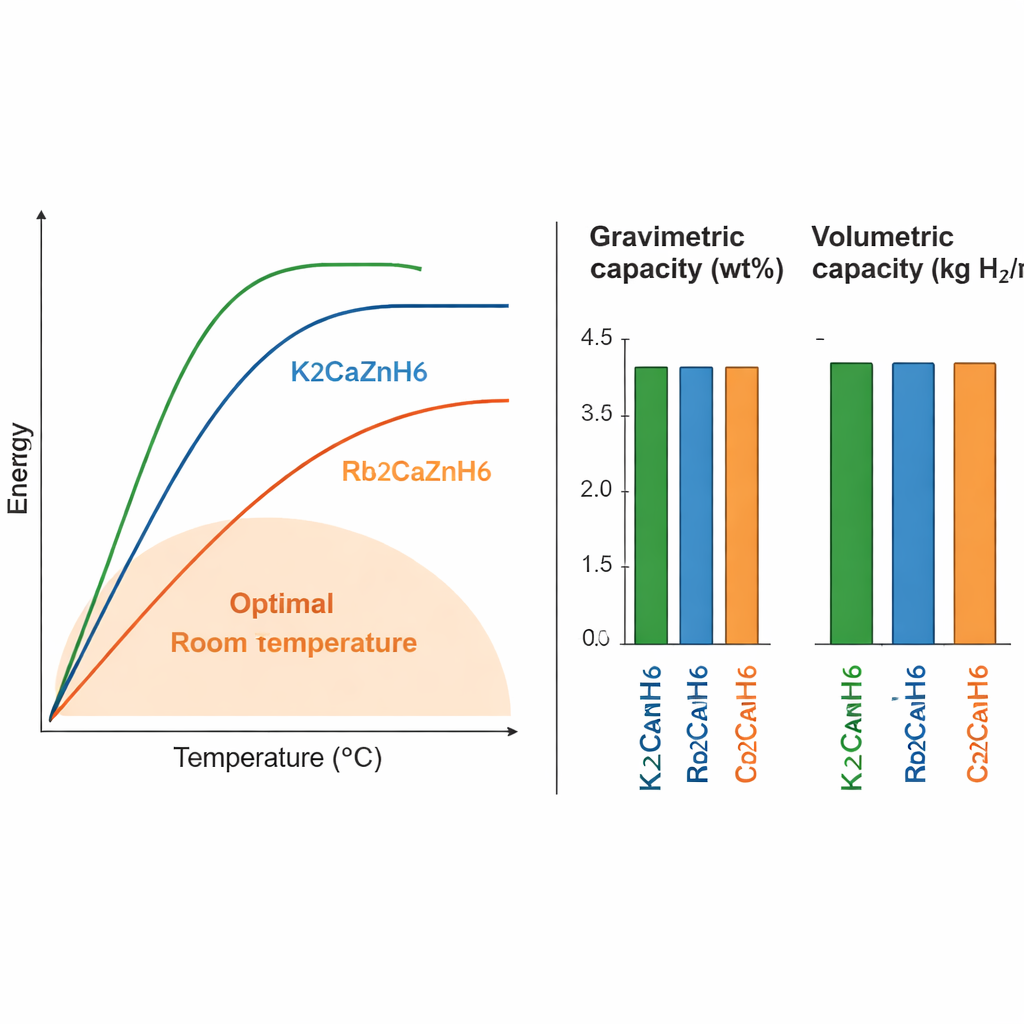
Pourquoi les atomes et les électrons comptent
Pour comprendre le comportement de ces matériaux, les auteurs examinent comment les électrons sont partagés entre les atomes et comment cela affecte la liaison chimique. Dans les trois composés, le potassium, le rubidium ou le césium jouent le rôle de donneurs d’électrons, tandis que le zinc, le calcium et l’hydrogène attirent des électrons. Les atomes d’hydrogène acquièrent une charge partiellement négative, et leurs liaisons au calcium et au zinc sont essentiellement ioniques avec une part de caractère covalent. Ce type de liaison a tendance à retenir l’hydrogène suffisamment fermement pour éviter les fuites, tout en étant assez faible pour que le chauffage puisse le libérer quand nécessaire. Fait important, les atomes d’hydrogène ne forment pas de liaisons H–H fortes à l’intérieur du cristal, ce qui signifie que l’hydrogène est stocké sous forme d’atomes séparés plutôt que de molécules préformées, ce qui est favorable à une libération contrôlée.
Lumière, électricité et résistance
Ces cristaux sont également des semi-conducteurs, avec une ouverture d’énergie modeste entre les états électroniques remplis et vides. Cela signifie qu’ils peuvent interagir avec la lumière sur une large gamme de longueurs d’onde, en particulier dans les parties visible et ultraviolette du spectre. Les calculs montrent une forte absorption lumineuse et une conductivité optique significative, ouvrant la possibilité que la lumière aide à déclencher la libération d’hydrogène, une sorte de stockage assisté par le solaire. Parallèlement, les matériaux satisfont aux critères usuels de stabilité mécanique : ils résistent à la compression, au cisaillement et à la rupture dans des limites raisonnables, et leurs vibrations atomiques à température ambiante restent bien comportées dans des tests de chauffage simulés. Ensemble, ces caractéristiques indiquent un réseau robuste capable de supporter des cycles répétés de chargement et de déchargement d’hydrogène.
Que signifie cela pour les systèmes énergétiques du futur
En termes concrets, l’étude identifie trois nouveaux matériaux « éponges à hydrogène » qui sont stables, suffisamment résistants et capables de concentrer l’hydrogène dans un solide compact. Bien que leur teneur en hydrogène en pourcentage massique ne réponde pas encore aux objectifs les plus ambitieux, leur stockage volumique est prometteur, et le composé à base de rubidium fonctionne à des températures compatibles avec de nombreux systèmes pratiques. Parce que leur comportement peut être ajusté simplement en remplaçant un élément alcalin par un autre, ces hydrures à double pérovskite offrent une plateforme flexible pour concevoir de meilleurs carburants solides à l’hydrogène, et potentiellement pour combiner le stockage avec un contrôle induit par la lumière dans de futures technologies d’énergie propre.
Citation: Al-Zoubi, N., Almahmoud, A., Almahmoud, A. et al. Computational analysis of X2CaZnH6 (X = K, Rb and Cs) hydrides for hydrogen storage. Sci Rep 16, 6889 (2026). https://doi.org/10.1038/s41598-026-37564-1
Mots-clés: stockage d’hydrogène, hydrures métalliques, double pérovskite, énergie à l’état solide, carburants propres