Clear Sky Science · fr
Prévalence et génotypage de Pseudomonas aeruginosa provenant d’aliments et de sources humaines
Pourquoi un germe courant importe dans la vie quotidienne
Pseudomonas aeruginosa est difficile à prononcer, mais c’est un germe qui peut discrètement passer de l’eau et des aliments crus aux hôpitaux et aux personnes, provoquant parfois des infections graves difficiles à traiter. Cette étude, réalisée dans une ville égyptienne, a suivi les lieux où cette bactérie apparaît dans des éléments du quotidien comme l’eau du robinet, le poisson, la viande et le lait, ainsi que dans des infections de plaies chez des patients. Elle a aussi examiné sa résistance aux antibiotiques et la présence de « outils » génétiques qui la rendent plus dangereuse. Les résultats aident à comprendre pourquoi l’hygiène alimentaire, l’eau propre et l’usage prudent des antibiotiques sont liés pour protéger la santé publique.
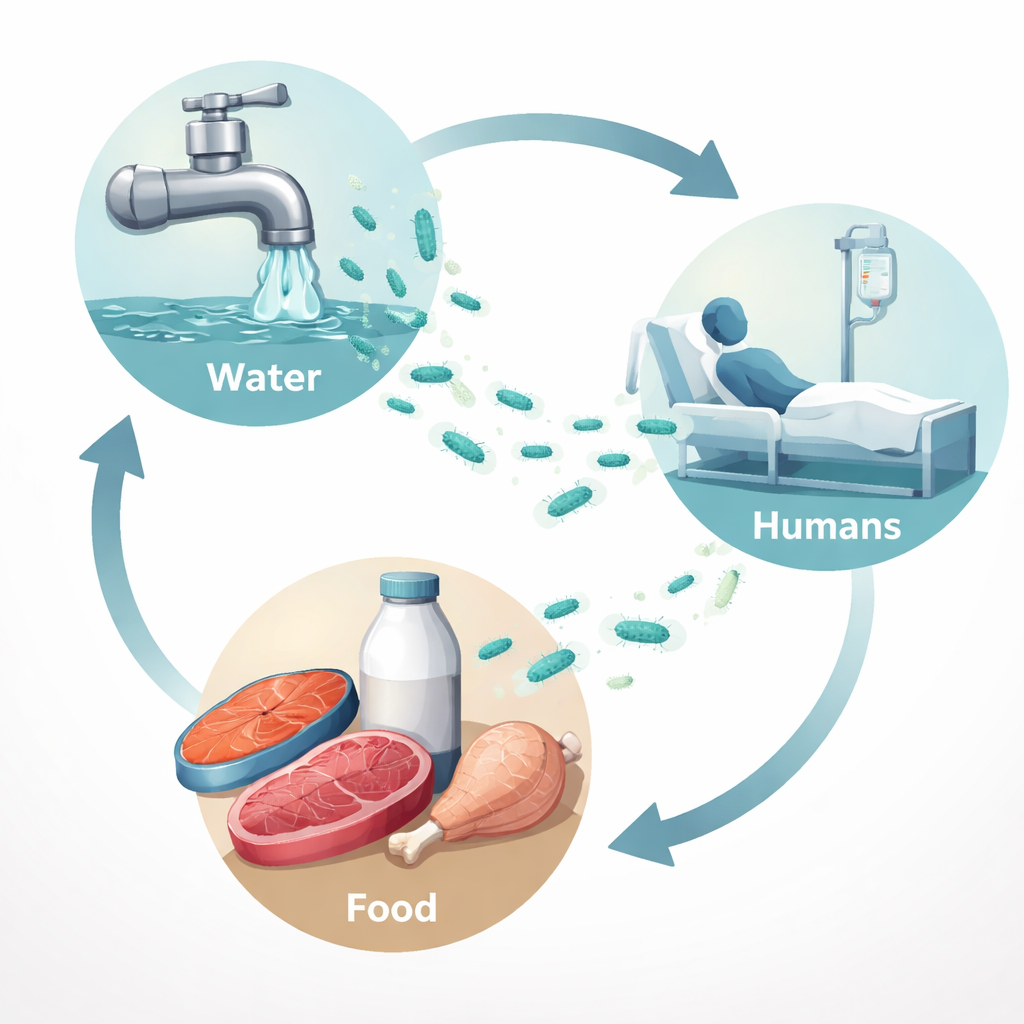
Suivre le germe du marché à l’hôpital
Les chercheurs ont collecté 350 échantillons autour de la ville de Sadat, dans le gouvernorat de Menoufia, en Égypte. Ceux‑ci comprenaient du pus humain provenant de plaies infectées, de l’eau du robinet, des écouvillons de poisson, de la viande de poulet, de la viande hachée, du lait cru et des surfaces hospitalières. Ils recherchaient spécifiquement P. aeruginosa. Au total, la bactérie a été trouvée dans environ un échantillon sur sept. Elle apparaissait le plus souvent dans les prélèvements de plaies humaines (environ un sur quatre), mais était également présente dans l’eau du robinet, le poisson et le lait cru, et dans une moindre mesure dans le poulet et la viande hachée. Fait intéressant, aucun des écouvillons de surfaces hospitalières n’a été positif, ce qui suggère que, dans ce contexte, la menace principale pourrait provenir des aliments et de l’eau entrant à l’hôpital plutôt que des comptoirs et équipements contaminés.
À quel point ces bactéries sont‑elles dangereuses ?
Trouver le germe ne suffit pas ; son comportement compte tout autant. L’équipe a testé chaque isolat bactérien avec des méthodes de laboratoire standard pour savoir s’il pouvait former une couche protectrice visqueuse appelée biofilm. Environ un tiers des isolats le faisaient, certains formant des couches épaisses et robustes. Les biofilms rendent les bactéries beaucoup plus difficiles à éliminer car ils protègent les cellules contre les agents de nettoyage et les antibiotiques. Les tests génétiques sur les souches formant des biofilms ont montré qu’elles portaient plusieurs gènes de « virulence », qui codent des protéines endommageant les tissus hôtes ou aidant les bactéries à adhérer aux surfaces et à échapper au système immunitaire. En termes simples, beaucoup des souches détectées n’étaient pas seulement présentes : elles étaient bien équipées pour causer des maladies.
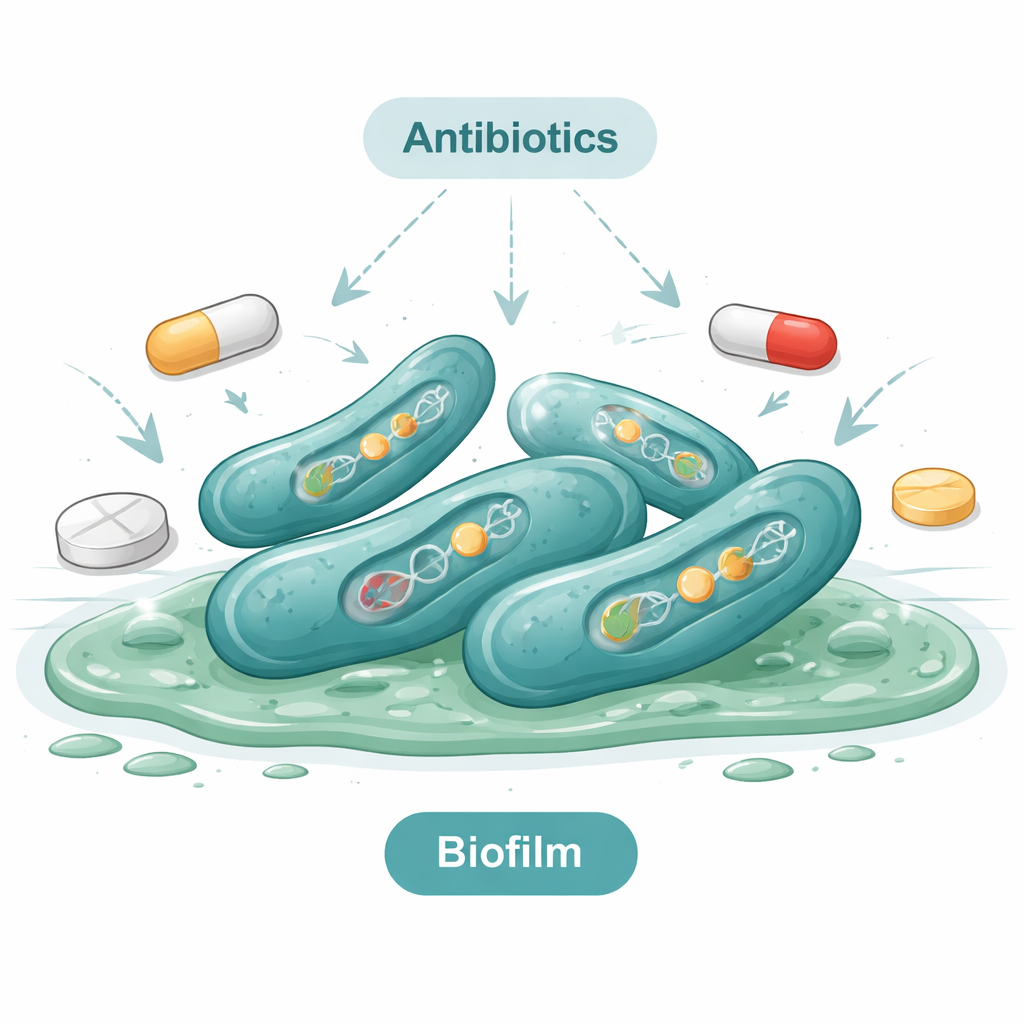
Antibiotiques inefficaces — et quelques‑uns qui fonctionnent encore
L’étude s’est ensuite penchée sur une question cruciale : quels antibiotiques restent efficaces contre ces souches ? Lorsqu’ils ont exposé 50 isolats à 16 médicaments différents, les chercheurs ont constaté que nombre d’antibiotiques courants étaient presque inefficaces. Tous les isolats résistaient à l’amoxicilline, et presque tous résistaient à l’érythromycine et à plusieurs autres agents plus anciens. La plupart restaient également insensibles au colistine, un antibiotique souvent réservé en dernier recours. Plus positivement, quelques antibiotiques — dont l’imipénème et certains médicaments apparentés — demeuraient efficaces contre de nombreux isolats. Malgré tout, plus de quatre souches sur cinq étaient résistantes à plusieurs classes d’antibiotiques simultanément, une situation connue sous le nom de multirésistance. Les tests génétiques confirmaient cela : les bactéries portaient des gènes de résistance qui leur permettent d’inactiver les antibiotiques ou de les expulser de leurs cellules.
Lier aliments, eau et infections humaines
Pour explorer les liens entre les souches selon les sources, l’équipe a utilisé une méthode de « profilage » de l’ADN appelée ERIC‑PCR sur un sous‑ensemble d’isolats cliniques. Cette technique regroupe les bactéries selon des motifs répétés dans leur génome. L’analyse a réparti les souches en grappes contenant des échantillons à la fois humains et alimentaires, comme le poisson, le lait, le poulet et la viande hachée. Ce schéma suggère que les aliments et l’eau peuvent servir de tremplins, permettant à des souches similaires de P. aeruginosa de circuler entre l’environnement et les patients. Concrètement, la bactérie détectée dans un morceau de poisson cru au marché peut être étroitement apparentée à celle qui cause une infection de plaie dans un hôpital voisin.
Ce que cela implique pour la santé quotidienne
Pour le grand public, le message est simple : un germe environnemental courant trouve son chemin de l’eau et des aliments d’origine animale vers les personnes, et plusieurs de ses souches sont dotées de gènes qui les rendent résistantes, tenaces et dangereuses. Parce qu’un grand nombre d’isolats résistent à plusieurs antibiotiques, le traitement des infections devient plus compliqué, coûteux et risqué. Les auteurs préconisent une meilleure hygiène dans la production et la manipulation des aliments, des systèmes d’eau plus sûrs et un usage plus prudent des antibiotiques chez l’homme et chez les animaux afin de ralentir la propagation de ces souches robustes. Ils appellent également à une surveillance continue et à des études génétiques plus détaillées pour cartographier la manière dont P. aeruginosa circule dans la chaîne alimentaire et entre dans les hôpitaux, afin de mieux prédire et prévenir de futures épidémies.
Citation: Mousa, W.S., Abdeen, E.E., El-Gendy, H.F. et al. Prevalence and genotyping of Pseudomonas aeruginosa from food and human sources. Sci Rep 16, 7179 (2026). https://doi.org/10.1038/s41598-026-37559-y
Mots-clés: Pseudomonas aeruginosa, bactéries d’origine alimentaire, résistance aux antibiotiques, biofilm, contamination de l’eau