Clear Sky Science · fr
Cadre inédit d’apprentissage profond hybride pour la classification de la maladie de Parkinson
Pourquoi cela compte pour les patients et les familles
La maladie de Parkinson débute souvent par des changements discrets — mouvements ralentis, voix plus faible ou tremblement léger — qui peuvent facilement être interprétés comme des effets normaux du vieillissement. Au moment où le diagnostic est certain, une grande partie des lésions cérébrales est déjà installée. Cette étude présente une approche informatique qui analyse les images cérébrales pour détecter la maladie de Parkinson avec une très grande précision, même lorsque les signes restent ténus. Si de tels outils sont fiables et largement adoptés, ils pourraient aider les médecins à diagnostiquer plus tôt, à traiter plus rapidement et à donner aux patients et à leurs proches davantage de temps pour s’organiser.
Explorer le cerveau avec des scans intelligents
Les chercheurs se sont concentrés sur l’imagerie par résonance magnétique (IRM), un examen déjà courant dans les hôpitaux et sans rayonnement. Ils ont utilisé une grande collection publique d’images cérébrales issue de la Parkinson’s Progression Markers Initiative, qui comprend des scans de personnes atteintes de la maladie de Parkinson et de volontaires sains. Plutôt que d’analyser l’ensemble du volume 3D d’un coup, l’équipe a travaillé sur des vues slice par slice à travers le cerveau, en particulier la région du mésencéphale où se trouvent les cellules productrices de dopamine. Ces cellules sont cruciales pour la fluidité du mouvement, et leur perte est une caractéristique de la maladie de Parkinson. Pour rendre les structures faibles plus faciles à “voir” par un ordinateur, les images ont d’abord subi des ajustements soignés qui standardisent la luminosité et améliorent le contraste dans les zones clés.
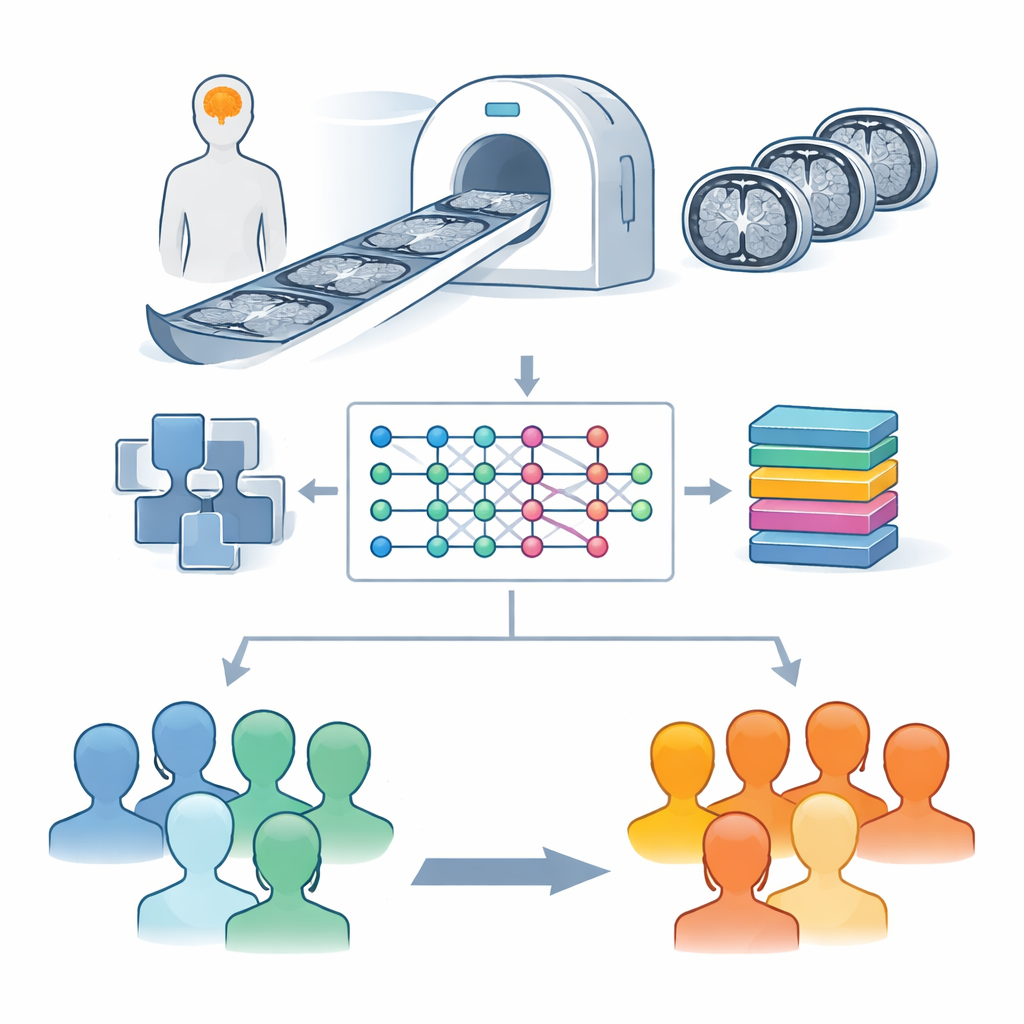
Apprendre à un modèle hybride à repérer des motifs
Le cœur de l’étude est un système hybride qui combine deux idées puissantes de l’informatique moderne. La première est un réseau d’apprentissage profond appelé EfficientNetB0, conçu à l’origine pour des tâches générales de reconnaissance d’images. Ici, il joue le rôle d’un œil très entraîné, parcourant chaque coupe cérébrale pour extraire des motifs subtils de forme et de texture susceptibles de distinguer les cerveaux sains de ceux affectés par la maladie de Parkinson. La seconde est une méthode de prise de décision connue sous le nom de XGBoost, qui excelle à tracer des frontières nettes entre catégories une fois qu’on lui fournit des caractéristiques informatives. En termes simples, EfficientNetB0 condense chaque coupe IRM en une signature compacte, et XGBoost utilise ces signatures pour décider si le scan appartient à une personne saine ou à une personne atteinte de Parkinson, et pour identifier le type d’acquisition IRM.
Équilibrer des données limitées et inégales
Un des principaux problèmes pratiques en IA médicale est que les données sont souvent à la fois rares et déséquilibrées : il peut y avoir beaucoup plus de scans de patients que de volontaires sains, ou l’inverse. Ici, l’équipe a démarré avec des scans de 77 sujets sains et 223 sujets atteints de Parkinson, un effectif modeste pour l’apprentissage profond. Pour éviter d’enseigner au système des leçons biaisées, ils ont étendu l’ensemble d’images de manière contrôlée. Chaque coupe cérébrale d’origine a été tournée ou retournée pour imiter les petites différences de position de la tête qui se produisent lors des scanners réels. Ils ont également appliqué une technique d’amélioration du contraste appelée CLAHE, qui éclaire les détails fins sans exagérer le bruit. Cet “étirement” soigneux du jeu de données a produit plus de 26 000 images, donnant au modèle suffisamment de variété pour apprendre des motifs robustes tout en réduisant le risque de surapprentissage sur des particularités des scans initiaux.
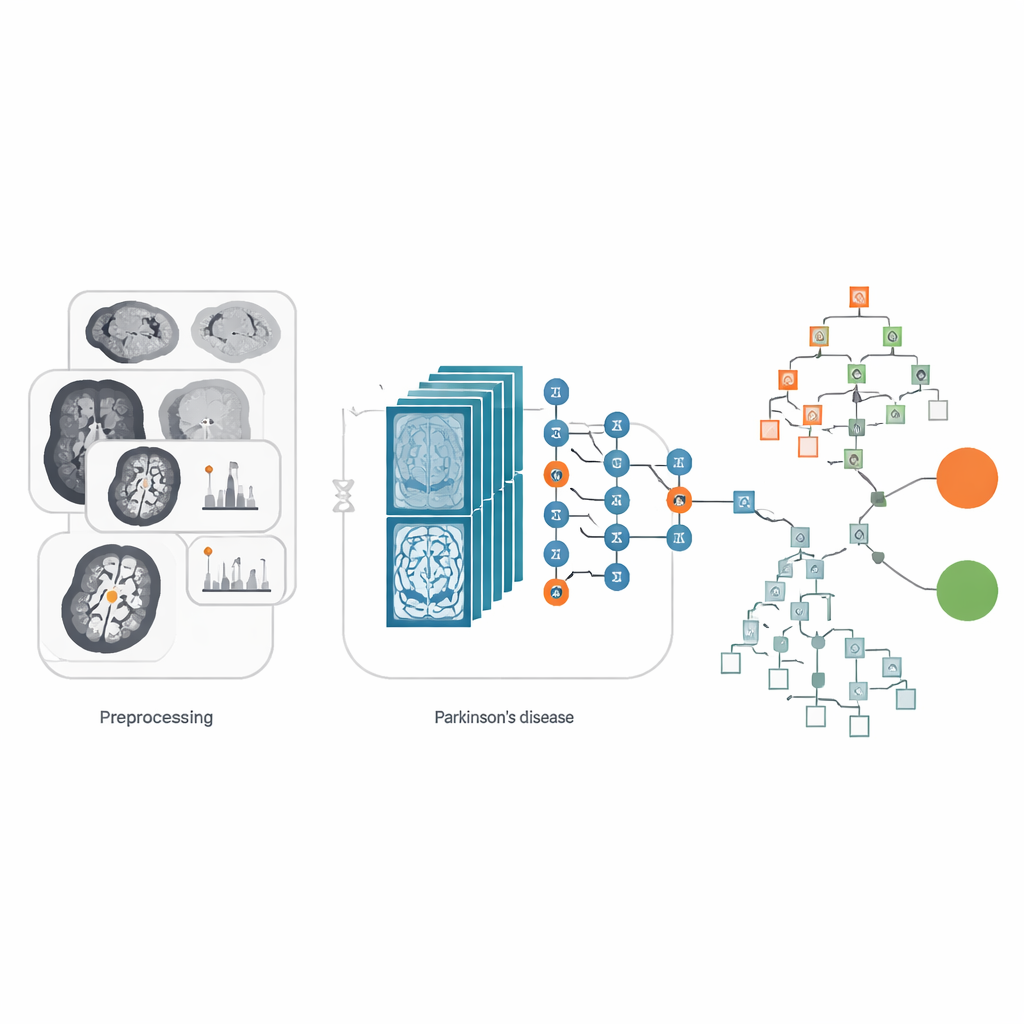
Quelle est la performance du système ?
Pour évaluer la fiabilité, les chercheurs ont comparé plusieurs versions de leur approche. Ils ont testé trois réseaux d’image populaires — VGG16, ResNet50 et EfficientNetB0 — dans trois modes : utilisés tels quels, ajustés (fine-tuning), et combinés avec l’étape de décision XGBoost. Parmi ces options, les configurations hybrides ont systématiquement obtenu les meilleurs résultats. La configuration gagnante, EfficientNetB0 plus XGBoost, a correctement classé les scans dans 99,02 % des cas sur l’ensemble de test. Elle a bien géré les quatre catégories : sain et Parkinson, chacun avec et sans un réglage IRM particulier connu sous le nom de FLAIR. Des mesures qui se concentrent sur les cas manqués et les fausses alertes, comme le rappel et le score F1, étaient également très élevées, ce qui suggère que l’outil n’échange pas simplement un type d’erreur contre un autre. Fait important, le modèle est resté efficace en termes de temps de calcul, ce qui le rend plus réaliste pour une utilisation dans des environnements cliniques chargés.
Ce que cela pourrait signifier en clinique
Aucun système informatique ne peut remplacer un neurologue expérimenté, mais ce travail montre qu’un modèle hybride bien conçu peut agir comme un assistant puissant. En analysant rapidement des IRM de routine à la recherche de signes subtils de la maladie de Parkinson, de tels outils pourraient signaler des patients à risque pour un suivi plus étroit bien avant que les symptômes ne deviennent évidents. Les auteurs soulignent que leur travail doit encore être testé sur des groupes de patients plus larges et plus divers, et finalement combiné avec d’autres informations comme des tests moteurs ou des marqueurs sanguins. Néanmoins, leurs résultats suggèrent qu’un logiciel intelligent basé sur des scans déjà disponibles à l’hôpital pourrait devenir un allié rapide, peu coûteux et facilement déployable pour la détection précoce de la maladie de Parkinson.
Citation: Desai, S., Vora, M., Shah, S. et al. Hybrid deep learning novel framework for classification of parkinson’s disease. Sci Rep 16, 9143 (2026). https://doi.org/10.1038/s41598-026-37553-4
Mots-clés: Maladie de Parkinson, IRM cérébrale, apprentissage profond, imagerie médicale, diagnostic précoce