Clear Sky Science · fr
Une approche par ligase biotine scindée révèle les protéines associées à l’alpha‑synucléine oligomérique lors de l’agrégation
Pourquoi les protéines agglomérées dans le cerveau comptent
Dans la maladie de Parkinson et les affections apparentées, une protéine cérébrale normalement utile, l’alpha‑synucléine, peut s’agglomérer en dépôts collants appelés corps de Lewy. Ces dépôts apparaissent des décennies avant les symptômes et constituent un trait distinctif observé à l’autopsie, mais nous ignorons encore quelles autres protéines contribuent à pousser l’alpha‑synucléine d’un état inoffensif vers des agrégats dangereux. Cette étude utilise un « marqueur de proximité » moléculaire astucieux pour cartographier les protéines qui se trouvent près de l’alpha‑synucléine au moment où elle passe de molécules isolées à de petits agrégats, offrant de nouveaux indices sur le déclenchement de la maladie et sur les voies pouvant être ciblées pour la ralentir ou la prévenir.
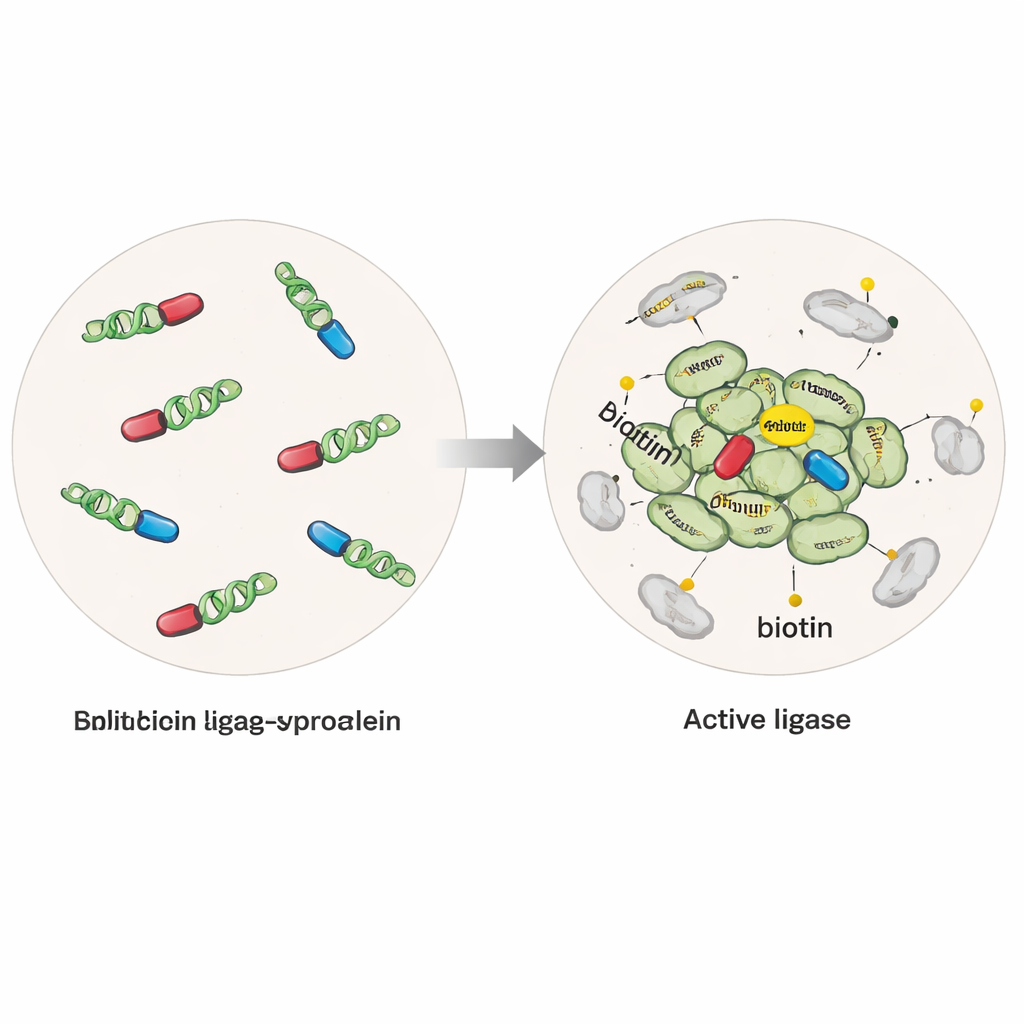
Un « marqueur » moléculaire qui illumine les voisins
Les chercheurs ont modifié des cellules humaines pour produire de l’alpha‑synucléine fusionnée à une enzyme modifiée capable d’attacher une petite étiquette biotine à toute protéine située à quelques milliardièmes de mètre. Dans une version, l’enzyme était intacte et active chaque fois que l’alpha‑synucléine était présente, capturant les protéines proches des molécules isolées comme des agrégats. Dans une seconde version « scindée » plus sélective, l’enzyme était coupée en deux moitiés inactives, chacune attachée à une molécule distincte d’alpha‑synucléine. Ce n’est que lorsque les molécules d’alpha‑synucléine se rassemblaient en multimères ou oligomères que les moitiés se réunissaient en une enzyme active, activant le marquage spécifiquement autour de ces premiers agrégats. En ajoutant des fibrilles d’alpha‑synucléine purifiées aux cellules, l’équipe pouvait également induire une agrégation de type pathologique et comparer les états normaux et pathologiques.
Construire une carte des protéines voisines
Après un temps de marquage, l’équipe a récupéré toutes les protéines marquées à la biotine et les a identifiées par spectrométrie de masse, une technique qui pèse et compte les protéines avec une grande précision. Dans toutes les conditions, ils ont trouvé 1 277 protéines distinctes et, après un filtrage attentif, les ont réduites à 581 protéines susceptibles d’être réellement proches de l’alpha‑synucléine. En comparant les systèmes d’enzyme intacts et scindés, ils ont pu distinguer les protéines qui s’associent principalement aux molécules isolées de celles qui préfèrent les multimères. Ils ont aussi comparé des cellules avec ou sans fibrilles ajoutées pour voir comment l’environnement protéique local de l’alpha‑synucléine change une fois l’agrégation déclenchée.
Principales voies cellulaires entraînées dans les agrégats
Le croquis d’interactome résultant met en évidence plusieurs thèmes biologiques majeurs. Dans des conditions normales, l’alpha‑synucléine multimérique se trouvait proche de nombreuses protéines impliquées dans le trafic membranaire et d’enzymes modifiant les protéines—en accord avec son rôle proposé dans la gestion des vésicules synaptiques et le maintien du contrôle de qualité protéique. Plusieurs enzymes ajoutant des groupements phosphate, dont les kinases PAK4, RIPK2 et MAP4K4, étaient enrichies près des multimères sains mais semblaient perdre le contact une fois les agrégats formés, ce qui suggère que la perturbation de ces relations pourrait favoriser des formes de la protéine liées à la maladie. L’équipe a également détecté des protéines liées à la signalisation de type facteur de croissance ressemblant à l’insuline, soutenant les liens cliniques entre résistance à l’insuline et maladie de Parkinson, et a constaté que l’agrégation recrute des protéines impliquées dans l’élimination des protéines endommagées, comme la famille de chaperonnes 14‑3‑3 et des composants spécifiques des voies de dégradation cellulaire.
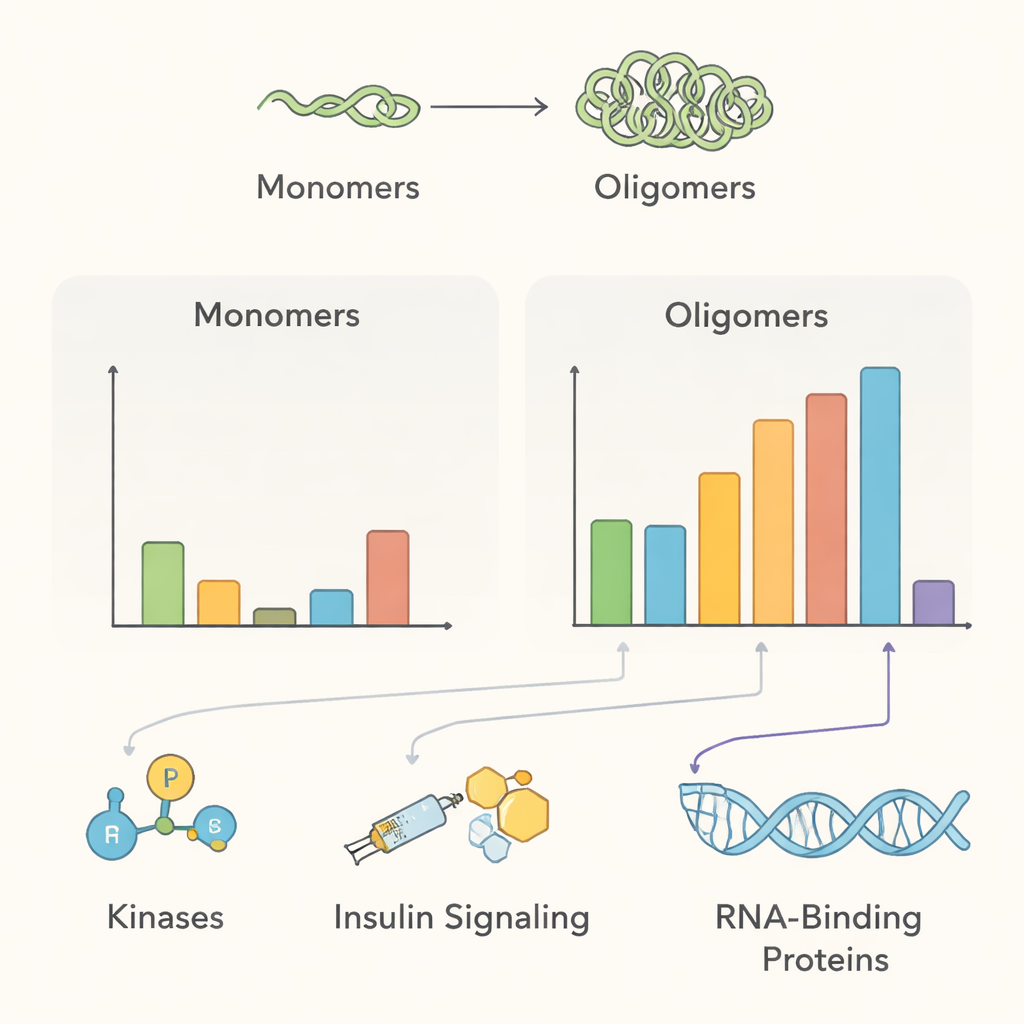
Liens inattendus avec d’autres troubles cérébraux
Au‑delà de la maladie de Parkinson, les données soulignent une connexion surprenante avec la sclérose latérale amyotrophique (SLA) et la démence frontotemporale (DFT). Une protéine liant l’ARN appelée FUS, qui se relocalise et s’agrège dans ces affections, apparaissait proche de l’alpha‑synucléine multimérique tant dans les conditions normales que dans les conditions d’agrégation. D’autres protéines liées à l’ARN ont également modifié leur proximité à mesure que l’alpha‑synucléine s’agrégeait. Ces résultats suggèrent que de petits assemblages d’alpha‑synucléine pourraient piéger des protéines de gestion de l’ARN au mauvais endroit dans la cellule, reliant potentiellement la biologie des maladies à corps de Lewy à celle de la SLA et de la DFT, bien que des interactions physiques directes restent à vérifier.
Ce que cela signifie pour la compréhension de la maladie
Pour les non‑spécialistes, l’idée principale est que ce travail fournit une « liste de contacts » en stade précoce des protéines qui accompagnent l’alpha‑synucléine lorsqu’elle passe d’un rôle utile à un agrégat nocif. L’étude suggère que la perte de certaines relations protectrices—comme avec des kinases spécifiques ou des enzymes de contrôle qualité—peut être aussi importante que l’acquisition de nouveaux partenaires toxiques. Bien que les expériences aient été réalisées dans un modèle cellulaire simplifié et ne prouvent pas encore la causalité, elles mettent en lumière des candidats et des voies concrets pour des tests futurs dans des neurones et des tissus cérébraux. À long terme, cartographier ces quartiers protéiques changeants pourrait guider des stratégies visant à restaurer des interactions protectrices, soutenir la signalisation liée à l’insuline ou empêcher la capture de protéines liant l’ARN, ralentissant potentiellement la progression des modifications moléculaires subtiles vers les maladies à corps de Lewy.»
Citation: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Mots-clés: alpha-synucléine, maladie à corps de Lewy, agrégation des protéines, protéomique de proximité, maladie de Parkinson