Clear Sky Science · fr
Perspectives sur les différences structurelles entre homo- et hétérodimères enrichis à partir d’un cocktail d’anticorps monoclonaux contre le SARS-CoV-2
Pourquoi le mélange d’anticorps peut réserver des surprises
Pendant la pandémie de COVID-19, des médicaments à base d’anticorps comme le cocktail REGEN-COV ont été utilisés pour neutraliser le virus responsable, le SARS-CoV-2. Ces médicaments sont conçus avec soin, mais une fois mélangés en flacon, ils peuvent former des appariements rares appelés hétérodimères — deux anticorps différents associés en paire. Cette étude pose une question pratique aux importantes implications pour la sécurité et l’efficacité : lorsque ces paires inhabituelles se forment, se comportent-elles différemment des paires plus familières d’anticorps identiques, et cela pourrait-il modifier l’efficacité du médicament ?
Paires inhabituelles dans un puissant traitement contre la COVID-19
REGEN-COV combine deux anticorps monoclonaux, le casirivimab et l’imdevimab, chacun conçu pour se lier à la protéine spike du SARS-CoV-2 d’une manière différente. Lorsqu’ils sont formulés ensemble, une faible fraction des anticorps s’associe en paires. Certaines paires sont des homodimères (deux copies du même anticorps) ; d’autres sont des hétérodimères (un casirivimab plus un imdevimab). Les hétérodimères sont considérés comme des impuretés car ils ne font pas partie de la conception initiale du médicament, et leur comportement dans l’organisme était largement inconnu. Les auteurs ont d’abord utilisé un procédé de purification en plusieurs étapes pour isoler plusieurs espèces distinctes d’homodimères ainsi que l’hétérodimère à partir du même lot de REGEN-COV, leur offrant une opportunité rare de comparer toutes ces assemblées côte à côte.
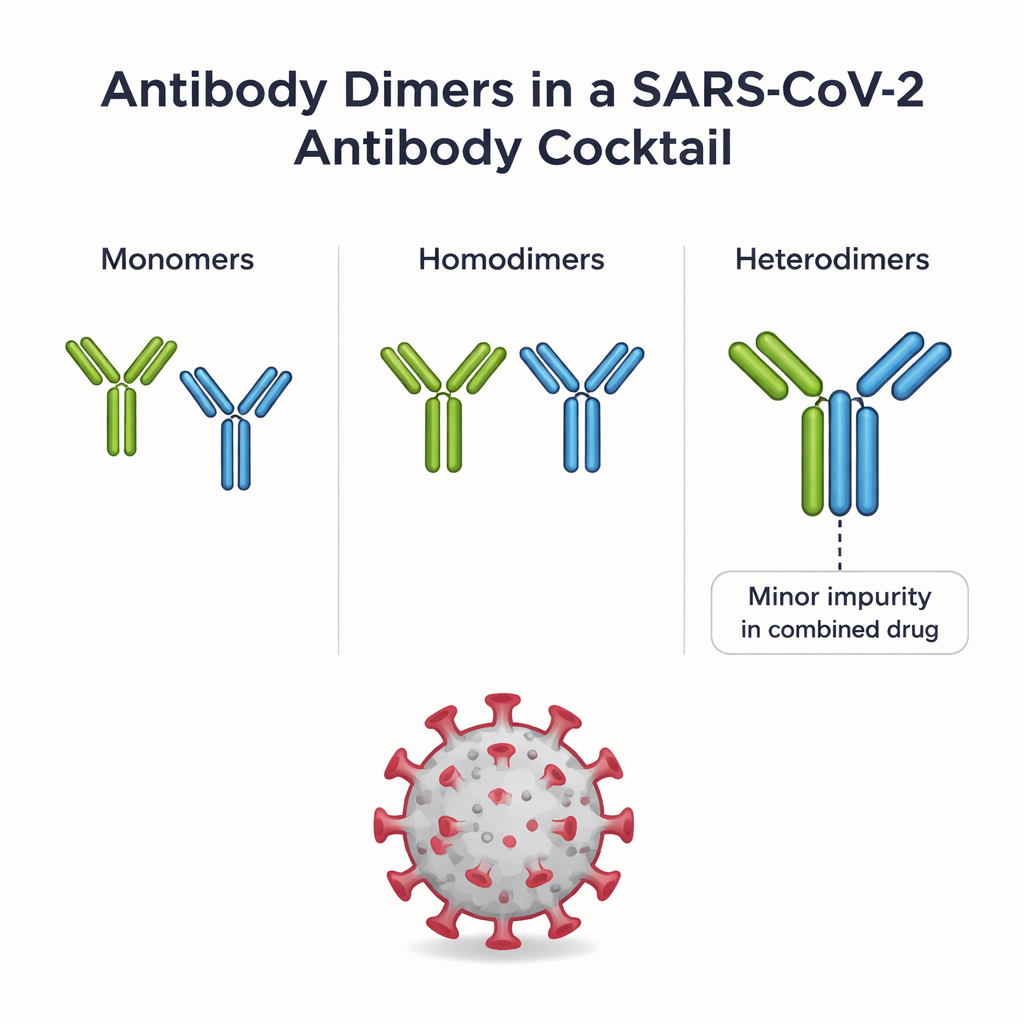
Explorer la forme, l’adhérence et les liaisons chimiques
Pour comprendre ce qui rend chaque type de dimère unique, l’équipe a combiné plusieurs outils analytiques de pointe. Des expériences de chromatographie ont révélé comment les dimères diffèrent en « adhérence » de surface (hydrophobicité), tandis que l’électrophorèse capillaire et une forme spécialisée de spectrométrie de masse ont montré si les deux anticorps d’un dimère sont maintenus ensemble par des attractions faibles ou par des liaisons covalentes plus fortes. La microscopie électronique et l’ultracentrifugation analytique ont ensuite fourni des renseignements sur la forme globale — si un dimère est allongé et flexible ou compact et fortement empaqueté. Ensemble, ces méthodes ont montré que le casirivimab et l’imdevimab forment plusieurs homodimères distincts avec des formes et des schémas de liaison différents, et que l’hétérodimère est particulièrement compact et enrichi en liaisons covalentes impliquant différentes parties des bras et de la tige de l’anticorps.
Comment la structure se relie au blocage du virus et à la destruction cellulaire
Les chercheurs ont ensuite cherché à savoir comment ces différences structurelles affectent ce qui compte vraiment : arrêter le virus et mobiliser le système immunitaire. Ils ont testé chaque dimère dans un test de neutralisation par pseudovirus, qui mesure la capacité des anticorps à bloquer l’entrée d’une particule de type viral, et dans un essai d’activité cytotoxique cellulaire dépendante des anticorps (ADCC), qui évalue l’efficacité avec laquelle les anticorps recrutent des cellules immunitaires pour détruire des cibles infectées. De manière surprenante, la plupart des formes dimériques étaient au moins aussi performantes, et parfois meilleures, que leurs monomères individuels pour neutraliser le virus. En particulier, les homodimères d’imdevimab ont montré une neutralisation « hyper-puissante », probablement parce que leur géométrie leur permet de relier plusieurs protéines spike à la surface virale. Certains homodimères de casirivimab ont produit des signaux ADCC particulièrement forts, apparemment parce que leur orientation laisse les régions terminales (les portions Fc) bien exposées aux récepteurs des cellules immunitaires.
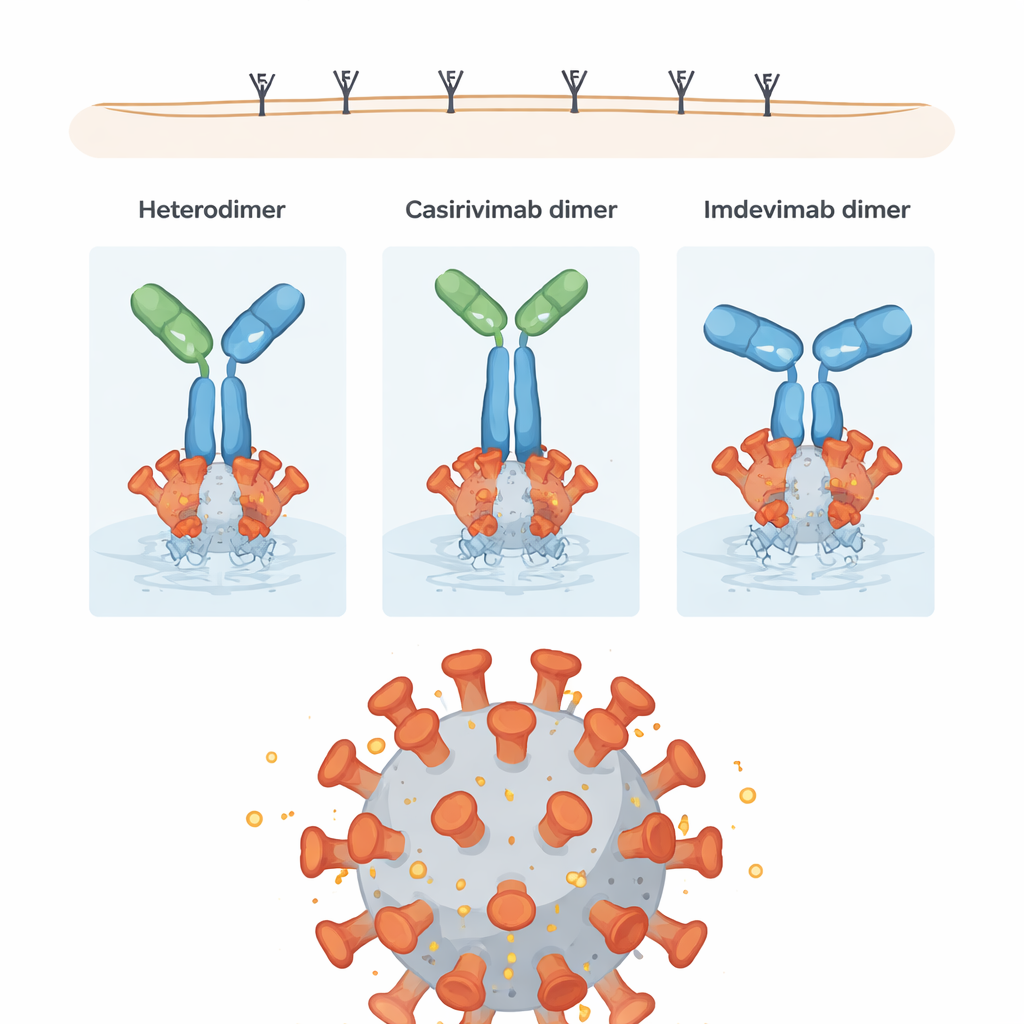
Une impureté compacte aux performances mitigées
L’hétérodimère, malgré sa richesse en connexions fortes et compactes entre ses deux anticorps différents, a montré des performances quelque peu réduites : environ 70 % de l’activité de neutralisation et d’ADCC du mélange co-formulé prévu. Le croisement étendu entre ses bras et sa tige semble restreindre la liberté de rotation et de réorientation de la molécule lorsqu’elle est liée à la spike virale, ce qui peut à son tour limiter à la fois le blocage du virus et la signalisation vers les cellules immunitaires. Néanmoins, bon nombre de ses liaisons sont du type susceptible de se rompre lentement en conditions physiologiques, rendant l’hétérodimère relativement instable au fil du temps et sujet à revenir à des anticorps individuels.
Ce que cela signifie pour les médicaments à base d’anticorps
Pour les patients et les développeurs de médicaments, le message principal est rassurant mais nuancé. Cette étude approfondie des dimères de REGEN-COV suggère que la plupart des formes dimériques, y compris l’impureté hétérodimérique inhabituelle, conservent une activité antivirale substantielle, et il n’existe pas de signal clair de risque de sécurité accru lié aux agrégats de haut poids moléculaire dans ce système. En même temps, le travail montre que des détails fins — où les anticorps se touchent, à quel point ils sont réticulés, et s’ils sont compacts ou allongés — peuvent modifier sensiblement la puissance. Les auteurs soutiennent qu’un profilage structurel et fonctionnel similaire des dimères dans d’autres médicaments à base d’anticorps pourrait devenir une approche non clinique puissante pour comprendre et gérer les impuretés, et pourrait même inspirer de nouveaux anticorps multimériques intentionnellement conçus qui tirent parti de la géométrie pour mieux reconnaître et neutraliser les virus.
Citation: Nguyen, J.B., Liu, S., Yan, Y. et al. Insights into the structural differences between homo- and heterodimers enriched from a cocktail of monoclonal antibodies against SARS-CoV-2. Sci Rep 16, 7024 (2026). https://doi.org/10.1038/s41598-026-37545-4
Mots-clés: dimères d’anticorps, REGEN-COV, spicule du SARS-CoV-2, cocktails d’anticorps monoclonaux, agrégats protéiques