Clear Sky Science · fr
Immobilisation covalente de la peroxydase de Lepidium draba sur des nanoparticules magnétiques recouvertes de chitosane et application au biosurveillance du glucose
Pourquoi les tout petits aimants comptent pour la glycémie
Maintenir la glycémie sous contrôle est essentiel pour gérer le diabète et prévenir des atteintes à long terme du cœur, des reins, des yeux et des nerfs. Les tests de glucose actuels sont efficaces, mais les enzymes qu’ils contiennent peuvent être fragiles, de courte durée de vie et difficilement réutilisables, ce qui augmente les coûts et les déchets. Cette étude explore un procédé astucieux pour rendre une enzyme végétale plus robuste et plus durable en la fixant sur des billes magnétiques microscopiques, ouvrant la voie à des tests de glucose plus rapides, plus fiables et potentiellement moins coûteux.
Un aide‑plante inspiré du raifort
De nombreux tests médicaux reposent sur des enzymes — des protéines qui accélèrent des réactions chimiques. Un pilier des laboratoires diagnostiques est la peroxydase de raifort, utilisée pour transformer des changements chimiques invisibles en variations de couleur visibles à l’œil nu. Les chercheurs ont travaillé avec un proche cousin végétal de cette enzyme, nommé peroxydase de Lepidium draba, produit en bactérie afin de pouvoir l’obtenir en grande quantité. À l’état libre, cette enzyme est puissante mais délicate : elle perd de l’activité sous l’effet de la chaleur, du stockage et des usages répétés, ce qui limite son intérêt pour les capteurs industriels et les kits cliniques.
Transformer des enzymes en outils magnétiques
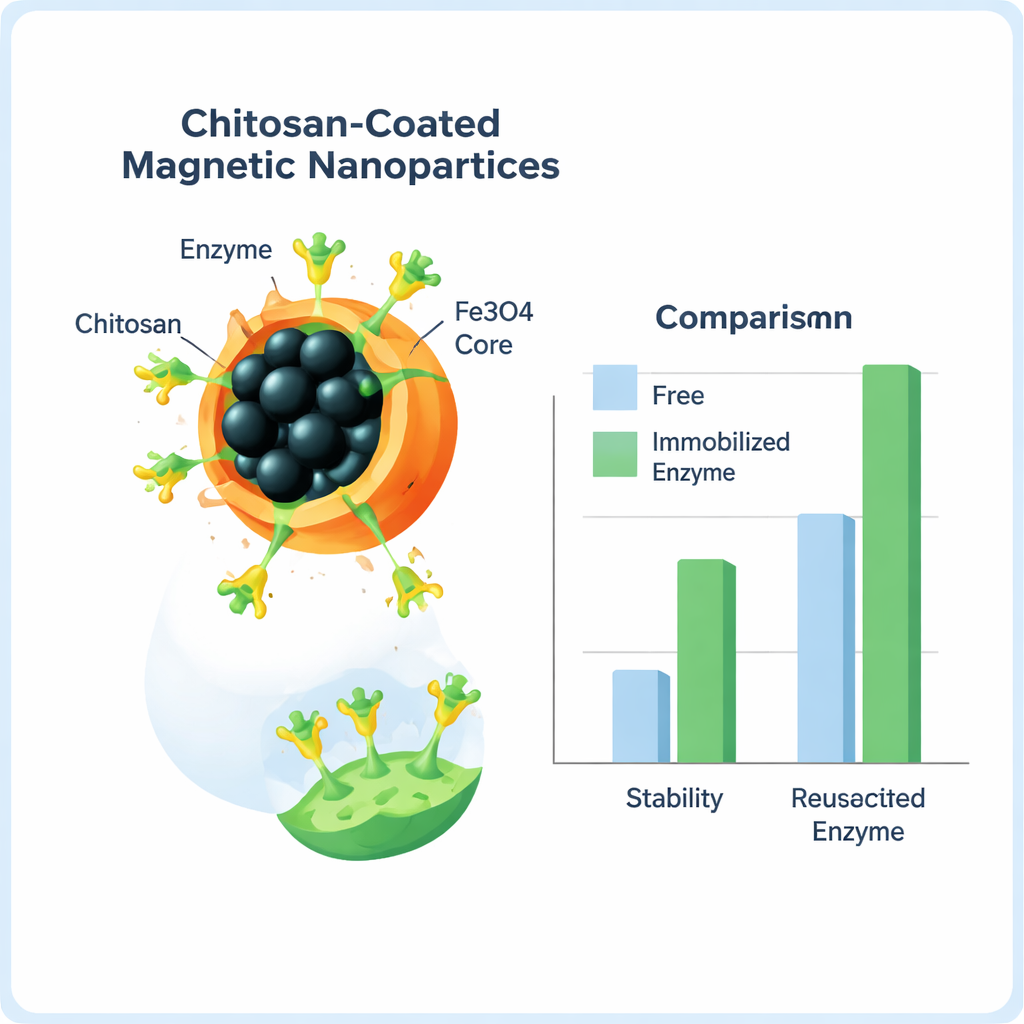
Pour protéger et réutiliser l’enzyme, l’équipe l’a fixée sur des nanoparticules d’oxyde de fer — de minuscules grains de matériau magnétique — recouvertes d’un polymère naturel appelé chitosane, dérivé des coquilles de crustacés. Le chitosane fournit une couche douce et biocompatible riche en « poignées » chimiques capables d’accrocher les enzymes. À l’aide d’une petite molécule de réticulation, le glutaraldéhyde, ils ont formé des liaisons covalentes solides entre l’enzyme et les particules recouvertes. Les scientifiques ont ensuite ajusté la quantité de réticulant utilisée, la durée de la réaction et la quantité de support ajoutée, pour aboutir à des conditions offrant le meilleur compromis entre la quantité d’enzyme fixée et son activité résiduelle.
Contrôler la structure, la robustesse et la tenue dans le temps
Après immobilisation, l’équipe a confirmé la présence de l’enzyme sur les particules en utilisant plusieurs outils structuraux qui lisent les vibrations de liaisons, les motifs cristallins et la topographie de surface. Plus important pour une utilisation pratique, l’enzyme immobilisée s’est montrée supérieure à sa forme libre. Elle a affiché une affinité plus élevée pour son substrat colorant et l’a converti en produit coloré bien plus efficacement — jusqu’à 11 fois plus d’efficacité catalytique dans certains tests. L’enzyme fixée a aussi toléré une plage d’acidité plus large, conservé une activité plus élevée sur des températures utiles, et résisté plus longtemps à une incubation à 50 °C. Sa demi‑vie à cette température a plus que doublé, et après deux mois au réfrigérateur elle conservait environ deux fois plus d’activité que l’enzyme libre. Du fait de la nature magnétique des particules, elles pouvaient être retirées de la solution à l’aide d’un aimant et réutilisées ; même après 11 cycles réactionnels, environ 40 % de l’activité initiale était encore présente.
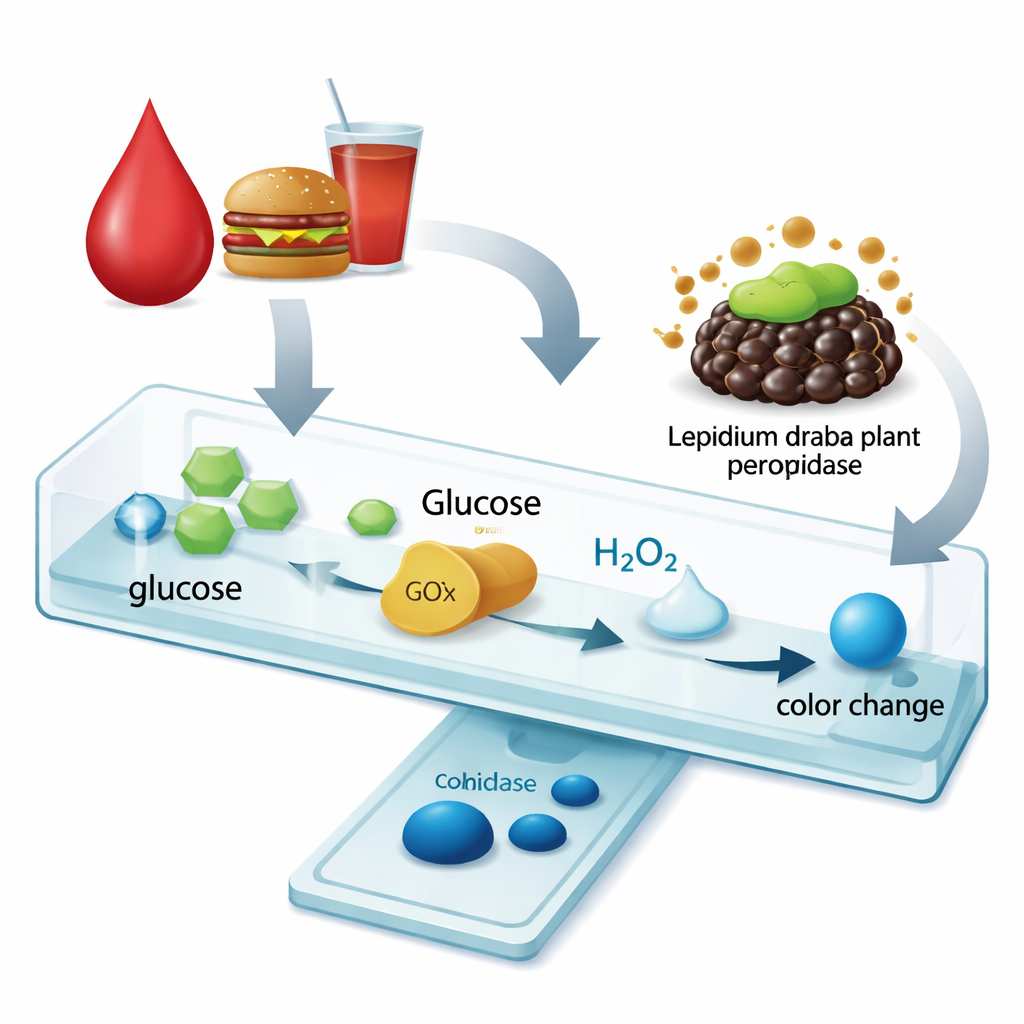
Un changement de couleur plus net pour les tests de glucose
Pour vérifier si cette enzyme renforcée améliore réellement un test pratique, les chercheurs ont construit un essai simple de détection du glucose par couleur. D’abord, une glucose oxydase standard convertit le glucose en peroxyde d’hydrogène. Ensuite, la peroxydase de Lepidium draba, libre ou immobilisée sur les billes de chitosane magnétiques, utilise ce peroxyde d’hydrogène pour transformer un colorant incolore en bleu profond. Avec la forme immobilisée, la gamme de mesure utile pour le glucose s’est considérablement élargie — passant d’une couverture de seulement 0,1 à 1 millimole par litre avec l’enzyme libre à 0,1 à 10 millimoles par litre une fois immobilisée. Parallèlement, le temps de réaction requis pour l’essai a été réduit à environ un tiers, tandis que le seuil de détection minimal du glucose restait très bas et cliniquement pertinent.
Ce que cela signifie pour la santé au quotidien
En ancrant une enzyme végétale sur des nanoparticules magnétiques recouvertes de chitosane, les auteurs ont créé un composant de capteur de glucose colorimétrique robuste, réutilisable et très sensible. Pour le grand public, cela signifie que de futures bandelettes de test, kits de laboratoire ou même emballages intelligents pour aliments pourraient devenir plus stables, plus précis sur une plage de sucres plus large et potentiellement moins coûteux parce que l’enzyme active peut être récupérée et réutilisée. Bien que des travaux supplémentaires soient nécessaires pour augmenter la quantité d’enzyme que les particules peuvent accueillir et pour étendre l’approche à d’autres marqueurs sanguins comme le cholestérol ou l’urée, cette étude montre comment des nanomatériaux et des polymères naturels peuvent s’associer pour transformer des outils biochimiques familiers en systèmes diagnostiques plus résistants, plus propres et plus polyvalents.
Citation: Sepahi-Baghan, M., Asoodeh, A. & Riahi-Madvar, A. Covalent immobilization of Lepidium draba peroxidase on chitosan-coated magnetic nanoparticles and its application in glucose biosensing. Sci Rep 16, 7035 (2026). https://doi.org/10.1038/s41598-026-37542-7
Mots-clés: biocapteur de glucose, immobilisation d’enzyme, nanoparticules magnétiques, détection colorimétrique, peroxydase