Clear Sky Science · fr
Interaction du champ électromagnétique pulsé basse fréquence (PEMF) avec les mitochondries
Champs délicats et centrales énergétiques de la cellule
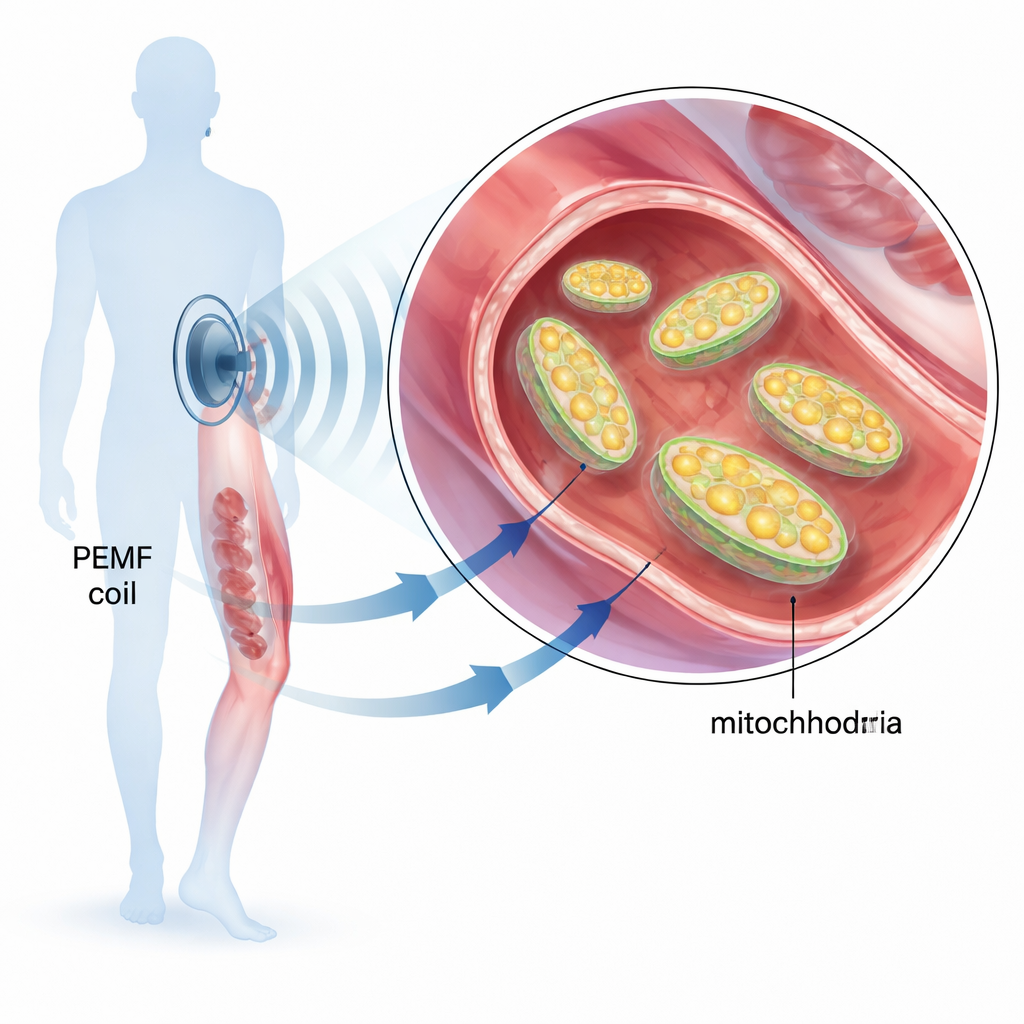
La thérapie par champ électromagnétique pulsé (PEMF) est déjà utilisée en clinique pour favoriser la consolidation osseuse, soulager les douleurs articulaires et accélérer la récupération après chirurgie. Pourtant, nous ne comprenons pas entièrement comment ces champs doux et basse fréquence agissent à l’intérieur de notre corps. Cette étude pose une question simple mais importante : les signaux PEMF influencent‑ils directement les mitochondries, ces petites centrales des cellules qui génèrent la majeure partie de notre énergie, et si oui, comment ?
Pourquoi les mitochondries comptent pour la santé quotidienne
Les mitochondries transforment la nourriture et l’oxygène en ATP, la « monnaie énergétique » universelle des cellules. Quand les mitochondries défaillent, les tissus guérissent plus lentement, les muscles se fatiguent plus vite et les maladies liées à un métabolisme altéré peuvent s’aggraver. Comme des travaux antérieurs laissaient entendre que les traitements PEMF améliorent le métabolisme énergétique et soutiennent la réparation tissulaire, les auteurs se sont concentrés sur la question de savoir si un dispositif PEMF spécifique pouvait ajuster l’activité mitochondriale. Ils ont utilisé un signal magnétique bien défini : des impulsions courtes, de l’ordre de la milliseconde, d’une sinusoïde à 30 kHz avec une faible énergie d’entrée, appliquées à des cellules musculaires en culture, à des tissus de rat et à des mitochondries purifiées.
Regarder de plus près à l’intérieur des cellules vivantes
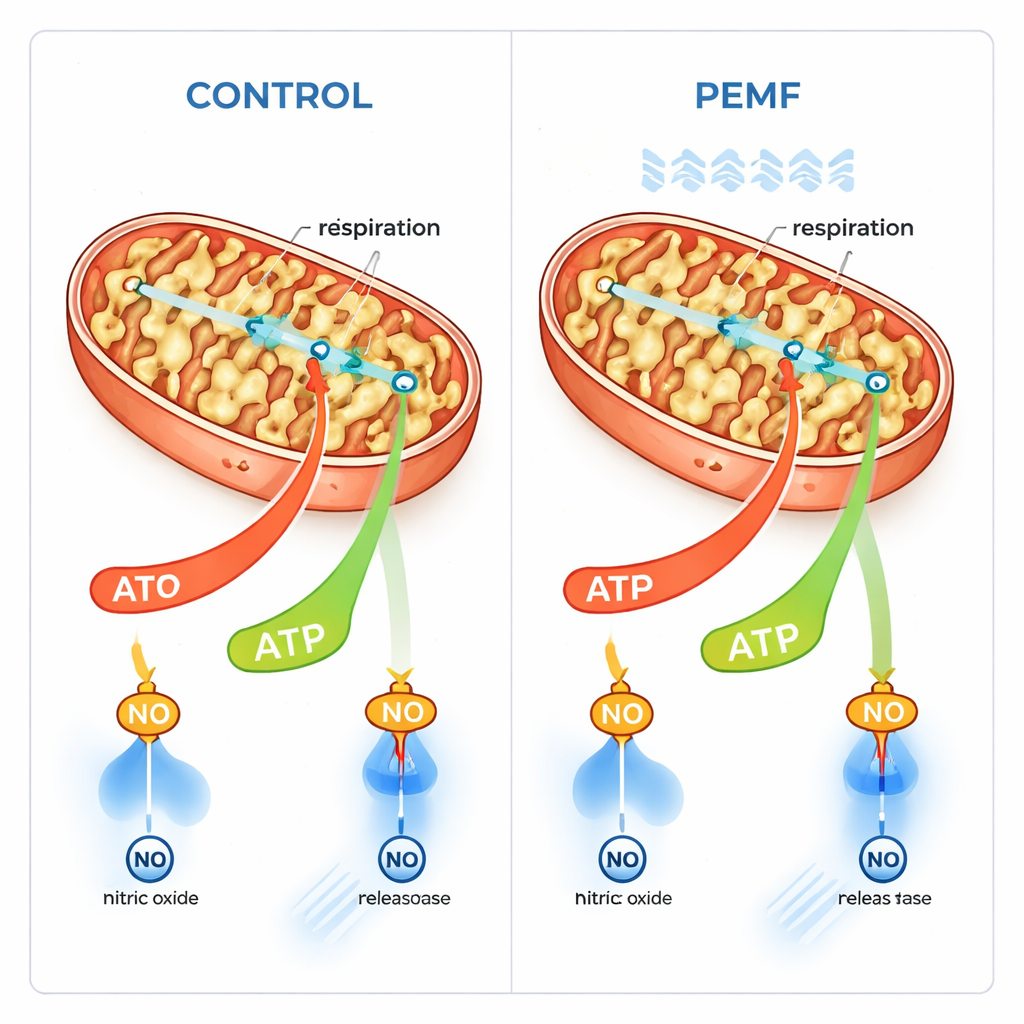
Dans des cellules musculaires humaines cultivées en laboratoire, l’équipe a mesuré trois indicateurs clés après exposition au PEMF : le potentiel électrique à travers la membrane interne mitochondriale (une sorte de petite batterie), les niveaux d’espèces réactives de l’oxygène (des niveaux élevés peuvent être dommageables) et l’oxyde nitrique, un gaz pouvant temporairement bloquer la respiration mitochondriale. Environ 90 minutes après le traitement, le potentiel de membrane mitochondriale était légèrement inférieur, tandis que les niveaux d’oxyde nitrique diminuaient ; les espèces réactives de l’oxygène n’augmentaient pas. Une petite baisse du potentiel de membrane peut signaler soit des dommages soit une production d’ATP plus active. Comme les cellules ne présentaient pas de signes de stress, les auteurs ont supposé que les mitochondries fonctionnaient simplement un peu plus vite et utilisaient la tension stockée à travers leur membrane interne.
Tester la « respiration » des mitochondries
Pour tester cette idée de façon plus directe, les chercheurs ont perforé délicatement la membrane externe des cellules afin de fournir avec précision différents carburants aux mitochondries et de mesurer la consommation d’oxygène. Ils ont observé de manière constante une tendance à une respiration plus élevée liée à la production d’ATP après PEMF, en particulier en présence de glutamate, un carburant mitochondrial courant. L’analyse statistique sur de nombreux échantillons a suggéré que la combinaison de l’exposition PEMF et du choix du carburant influençait significativement la vitesse de consommation d’oxygène des mitochondries. Il est important de noter qu’il n’y avait aucune trace d’un effet nocif du PEMF sur les cellules ou leurs mitochondries. Au contraire, les champs semblaient stimuler sélectivement le mode « couplé » de la respiration, où la consommation d’oxygène est étroitement liée à la fabrication d’ATP, sans augmenter la combustion inefficace et découplée du carburant.
Inflammation, oxyde nitrique et une surprise de la lumière bleue
Parce que l’oxyde nitrique peut s’accumuler lors d’une inflammation et bloquer une étape clé de la respiration mitochondriale, l’équipe a cherché à savoir si le PEMF pouvait aider les mitochondries à se remettre d’une telle inhibition. Ils ont ajouté un donneur chimique d’oxyde nitrique à des homogénats de muscle et de foie et à des mitochondries hépatiques isolées, ralentissant fortement la respiration. Dans ces conditions, le PEMF n’a pas restauré la fonction mitochondriale, même lorsque les mitochondries étaient très concentrées. Pour vérifier si le blocage était du tout réversible, ils ont éclairé les mitochondries inhibées par l’oxyde nitrique avec de la lumière bleue, en utilisant une méthode connue pour libérer l’oxyde nitrique de son site de liaison. La lumière bleue a partiellement restauré la respiration, confirmant que le système pouvait récupérer, mais le PEMF n’a apporté aucun bénéfice supplémentaire. Cela montre que les effets positifs du PEMF ne proviennent pas d’un retrait de l’oxyde nitrique dans des conditions de type inflammatoire.
Portes membranaires et flux d’énergie
En traçant une analogie entre les cellules et les circuits électriques, les auteurs suggèrent que le PEMF agit principalement sur les membranes biologiques. Les mitochondries sont entourées d’une membrane externe qui contient une protéine porteuse clé appelée VDAC, permettant le passage des molécules liées à l’énergie. Contrairement à la membrane interne qui présente une très haute tension, la membrane externe a une tension plus faible, plus facilement modulable. Les auteurs proposent que le PEMF altère subtilement ce potentiel de membrane externe, modifiant la fréquence d’ouverture des portes VDAC et facilitant ainsi le flux de carburant et d’ATP consommé à travers la membrane. Cela stimulerait naturellement le mode de respiration couplé, producteur d’ATP, sans modifier la capacité maximale de la machinerie de transport d’électrons elle‑même.
Ce que cela signifie pour les thérapies futures
Globalement, l’étude ne trouve aucune preuve que ce type de PEMF soit nocif pour les mitochondries. Au contraire, le PEMF améliore légèrement la partie de la respiration mitochondriale qui produit de l’ATP, tout en laissant inchangées la capacité respiratoire maximale et le stress oxydatif. Cependant, il ne restaure pas les mitochondries bloquées par un fort oxyde nitrique, ce qui suggère que ses bénéfices dans les tissus inflammés doivent passer par d’autres mécanismes. Pour les patients et les cliniciens, ces résultats soutiennent l’idée que des champs électromagnétiques soigneusement réglés peuvent inciter les centrales cellulaires à un état plus efficace de production d’énergie — offrant une explication mécanistique plausible à certains effets de guérison rapportés dans la réparation osseuse, les soins des plaies et la récupération post‑chirurgicale.
Citation: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Mots-clés: thérapie par champ électromagnétique pulsé, mitochondries, énergie cellulaire, oxyde nitrique, production d’ATP