Clear Sky Science · fr
Validation d’un nouveau biomarqueur génomique de l’évolutivité des cellules souches mésenchymateuses et implications du statut génotypique sur les phénotypes de sénescence cellulaire
Pourquoi la culture des cellules souches devient plus difficile avec le temps
Les cellules souches issues de la moelle osseuse adulte sont au cœur de nombreuses thérapies expérimentales, de la réparation osseuse à la modulation de l’inflammation. Mais il y a un hic : pour traiter un patient, les laboratoires doivent faire croître ces cellules hors du corps, et plus l’expansion dure, plus elles ralentissent et adoptent un comportement de cellules « vieillies ». Cette étude examine pourquoi les cellules souches de certaines personnes vieillissent plus lentement en culture, et si un petit fragment d’ADN manquant peut aider les chercheurs à sélectionner les cellules les plus robustes pour des traitements futurs.
Un gène absent qui change les règles
Les chercheurs se sont concentrés sur un gène appelé GSTT1, qui aide les cellules à détoxifier les molécules nuisibles produites lors du métabolisme et du stress. Fait surprenant, une fraction non négligeable de la population est totalement dépourvue de ce gène – on parle de « GSTT1 null ». Des travaux antérieurs laissaient entendre que les cellules souches de moelle osseuse de ces individus pourraient croître plus rapidement et conserver plus longtemps leurs protections chromosomiques, les télomères. Dans ce projet, l’équipe a étudié les cellules souches de six donneurs sains, les a regroupées en GSTT1‑positifs et GSTT1‑null, puis a suivi leur comportement au cours de nombreuses divisions et après exposition à des rayons X, un puissant déclencheur de sénescence cellulaire.
Des cellules à multiplication rapide qui résistent aux signaux du vieillissement
Lorsque les scientifiques ont suivi le nombre de cellules sur plusieurs jours, les cellules souches GSTT1‑null se sont multipliées plus rapidement aux premiers passages que les cellules porteuses du gène. Sur de très longues périodes d’expansion, les taux de croissance entre les groupes sont devenus plus proches, mais l’avantage initial était net. Pour évaluer directement la sénescence, l’équipe a utilisé une coloration classique qui colore en bleu les cellules sénescentes, ou « âgées ». Après de nombreux cycles de division, et à nouveau après irradiation, les cultures GSTT1‑null contenaient systématiquement moins de cellules bleues sénescentes que les cultures GSTT1‑positives. Il est important de noter que cette différence ne résultait pas d’un ralentissement de l’érosion des télomères ni d’une activité accrue de l’enzyme qui maintient les télomères (hTERT) ; ces deux mesures étaient semblables quel que soit le statut GSTT1, ce qui suggère qu’un autre mécanisme était en jeu.
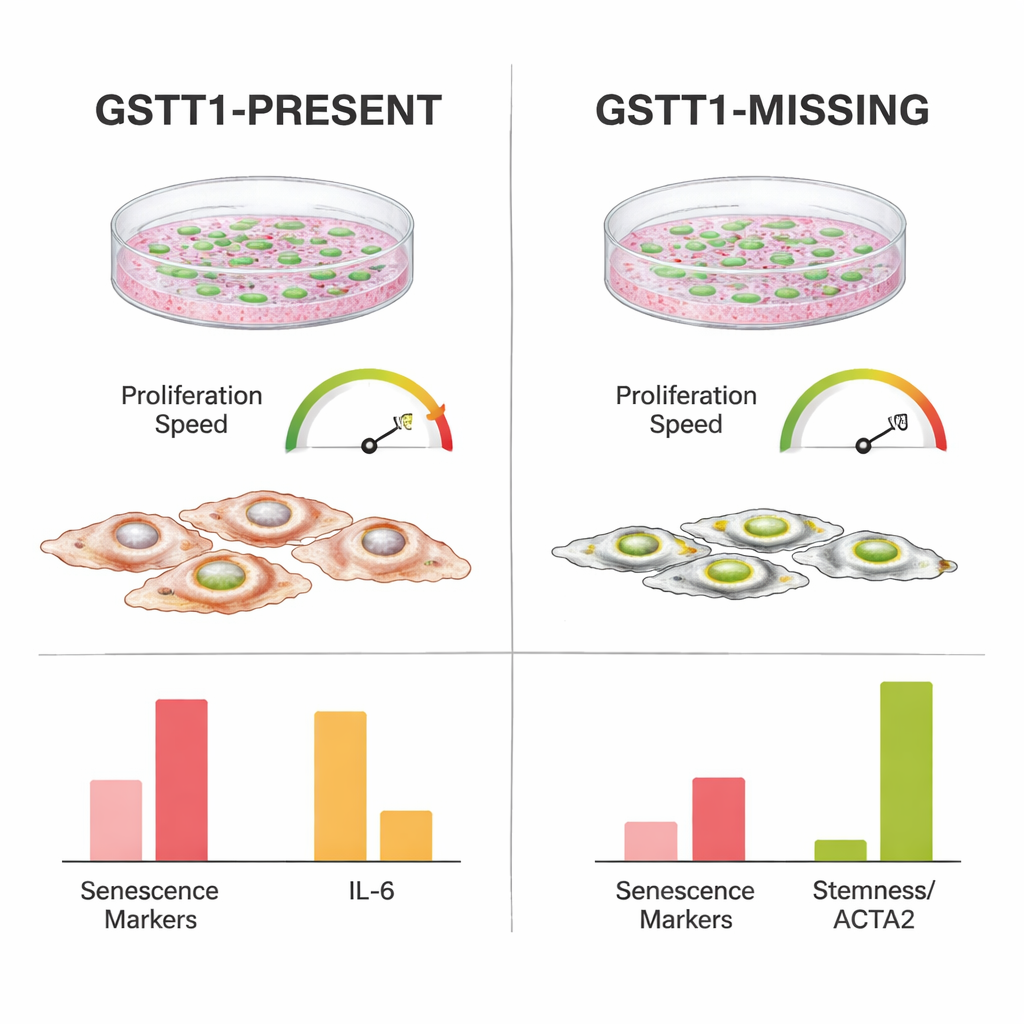
Moins de stress et d’inflammation en culture
Pour comprendre ce qui rendait les cellules GSTT1‑null plus résistantes, les chercheurs ont mesuré l’activité de gènes liés à l’arrêt du cycle cellulaire, aux dommages de l’ADN et au soi‑disant phénotype sécrétoire associé à la sénescence (SASP) — un cocktail de signaux inflammatoires et de stress libérés par les cellules vieillissantes. Les cellules portant GSTT1 montraient des niveaux plus élevés de signaux « stop » clés tels que p21 et p14, en particulier aux passages tardifs et après irradiation. Elles augmentaient également l’expression d’IL‑6, une molécule inflammatoire puissante, et d’autres gènes liés au stress plus fortement que les cellules GSTT1‑null. En revanche, les cellules souches GSTT1‑null conservaient des niveaux plus faibles de ces marqueurs de vieillissement et d’inflammation, tout en maintenant des niveaux plus élevés d’ACTA2 et de TWIST1, des gènes associés à l’intégrité structurelle et au caractère souches. Il est notable que les deux génotypes ont conservé une capacité similaire à se spécialiser en cellules osseuses et adipeuses, ce qui indique que l’effet protecteur n’était pas simplement dû à une perte de la fonction normale des cellules souches.
Ce que cela pourrait signifier pour les thérapies cellulaires futures
Ensemble, les résultats suggèrent que les cellules souches de moelle osseuse dépourvues de GSTT1 sont partiellement protégées de l’usure habituelle liée à l’expansion en laboratoire et à la radiation. Elles croissent plus vite au départ, accumulent moins de cellules manifestement sénescentes et présentent un profil moins inflammatoire, même si leurs chromosomes raccourcissent à des rythmes similaires. Pour les entreprises et les cliniques qui fabriquent de grandes quantités de cellules souches, le statut GSTT1‑null pourrait servir de marqueur génétique pratique pour identifier des donneurs dont les cellules tolèrent mieux l’expansion, ce qui pourrait permettre d’obtenir des thérapies plus constantes et plus puissantes. Bien sûr, l’étude porte sur un petit nombre de donneurs et des conditions de culture non cliniques, donc des études plus larges et rigoureusement contrôlées sont nécessaires. Néanmoins, ce travail illustre comment une différence héréditaire unique peut faire pencher la balance entre un comportement juvénile et un comportement de vieillissement chez des cellules souches cultivées pour la médecine régénérative.
Citation: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Mots-clés: cellules souches mésenchymateuses, sénescence cellulaire, biomarqueurs, fabrication de thérapies cellulaires, polymorphisme GSTT1