Clear Sky Science · fr
Nouvelles perspectives sur la base moléculaire de la gamétogenèse chez la grenouille d’eau hybridogénétique Pelophylax esculentus
Pourquoi ces grenouilles particulières sont importantes
La plupart des animaux, y compris les humains, remélangent leurs gènes à chaque génération lorsque spermatozoïde et ovule se rencontrent. Mais quelques organismes singuliers contournent ces règles et transmettent des génomes entiers tels quels, comme des clones. Les grenouilles d’eau européennes font partie de ce groupe restreint. Elles constituent des expériences vivantes sur la façon dont le sexe, l’asexualité et l’hybridation peuvent s’entrelacer. Comprendre comment ces grenouilles fabriquent leurs ovules et leurs spermatozoïdes n’est pas seulement une curiosité pour un amphibien atypique : cela éclaire aussi la manière dont les génomes sont contrôlés, réparés et parfois implacablement restructurés chez tous les vertébrés.
Des grenouilles qui bafouent les règles de l’hérédité
Dans de nombreux étangs européens, trois grenouilles d’eau étroitement apparentées coexistent. Deux sont des espèces sexuelles ordinaires, appelées ici simplement L et R. Lorsqu’elles s’accouplent, elles peuvent produire un hybride, LR, connu sous le nom de Pelophylax esculentus. Cet hybride fait quelque chose de remarquable : dans sa lignée germinale — les cellules qui deviendront ovules ou spermatozoïdes — il écarte un génome parental et copie l’autre sans le remélanger. Le résultat est une gamète clonale portant soit un génome L intact, soit un génome R intact, qui sera ensuite fécondée par une gamète normale d’une des espèces parentales. Selon le « système de population » local, les hybrides peuvent exclure de façon routinière le génome R, le génome L, ou, dans certains endroits, les deux selon les individus. L’étude pose la question : quels gènes contribuent à orchestrer cette exclusion ciblée du génome et cette transmission clonale ?
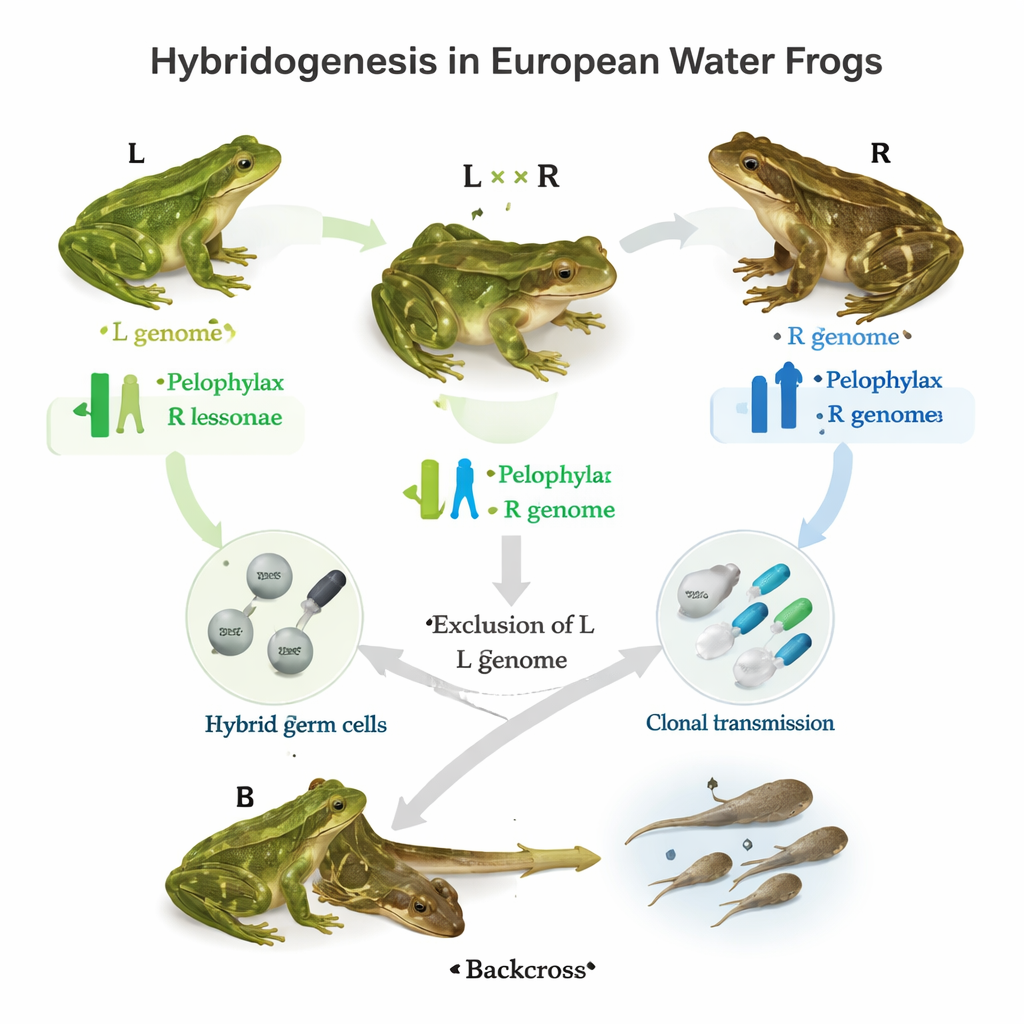
À la recherche des gènes derrière le sexe clonal
Les auteurs ont d’abord établi un catalogue de 160 gènes connus chez d’autres animaux pour participer à la gamétogenèse — le processus de fabrication des ovules et des spermatozoïdes. Ils ont séquencé ces gènes à partir de testicules de grenouilles L et R et comparé leurs caractéristiques de base, comme la longueur, la structure et la composition en bases d’ADN. La plupart de ces gènes se sont révélés fortement conservés entre les deux espèces, ce qui suggère qu’ils jouent des rôles importants tolérant peu de changements. Ensuite, l’équipe s’est concentrée sur 52 de ces gènes et les a analysés pour détecter des différences d’une seule lettre d’ADN, dites polymorphismes mononucléotidiques (SNP), chez plus de 650 grenouilles collectées à travers l’Europe. Ces individus provenaient de différents systèmes de population : ceux où coexistent uniquement L et hybrides, ceux où coexistent uniquement R et hybrides, des systèmes entièrement hybrides riches en triploïdes, et des populations purement R.
Signaux de flux génétique et structure cachée
En examinant les schémas de variation des SNP, les chercheurs ont mis au jour des preuves d’introgression — flux de gènes — entre les réservoirs génétiques L et R. Pour plusieurs gènes, les versions R étaient presque indiscernables de leurs homologues L, mieux expliquées par une hybridation et des rétrocroisements passés. Bien que les taux globaux de flux génique soient faibles, ils étaient plus élevés vers R que vers L, en accord avec des travaux génétiques antérieurs. Lorsque l’équipe a comparé les fréquences des SNP entre les systèmes de population, elle a constaté que certains variants génétiques se regroupaient fortement selon des systèmes particuliers. Par exemple, les hybrides LR issus de populations entièrement hybrides ressemblaient génétiquement davantage aux LR des systèmes R–hybrides qu’aux LR des systèmes diploïdes L–hybrides purs, révélant une structure cachée liée à l’organisation locale de la reproduction.
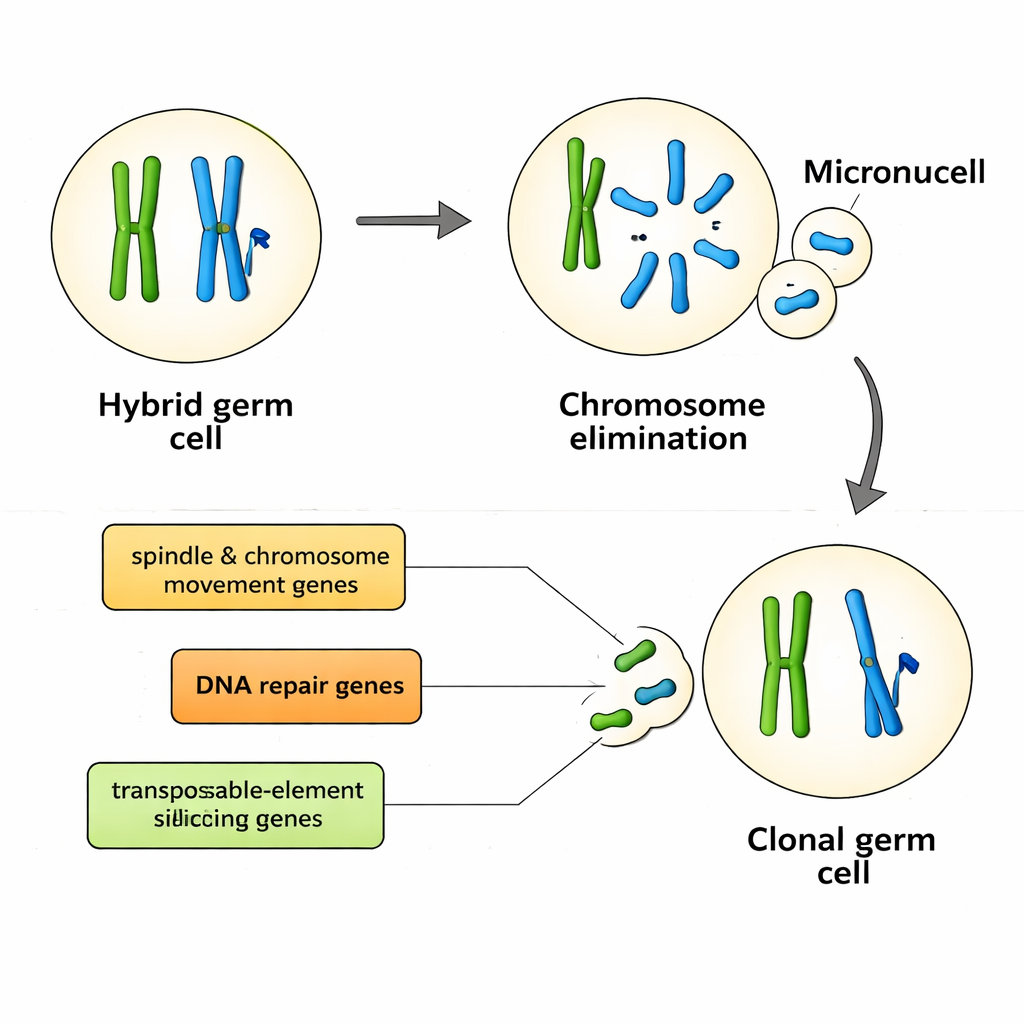
Acteurs clés du contrôle chromosomique et de la défense du génome
Dix gènes, en particulier, ont montré de fortes associations avec le système de population et donc avec la manière dont les génomes sont exclus et transmis de façon clonale. Ils se répartissent en plusieurs groupes fonctionnels. Certains, tels que kif22 et nusap1, aident à construire et contrôler le fuseau, la machine cellulaire qui déplace les chromosomes lors de la division cellulaire. D’autres, notamment hormad1, rad50, rad51ap1 et sfr1, sont centraux pour la formation et la réparation des cassures double-brin de l’ADN — des coupures contrôlées qui favorisent normalement le recombinaison mais pourraient aussi déclencher l’élimination ciblée de chromosomes. Un autre gène, henmt1, stabilise de petits ARN qui répriment les éléments transposables, ces morceaux d’ADN mobiles qui peuvent endommager les génomes ou remodeler les centromères, points d’ancrage nécessaires pour une ségrégation chromosomique correcte. Ensemble, ces gènes dessinent un tableau où l’exclusion du génome résulte de l’interaction entre transport chromosomique, réparation de l’ADN et voies de défense du génome, plutôt que d’un interrupteur maître unique.
Évolution à la limite de la stabilité
L’étude suggère que de rares événements de recombinaison et un flux génique bidirectionnel entre L et R ont contribué à générer des variantes génomiques distinctes favorisant différents modes d’hérédité non mendéliens. Certaines lignées hybrides peuvent accumuler des mutations délétères à mesure que leurs génomes clonaux avancent par « cliquetage », tandis que des recombinaisons sporadiques et l’introgression les rafraîchissent occasionnellement, au prix de problèmes développementaux chez certains descendants. Plutôt que de se conformer à une règle simple fondée sur le degré de divergence entre deux espèces, le système Pelophylax paraît gouverné par un réseau complexe de facteurs interactifs qui ajustent finement si un hybride devient une lignée clonale stable ou une impasse évolutive.
Que signifie cela au-delà des grenouilles
Pour le lecteur général, la leçon principale est que l’hérédité peut être bien plus flexible que ne le suggèrent les schémas mendéliens des manuels. Ces grenouilles d’eau montrent que les génomes des vertébrés peuvent être supprimés sélectivement, copiés et réutilisés comme des blocs modulaires, selon le contexte. En identifiant des gènes réels liés à ce processus, l’étude transforme ce tour reproductif étonnant en un problème moléculaire abordable. Des expériences futures, guidées par ce nouveau catalogue de gènes, testeront comment des ajustements des voies de gestion des chromosomes et de défense du génome peuvent basculer une population entre la reproduction sexuelle ordinaire et la reproduction hybride clonale — un éclairage qui pourrait, en fin de compte, mieux expliquer la fertilité, la stabilité génomique et l’évolution du sexe chez de nombreux autres animaux.
Citation: Plötner, M., Meixner, M., Poustka, A.J. et al. New insights into the molecular basis of gametogenesis in the hybridogenetic water frog Pelophylax esculentus. Sci Rep 16, 5012 (2026). https://doi.org/10.1038/s41598-026-37515-w
Mots-clés: hybridogénèse, grenouilles d’eau, hérédité clonale, exclusion du génome, gamétogenèse