Clear Sky Science · fr
Un modèle d’apprentissage profond cliniquement applicable et généralisable pour les tumeurs médiastinales antérieures sur images CT entre plusieurs institutions
Pourquoi il est important de repérer des tumeurs thoraciques rares
La plupart d’entre nous n’entendront jamais l’expression « tumeur médiastinale antérieure » en consultation, précisément parce que ces masses — touchant souvent la glande thymique située devant le cœur — sont rares. Pourtant, lorsqu’elles se produisent, elles sont difficiles à reconnaître et encore plus difficiles à mesurer avec précision sur des scanners CT, des tâches qui exigent généralement des spécialistes dans de grands centres oncologiques. Cette étude examine si un système d’intelligence artificielle (IA) soigneusement entraîné peut aider des médecins de nombreux hôpitaux à détecter et à délimiter de manière fiable ces tumeurs insaisissables sur des images CT de routine, améliorant potentiellement le diagnostic et la planification des traitements pour des patients qui pourraient autrement passer entre les mailles du filet.
Rassembler des cas rares à l’échelle nationale
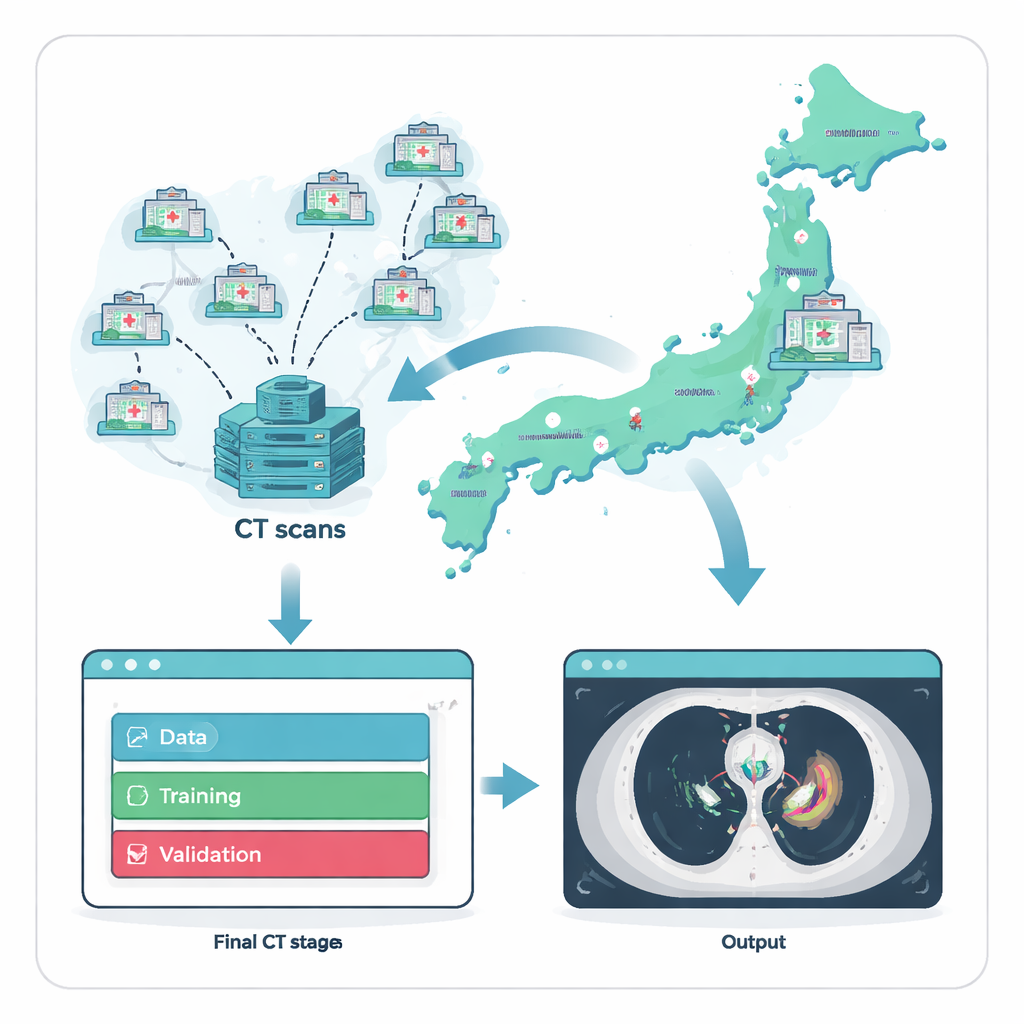
Comme les tumeurs médiastinales antérieures sont peu fréquentes, le premier obstacle est simplement de trouver suffisamment d’exemples pour entraîner un système d’IA. Les chercheurs ont relevé ce défi en collaborant avec le National Cancer Center Hospital du Japon et 135 hôpitaux référents à l’échelle nationale. Sur deux décennies, ils ont constitué 711 scanners thoraciques, chacun provenant d’un patient adulte différent dont le diagnostic tumoral avait été confirmé au microscope. Pour garantir un test juste et réaliste, ils ont divisé les données en trois groupes : un grand ensemble pour l’entraînement, un plus petit pour l’ajustement fin, et un ensemble de test externe entièrement séparé de 164 scanners prélevés dans 121 hôpitaux n’ayant fourni aucune image d’entraînement. Cette séparation stricte imite la façon dont le système se comporterait lorsqu’il serait déployé dans de nouveaux hôpitaux qu’il n’a jamais « vus » auparavant.
Transformer les scanners en matériel d’apprentissage fiable
Un modèle d’IA n’est aussi bon que les exemples dont il apprend, aussi l’équipe a-t-elle fortement investi dans l’étiquetage expert. Pour chaque scanner CT, des spécialistes ont tracé les limites exactes des tumeurs dans la partie antérieure du thorax. Un chirurgien thoracique ou un technologue en radiologie a dessiné les contours initiaux, qui ont ensuite été vérifiés par deux radiologues diagnostiques expérimentés. Tout désaccord a été résolu par discussion, créant une référence de haute qualité reflétant la manière dont des experts interpréteraient les images en pratique. En utilisant une plateforme commerciale d’IA sans code, des cliniciens — sans écrire de code informatique — ont ensuite construit et entraîné un modèle tridimensionnel pour reproduire ces contours d’experts, permettant au personnel médical de piloter directement le processus de développement.
Comment l’IA perçoit les tumeurs en trois dimensions
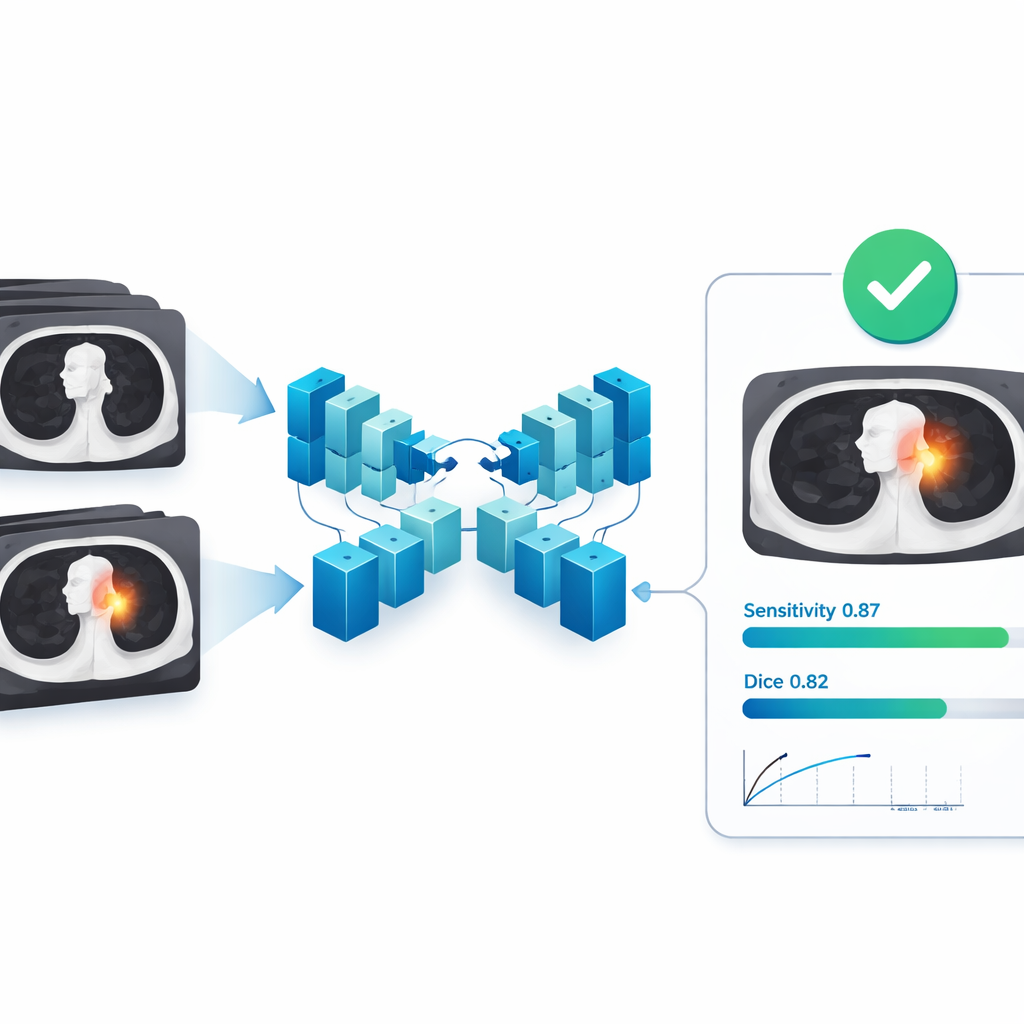
Le noyau du système est une version 3D d’une architecture de réseau neuronal connue sous le nom de U-Net, conçue pour analyser des volumes CT complets plutôt que des coupes isolées. Elle prend une pile d’images thoraciques et prédit, pour chaque petit élément de volume, s’il appartient à une tumeur ou au tissu normal, peignant ainsi en pratique un masque 3D sur la tumeur. Pendant l’entraînement, le modèle a été exposé à des rotations aléatoires, des changements d’échelle et des recadrages des images afin de devenir robuste aux légères différences de position du patient et de paramètres du scanner. Les chercheurs ont ensuite mesuré dans quelle mesure les régions tumorales prédites par le modèle correspondaient aux tracés d’experts, en utilisant des scores d’overlap standard qui récompensent à la fois la précision des limites et la couverture complète du volume tumoral.
Performances à travers de nombreux hôpitaux et types de tumeurs
Sur l’ensemble de test externe provenant de 121 hôpitaux indépendants, le modèle d’IA a montré une forte concordance avec les segmentations expertes. En moyenne, son score d’overlap (Dice) était de 0,82, avec une mesure connexe, l’Intersection over Union, à 0,72 ; la précision et le rappel étaient tous deux autour de 0,82–0,85, ce qui signifie que le modèle étiquetait rarement du tissu normal comme tumoral et capturait la plupart du tissu tumoral. Fait important, ces résultats se maintenaient entre différents fabricants de scanners, tailles de tumeur et types tumoraux, suggérant que le système peut faire face à la variété rencontrée en cliniques réelles. Lorsqu’il a été évalué comme détecteur — se limitant à savoir s’il trouve chaque lésion ou non — le modèle a atteint une sensibilité d’environ 0,87 même sous une règle de correspondance stricte, avec bien moins d’une fausse alerte par scanner en moyenne, un profil particulièrement attractif pour le soutien au dépistage du cancer.
Où le système aide et où l’humain reste crucial
Un examen plus détaillé des réussites et des échecs a révélé un schéma net : l’IA performe mieux sur les tumeurs de plus grande taille et a tendance à avoir des difficultés avec les lésions très petites ou peu denses, les manquant partiellement ou confondant des structures normales voisines comme des vaisseaux sanguins ou des collections liquidiennes. Cela concorde avec l’expérience quotidienne en radiologie, où les petites anomalies ou à faible contraste sont les plus faciles à négliger. Les auteurs soutiennent donc que l’outil est mieux utilisé dans un contexte « human-in-the-loop ». Il peut servir de premier lecteur efficace qui signale les tumeurs probables et en trace les limites, fournissant des volumes prêts à l’emploi pour des tâches comme la planification du traitement et la chirurgie, tandis que les radiologues concentrent leur attention sur la relecture des zones petites, subtiles ou ambiguës.
Ce que cela signifie pour les patients et les outils futurs
Pour le grand public, le message principal est qu’un système d’IA entraîné sur un groupe rare mais sérieux de tumeurs thoraciques peut aider de manière fiable les médecins à repérer et à délimiter ces cancers sur des scanners CT, même dans des hôpitaux qui n’ont jamais contribué à son entraînement. En fournissant des cartes tumorales 3D précises et en maintenant un faible taux de fausses alertes, le modèle pourrait accélérer le diagnostic, soutenir une planification plus précise de la radiothérapie et de la chirurgie, et offrir un filet de sécurité supplémentaire contre les lésions manquées. Dans le même temps, le travail souligne que l’IA ne remplace pas le jugement d’expert — en particulier pour les tumeurs les plus petites et les moins visibles — mais constitue un assistant prometteur qui devient plus puissant à mesure que cliniciens, données d’imagerie et plateformes d’IA faciles d’accès sont réunis.
Citation: Takemura, C., Miyake, M., Kobayashi, K. et al. A clinically applicable and generalizable deep learning model for anterior mediastinal tumors in CT images across multiple institutions. Sci Rep 16, 6774 (2026). https://doi.org/10.1038/s41598-026-37504-z
Mots-clés: tumeurs médiastinales antérieures, apprentissage profond en imagerie CT, segmentation d’images médicales, soutien au diagnostic du cancer, intelligence artificielle en radiologie