Clear Sky Science · fr
Le médicament resmétirom contre la stéato‑hépatite associée à une dysfonction métabolique (MASH) présente une activité étendue sur les récepteurs nucléaires avec un impact fonctionnel minimal
Pourquoi un nouveau médicament pour le foie importe
Des millions de personnes dans le monde vivent avec une forme dangereuse de maladie du foie gras désormais appelée stéato‑hépatite associée à une dysfonction métabolique, ou MASH. Elle peut endommager le foie silencieusement pendant des années et conduire finalement à une fibrose, une insuffisance hépatique ou un cancer. En 2024, un médicament nommé resmétirom est devenu la première thérapie approuvée aux États‑Unis spécifiquement pour la MASH. Cette étude pose une question cruciale pour les patients et les médecins : le resmétirom agit‑il proprement sur sa cible prévue dans le foie, ou touche‑t‑il aussi d’autres commutateurs moléculaires susceptibles d’atténuer ses bénéfices ou de provoquer des effets indésirables ?
Une façon ciblée de brûler la graisse hépatique
Le resmétirom a été conçu pour fonctionner comme une version ciblée de l’hormone thyroïdienne naturelle. Les hormones thyroïdiennes contrôlent la vitesse à laquelle nos cellules utilisent l’énergie, influençant la fréquence cardiaque, la température corporelle et la manière dont les graisses et les sucres sont traités. Elles agissent via deux récepteurs apparentés, appelés alpha et bêta. La forme bêta est la plus abondante dans le foie, tandis que la forme alpha domine dans le cœur et les os. Chez les personnes atteintes de MASH, la signalisation des hormones thyroïdiennes à l’intérieur du foie est souvent lente, même lorsque les tests sanguins paraissent normaux. Le resmétirom vise à « réveiller » le récepteur bêta dans les cellules hépatiques pour brûler davantage de graisse, décomposer le cholestérol et réduire l’accumulation lipidique, tout en épargnant le récepteur alpha afin d’éviter des effets secondaires cardiaques et osseux. 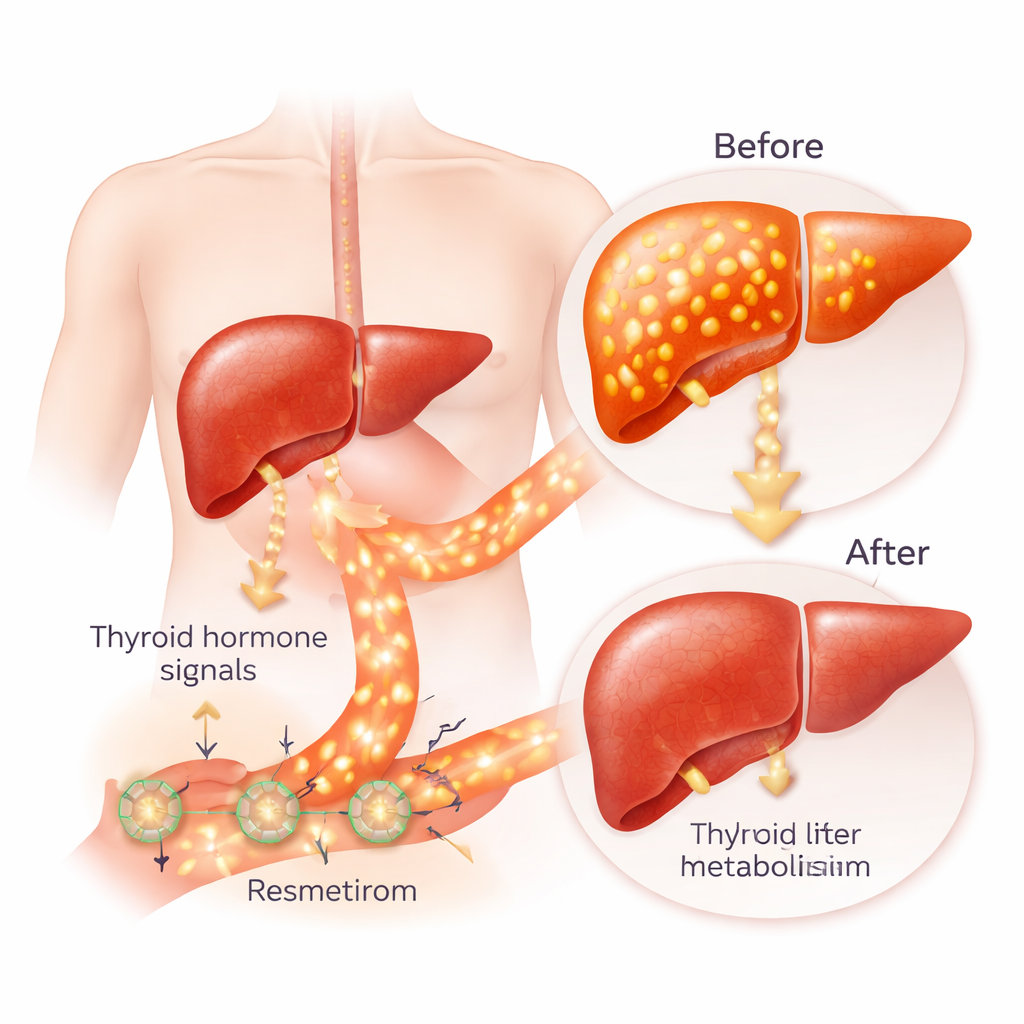
Vérifier la présence de cibles moléculaires indésirables
Parce que le resmétirom doit être administré à des doses relativement élevées pour accomplir son effet, les auteurs se sont demandé s’il pouvait également se lier à d’autres récepteurs nucléaires — des protéines du noyau cellulaire qui servent de commutateurs maîtres pour le métabolisme, la détoxification et les rythmes biologiques. À l’aide de la modélisation informatique et d’une série de tests rapporteurs en cellules, ils ont d’abord vérifié si le resmétirom se comportait comme certains produits de dégradation des hormones thyroïdiennes connus pour activer un autre récepteur appelé PPARγ. La modélisation suggérait que, malgré des formes similaires, le resmétirom s’adapterait mal dans la poche de liaison de PPARγ, et les tests cellulaires ont confirmé que le resmétirom n’activait pas ce récepteur.
Interactions hors cible, mais effets atténués
Les chercheurs ont ensuite soumis le resmétirom à un panel plus large de récepteurs nucléaires impliqués dans le contrôle des lipides et du glucose. Comme prévu, le resmétirom a activé le récepteur thyroïdien bêta plus fortement que la version alpha. Cependant, il a aussi interagi avec plusieurs autres récepteurs : il a bloqué un récepteur appelé CAR, réduit l’activité basale de trois récepteurs ROR, et atténué modestement un facteur protecteur hépatique connu sous le nom de HNF4α. Sur le papier, ces actions hors cible pourraient inquiéter, car tous ces commutateurs contribuent à réguler le métabolisme et la détoxification du foie. Pourtant, l’intensité de ces effets était seulement modérée, et souvent partielle, suggérant que le resmétirom stimule ou gêne ces récepteurs de façon progressive plutôt que de les activer ou les inhiber complètement.
Tester le médicament dans des cellules hépatiques plus réalistes
Pour savoir si ces interactions hors cible ont de l’importance dans des conditions plus proches du vivant, l’équipe s’est tournée vers des cellules cancéreuses hépatiques humaines couramment utilisées comme modèle du tissu hépatique. Ils ont mesuré l’activité de gènes clés connus pour répondre à l’hormone thyroïdienne ainsi qu’à CAR, aux ROR et à HNF4α. Le resmétirom a stimulé des gènes impliqués dans la production de glucose et la détoxification selon un schéma correspondant à l’action de l’hormone thyroïdienne, même si ses actions hors cible auraient dû pousser certains de ces gènes dans la direction opposée. Lorsque les scientifiques ont déclenché la production de graisse dans ces cellules, le resmétirom et l’hormone thyroïdienne naturelle ont tous deux clairement réduit l’accumulation lipidique, tandis que des médicaments ciblant spécifiquement ROR, CAR ou HNF4α seuls avaient peu d’effet. 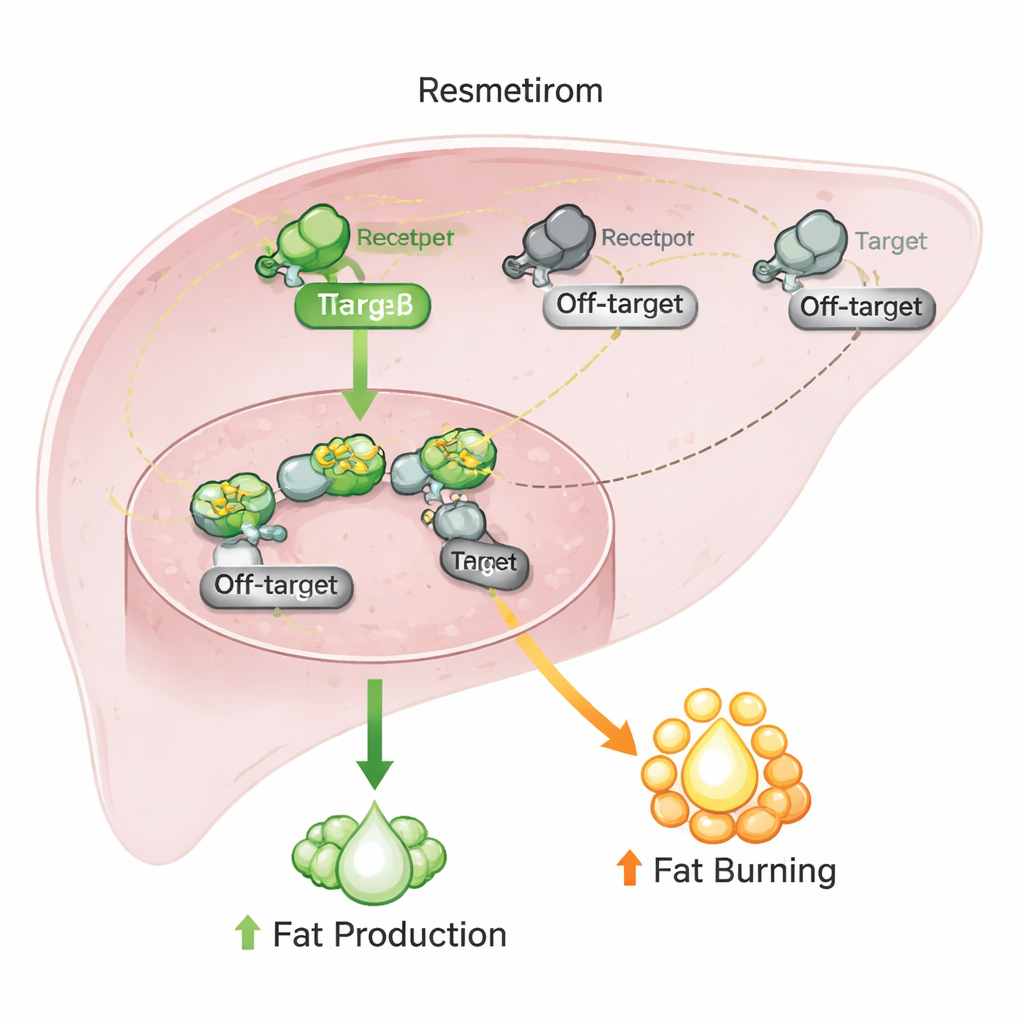
Ce que cela signifie pour les patients et les médicaments futurs
Pris dans leur ensemble, les résultats suggèrent que le resmétirom effleure effectivement plusieurs autres récepteurs nucléaires, mais que son effet principal dans les cellules hépatiques reste guidé par le récepteur thyroïdien bêta visé. En termes pratiques, cela signifie que la capacité du médicament à réduire la graisse hépatique et à améliorer la santé du foie dans la MASH est peu susceptible d’être compromise par ces activités secondaires, du moins dans les systèmes expérimentaux étudiés. Le travail souligne aussi une leçon plus générale : parce que le resmétirom n’est que modérément puissant, il nécessite des concentrations relativement élevées pour agir, ce qui augmente la probabilité d’effets hors cible subtils ailleurs dans l’organisme. Cela renforce l’importance de développer à l’avenir des médicaments basés sur les hormones thyroïdiennes qui se lient plus fortement et plus sélectivement au récepteur bêta, offrant les mêmes bénéfices hépatiques ou supérieurs avec des doses plus faibles et des interactions moléculaires non souhaitées réduites.
Citation: Kärcher, A., Isigkeit, L., Bandomir, N.C. et al. The metabolic dysfunction-associated steatohepatitis (MASH) drug resmetirom exhibits broad nuclear receptor activity with minimal functional impact. Sci Rep 16, 4083 (2026). https://doi.org/10.1038/s41598-026-37494-y
Mots-clés: maladie du foie gras, MASH, resmétirom, récepteur des hormones thyroïdiennes, métabolisme hépatique