Clear Sky Science · fr
Piégeage exceptionnellement sélectif du capteur de tension des canaux NaV1.5 par le Mg-protoporphyrine altère la migration des cellules cancéreuses
Un pigment végétal ouvre une nouvelle piste contre le cancer
Nos cœurs et nos tumeurs pourraient partager une vulnérabilité inattendue : un type particulier de verrou électrique dans la membrane cellulaire nommé NaV1.5. Cette étude montre qu’un cousin naturel des blocs de construction de la chlorophylle chez les plantes, la magnésium‑protoporphyrine IX (MgPpIX), peut fermer ce verrou avec une précision extraordinaire. Ce faisant, elle ralentit nettement le déplacement de certaines cellules cancéreuses — suggérant qu’une molécule inspirée par la chimie de la photosynthèse pourrait aider à maîtriser les métastases sans perturber fortement le cerveau ou les muscles.
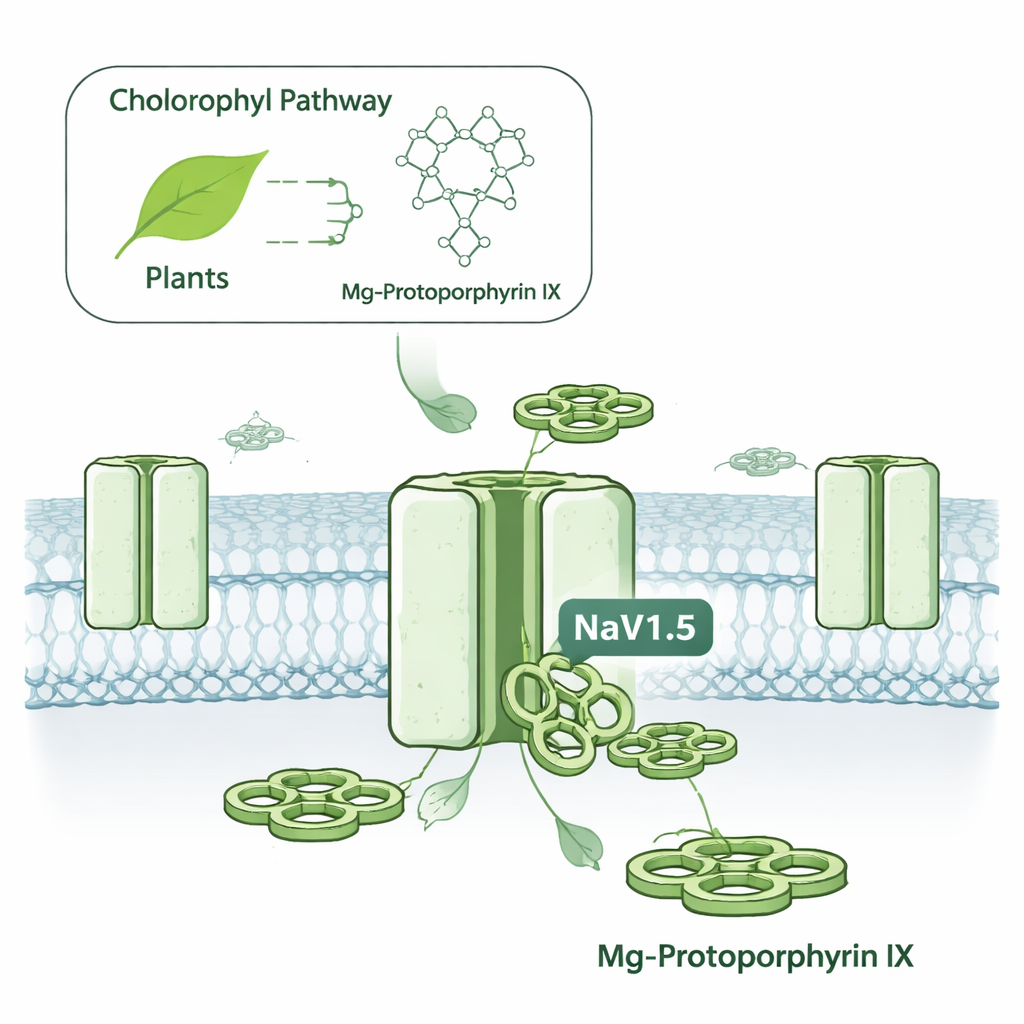
Un interrupteur électrique dissimulé dans les cellules cancéreuses
Les cellules utilisent des canaux sodiques dépendants du voltage comme de petites portes qui s’ouvrent et se ferment pour laisser passer des particules chargées, générant des signaux électriques. NaV1.5 est surtout connu pour son rôle dans les battements cardiaques, où il contribue à déclencher chaque contraction. Mais le même canal se retrouve aussi dans plusieurs cancers, notamment du sein et du côlon, où son activité a été associée à une augmentation de la mobilité et de l’invasivité cellulaire. Cibler NaV1.5 a été difficile parce que la plupart des médicaments contre les canaux sodiques affectent aussi des canaux apparentés dans les nerfs et les muscles squelettiques, au risque d’effets secondaires tels que convulsions, engourdissements ou faiblesse musculaire. Les auteurs ont cherché à savoir si de petites molécules pouvaient distinguer NaV1.5 de ses homologues avec une sélectivité beaucoup plus grande.
Un bloqueur inspiré des plantes avec une précision record
L’équipe a examiné une famille de molécules en anneau appelées protoporphyrines métalliques, qui ressemblent aux cœurs de l’hème dans le sang et de la chlorophylle dans les plantes mais contiennent différents atomes métalliques centraux. Lorsqu’ils ont appliqué diverses variantes aux canaux NaV1.5 humains produits dans des cellules en culture, un composé s’est distingué : le MgPpIX. Il a réduit le courant électrique à travers NaV1.5 d’environ 99 % à des concentrations nanomolaires, soit environ 100 fois plus puissant qu’un homologue à base de fer (hémine). D’autres versions métalliques, comme celles contenant du nickel ou du cuivre, étaient essentiellement inactives. Fait remarquable, le MgPpIX n’a affecté aucune des autres formes de canaux sodiques humains (utilisés par le cerveau, les nerfs périphériques et le muscle squelettique) aux mêmes doses, faisant de sa sélectivité l’une des plus aiguisées jamais rapportées pour cette famille de canaux.
Comment la molécule bloque un minuscule levier de tension
Pour comprendre cette précision inhabituelle, les chercheurs ont combiné modifications génétiques et simulations informatiques. Les canaux sodiques comportent quatre parties répétées, chacune contenant un « capteur de tension » qui change de position lorsque le potentiel de membrane varie. En échangeant des acides aminés individuels entre NaV1.5 et ses homologues insensibles, l’équipe a localisé l’action du MgPpIX au capteur de tension du deuxième domaine, en particulier à deux résidus exposés à l’extérieur de la cellule. Des simulations de dynamique moléculaire dans un environnement membranaire réaliste suggèrent que le MgPpIX s’installe contre ce capteur lorsqu’il est dans sa position de repos, dite « down ». Le noyau métallique chargé positivement du MgPpIX est attiré par une chaîne latérale chargée négativement du canal, tandis que l’anneau plat interagit avec les lipides environnants. Cette liaison semble verrouiller le capteur de tension, l’empêchant de passer à l’état actif « up » et donc maintenant le canal fermé. Fait intéressant, de fortes dépolarisations — comme celles qui se produisent lors d’un battement cardiaque — peuvent temporairement déloger la molécule, un comportement que les auteurs décrivent comme une « dépendance inverse à l’usage ».
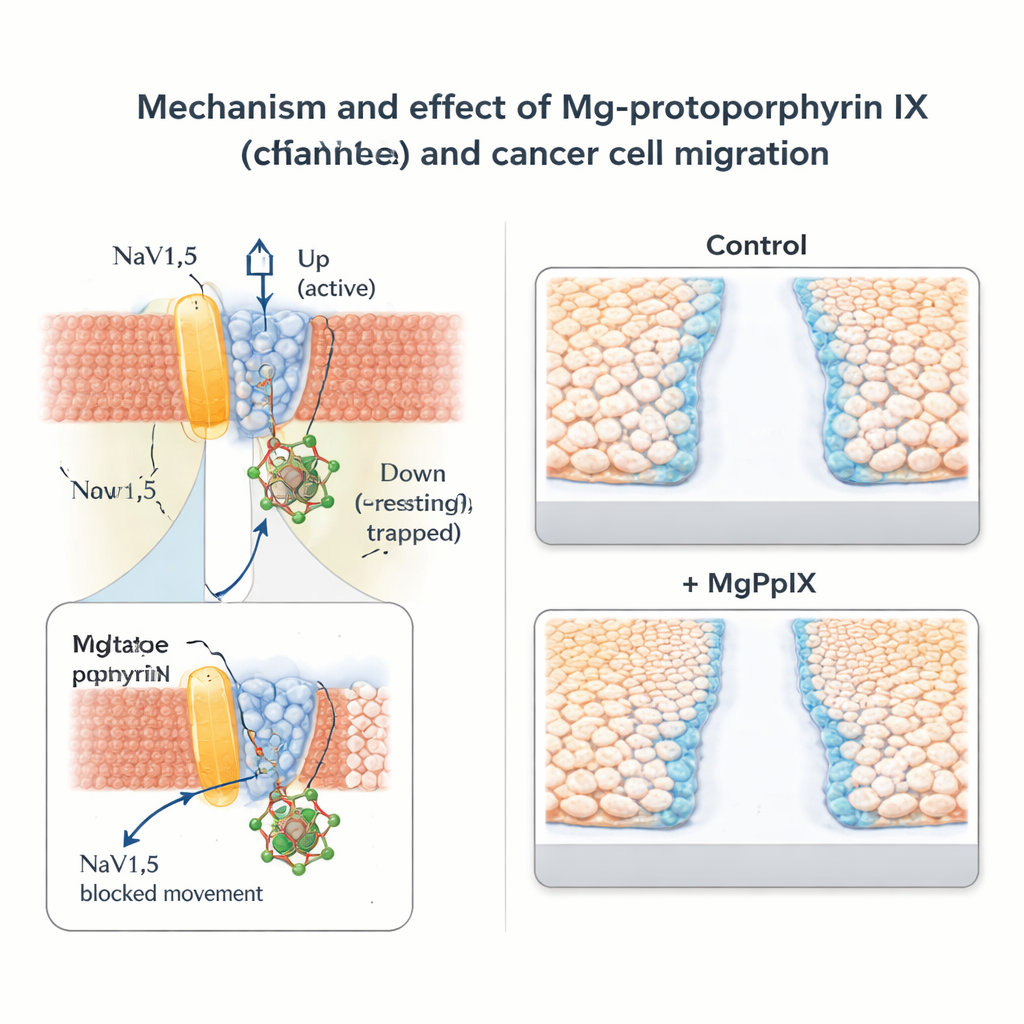
Ralentir la migration des cellules cancéreuses sans bloquer largement les nerfs
L’équipe a ensuite exploré ce que ce frein moléculaire signifie pour le comportement des cancers. Dans des lignées de cancer du sein (MDA‑MB‑231) et du côlon (SW‑480) qui expriment naturellement NaV1.5, le MgPpIX a fortement réduit les courants sodiques et ralenti la migration cellulaire dans des tests standard de « scratch » et de transwell. Plus un protoporphyrinien métallique bloquait NaV1.5, plus il entravait le déplacement cellulaire, renforçant le lien entre l’activité du canal et la motilité. En revanche, des lignées cancéreuses dépourvues de NaV1.5 n’ont montré aucune réponse au MgPpIX, ni sur le plan électrique ni dans les essais de migration, ce qui soutient l’idée que l’effet est hautement spécifique et non généralement toxique. Comparé à la toxine classique des canaux sodiques, la tétrodotoxine, le MgPpIX a obtenu une suppression plus forte de la migration à des concentrations bien plus faibles.
Promesses et prudence pour de futurs médicaments anti‑métastatiques
Pour le non‑spécialiste, le message central est que les chercheurs ont identifié une molécule d’origine végétale qui agit comme une pince de précision sur un verrou électrique de type cardiaque détourné par certains cancers. En piégeant le minuscule levier de tension du verrou dans sa position de repos, le MgPpIX peut fortement réduire la mobilité des cellules cancéreuses en laboratoire tout en épargnant d’autres canaux sodiques essentiels à la sensation et au mouvement. Comme l’activité électrique rapide du cœur peut partiellement lever ce blocage, il pourrait même exister une fenêtre de sécurité où les cellules tumorales sont plus inhibées que les cellules cardiaques. Si le MgPpIX lui‑même n’est peut‑être pas immédiatement prêt à devenir un médicament, son site de liaison et son mécanisme uniques fournissent une feuille de route puissante pour concevoir de futurs médicaments visant à arrêter la dissémination du cancer en ciblant NaV1.5 avec une sélectivité sans précédent.
Citation: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Mots-clés: canaux sodiques, Nav1.5, migration des cellules cancéreuses, molécules dérivées de la chlorophylle, drogues ciblant les canaux ioniques